Was du auf dieser Seite lernst
Du verstehst, warum reines Wasser elektrisch leitfähig ist, und lernst die Autoprotolyse (Eigenprotolyse) des Wassers kennen. Du leitest das Ionenprodukt KW über das Massenwirkungsgesetz her und berechnest die H3O+- und OH−-Konzentration in reinem Wasser bei 25 °C.
1.1 Das Ionenprodukt des Wassers
↑ Zum Vergrößern klicken
✕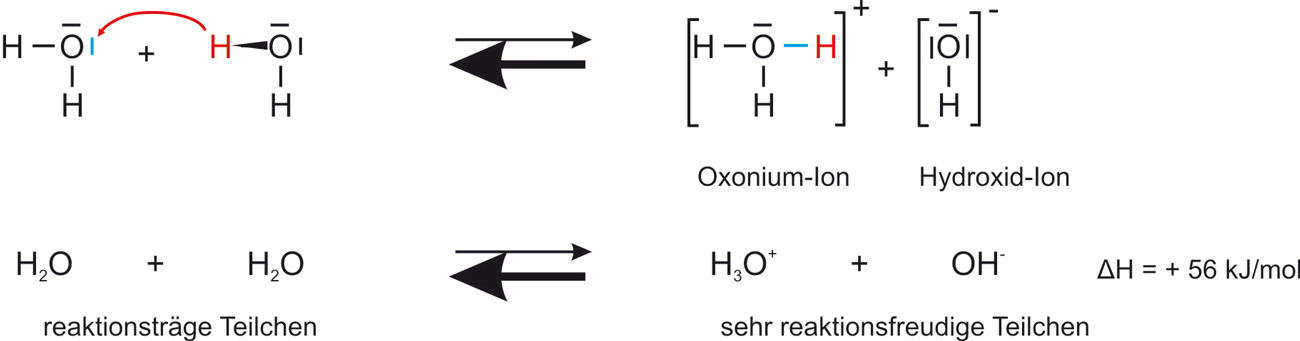
Destilliertes Wasser besitzt eine geringe elektrische Leitfähigkeit – ein Hinweis auf das Vorhandensein von Ionen. Diese Ionen entstehen durch eine Protolyse-Reaktion zweier Wassermoleküle miteinander (Autoprotolyse).
Hinweis zum MWG: Bei der Aufstellung des Massenwirkungsgesetzes steht das Oxonium-Ion in der Regel im Zähler:
Überlegungen – wie groß ist c(H2O)?
- 1 mol Wasser hat die Masse 18,0 g → M(H2O) = 18 g/mol
- 1 L Wasser besitzt bei 25 °C die Masse 997 g
Wie groß ist die Konzentration c(H2O) in Wasser?
| Dichte: | σ = m V ⇒ m = σ · V |
| Stoffmenge: | M = m n ⇒ n = m M = ρ · V M |
| Konzentration: | c = n V = ρ · V M · V = ρ M |
= 55,4 · 6,022 · 1023 Wassermoleküle pro Liter!
Die H2O-Konzentration in Wasser beträgt also konstant 55,4 mol/L.
Durch Leitfähigkeitsmessung lässt sich bei 25 °C bestimmen:
Diese Werte in das MWG einsetzen:
KC ist extrem klein → das Gleichgewicht liegt weitgehend auf der linken Seite → Die Konzentration von H2O ist daher auch bei Gleichgewichtsverschiebungen praktisch konstant. Sie kann mit KC zu einer neuen Konstanten KW (Ionenprodukt des Wassers) vereinigt werden:
KC · c²(H2O) = KW = c(H3O+) · c(OH−) = 1,00 · 10−14 mol²/L²
√KW = c(H3O+) = c(OH−) = (1,00 · 10−14 mol²/L²)½ = 1,00 · 10−7 mol/L
⚠️ Achtung: In reinem Wasser und in neutralen wässrigen Lösungen beträgt die Konzentration der Oxonium-Ionen und der Hydroxid-Ionen jeweils 10−7 mol/L.
Es haben also nur 2 Wassermoleküle von einer Milliarde zu einem Oxonium-Ion und einem Hydroxid-Ion reagiert.
Auf einen Blick – die wichtigsten Aussagen
Autoprotolyse
H2O + H2O ⇌ H3O+ + OH−
Gleichgewicht liegt links · endotherm (ΔH = +56 kJ/mol)
Ionenprodukt KW
KW = c(H3O+) · c(OH−) = 10−14 mol²/L² bei 25 °C
Neutrales Wasser
c(H3O+) = c(OH−) = 10−7 mol/L
→ pH = 7
Gleichgewichtslage
KC = 3,26 · 10−18 → extrem klein
Nur 2 von 109 H2O-Molekülen reagieren
Häufige Fragen zur Autoprotolyse
Warum leitet destilliertes Wasser Strom, obwohl keine Salze gelöst sind?
Durch die Autoprotolyse bilden sich in jeder wässrigen Lösung stets geringe Mengen an Oxonium-Ionen (H3O+) und Hydroxid-Ionen (OH−). Diese geladenen Teilchen ermöglichen einen sehr schwachen Stromfluss. Da das Gleichgewicht aber weit auf der linken Seite liegt, ist die Leitfähigkeit von reinem Wasser sehr gering – messbar, aber kaum spürbar.
Was ist der Unterschied zwischen KC und KW?
KC ist die allgemeine Gleichgewichtskonstante aus dem MWG: KC = c(H3O+) · c(OH−) / c²(H2O). Da die Wasserkonzentration mit 55,4 mol/L praktisch konstant ist, wird sie in KC eingearbeitet: KW = KC · c²(H2O). KW enthält dann nur noch die Ionenkonzentrationen und ist einfacher zu handhaben.
Ändert sich KW mit der Temperatur?
Ja – KW ist temperaturabhängig. Bei 25 °C gilt KW = 10−14 mol²/L². Da die Autoprotolyse endotherm ist, verschiebt sich das Gleichgewicht bei höherer Temperatur nach rechts → KW wird größer. Bei 37 °C (Körpertemperatur) gilt KW ≈ 2,4 · 10−14 mol²/L², der neutrale pH-Wert liegt dann bei ca. 6,8 – obwohl die Lösung chemisch neutral ist!
Was passiert mit c(OH−), wenn ich eine Säure zugebe?
Gibt man eine Säure hinzu, steigt c(H3O+). Da KW = c(H3O+) · c(OH−) bei konstanter Temperatur konstant bleibt, sinkt c(OH−) entsprechend. Beispiel: c(H3O+) = 10−3 mol/L → c(OH−) = 10−14 / 10−3 = 10−11 mol/L. → Kapitel 2: pH-Wert
Warum kann c(H2O) als Konstante behandelt werden?
KC = 3,26 · 10−18 ist extrem klein – das Gleichgewicht liegt fast vollständig auf der linken Seite. Von einer Milliarde Wassermolekülen reagieren nur etwa 2. Die Änderung von c(H2O) ist daher vernachlässigbar klein, c(H2O) ≈ 55,4 mol/L bleibt praktisch konstant und kann in KW eingearbeitet werden.
Lernkarten – Autoprotolyse und Ionenprodukt
Klicke auf eine Karte, um die Antwort zu sehen.
Was versteht man unter der Autoprotolyse des Wassers?
Zwei H2O-Moleküle reagieren miteinander – eines gibt ein Proton ab, das andere nimmt es auf:
H2O + H2O ⇌ H3O+ + OH−
Wie lautet das Ionenprodukt des Wassers KW bei 25 °C?
KW = c(H3O+) · c(OH−)
= 1,00 · 10−14 mol²/L²
(gilt für alle wässrigen Lösungen bei 25 °C)
Welche Ionenkonzentration herrscht in neutralem Wasser bei 25 °C?
c(H3O+) = c(OH−)
= 1,00 · 10−7 mol/L
→ pH = 7 (neutral)
Warum wird c(H2O) in KW „eingebaut"?
c(H2O) ≈ 55,4 mol/L = konstant (GG liegt weit links, KC = 3,26 · 10−18)
→ KW = KC · c²(H2O)
Berechne c(OH−), wenn c(H3O+) = 1,00 · 10−4 mol/L (25 °C).
c(OH−) =
KW / c(H3O+)
= 10−14 / 10−4
= 10−10 mol/L
Weiter im Kapitel Säure-Base
↑ Übersicht Säure-Base-Reaktionen → Kapitel 2: pH-Wert → Kapitel 3: Protolyse-Reaktionen → Kapitel 4: pK-Werte
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Du lernst den pH-Wert als negativen dekadischen Logarithmus der Oxonium-Ionenkonzentration kennen und verstehst seine Beziehung zum pOH-Wert. Du kannst aus einem gegebenen pH-Wert die c(H3O+) berechnen – und umgekehrt – und erkennst anhand der pH-Skala, ob eine Lösung sauer, neutral oder alkalisch ist.
Um das Ionenprodukt KW übersichtlicher beschreiben zu können, führt man den pH-Wert (potentia hydrogenii), den pOH-Wert und den pKW-Wert ein.
Der pH-Wert ist der negative dekadische Logarithmus der Oxonium-Ionenkonzentration.
pH = −lg c(H3O+)
c(H3O+) = 10−pH mol/L
pOH = −lg c(OH−)
pH + pOH = pKW
pH + pOH = 14 (bei 25 °C)
Folgende Werte gelten bei 25 °C:
| Größe | pH = 0 sauer |
pH = 6 | pH = 7 neutral |
pH = 8 | pH = 14 alkalisch |
Einheit |
|---|---|---|---|---|---|---|
| c(H3O+) | 100 | 10−6 | 10−7 | 10−8 | 10−14 | mol/L |
| c(OH−) | 10−14 | 10−8 | 10−7 | 10−6 | 100 | mol/L |
| pH | 0 | 6 | 7 | 8 | 14 | |
| pOH | 14 | 8 | 7 | 6 | 0 |
Zur Kennzeichnung, ob es sich um eine saure, neutrale oder alkalische Lösung handelt, reicht es vollständig aus, nur die Konzentration einer Ionensorte anzugeben (i. d. R. die Oxonium-Ionen-Konzentration).
Beispiele:
- pH = 2: c(H3O+) = 10−2 mol/L = 0,01 mol/L
- pH = 12: c(H3O+) = 10−12 mol/L = 0,000 000 000 001 mol/L
In einer alkalischen Lösung: c(OH−) > 10−7 mol/L ⇒ pH > 7
In einer neutralen Lösung: c(H3O+) = c(OH−) = 10−7 mol/L ⇒ pH = 7
Auf einen Blick – die wichtigsten Aussagen
pH-Definition
pH = −lg c(H3O+)
c(H3O+) = 10−pH mol/L
pKW-Beziehung
pH + pOH = 14 (bei 25 °C)
pOH = −lg c(OH−)
Neutral
pH = 7 bei 25 °C
c(H3O+) = c(OH−) = 10−7 mol/L
Merkhilfe
Kleiner pH → viele H3O+ → sauer
Großer pH → viele OH− → alkalisch
Häufige Fragen zum pH-Wert
Warum ist der pH-Wert ein negativer Logarithmus?
Die Konzentrationen von H3O+-Ionen in wässrigen Lösungen liegen typischerweise zwischen 100 und 10−14 mol/L – also sehr kleine Zahlen. Der negative Logarithmus macht diese Werte zu handlichen positiven Zahlen zwischen 0 und 14. Beispiel: c(H3O+) = 10−3 mol/L → pH = −lg(10−3) = 3.
Wie berechne ich c(H3O+) aus einem pH-Wert?
Umkehrung der pH-Definition: c(H3O+) = 10−pH mol/L. Beispiele: pH = 2 → c = 10−2 = 0,01 mol/L · pH = 9 → c = 10−9 = 0,000 000 001 mol/L. Bei nichtganzzahligen pH-Werten (z. B. pH = 4,75) wird der Taschenrechner benötigt: c = 10−4,75 ≈ 1,78 · 10−5 mol/L. → Mehr dazu: Kapitel 4 (pK-Werte)
Was bedeutet pH + pOH = 14?
Da KW = c(H3O+) · c(OH−) = 10−14 (bei 25 °C), gilt nach Logarithmieren: −lg(c(H3O+)) + (−lg(c(OH−))) = 14, also pH + pOH = 14. Kennt man einen der beiden Werte, lässt sich der andere sofort berechnen. → Zurück: Ionenprodukt KW
Ist pH = 7 immer gleich neutral?
Nur bei 25 °C! Da KW temperaturabhängig ist, verschiebt sich der neutrale pH-Wert mit der Temperatur. Bei 37 °C (Körpertemperatur) liegt der neutrale pH-Wert bei ca. 6,8 – obwohl c(H3O+) = c(OH−) gilt und die Lösung chemisch neutral ist. „Neutral" bedeutet immer: gleiche Konzentrationen beider Ionen, nicht zwingend pH = 7.
Welcher pH-Bereich kommt im Alltag vor?
Typische Beispiele: Magensäure pH ≈ 1–2 · Zitronensaft pH ≈ 2–3 · Kaffee pH ≈ 5 · Blut pH ≈ 7,35–7,45 (streng gepuffert) · Meerwasser pH ≈ 8,1 · Seifenwasser pH ≈ 9–10 · Natronlauge pH ≈ 13. Der biologisch verträgliche Bereich für Blut ist extrem eng – Abweichungen von ±0,4 sind lebensbedrohlich. → Kapitel 5: Indikatoren
Lernkarten – pH-Wert und pH-Skala
Klicke auf eine Karte, um die Antwort zu sehen.
Wie lautet die Definition des pH-Werts?
pH = −lg c(H3O+)
→ negativer dekadischer Logarithmus der Oxonium-Ionenkonzentration
Welche c(H3O+) hat eine Lösung mit pH = 3?
c(H3O+) = 10−pH
= 10−3 mol/L = 0,001 mol/L
Wie lautet die Beziehung zwischen pH und pOH (bei 25 °C)?
pH + pOH = pKW = 14
Beispiel: pH = 4 → pOH = 10
→ c(OH−) = 10−10 mol/L
Wann ist eine Lösung sauer, neutral oder alkalisch?
Sauer: pH < 7 · c(H3O+) > 10−7
Neutral: pH = 7
Alkalisch: pH > 7 · c(OH−) > 10−7
c(H3O+) = 0,001 mol/L. Berechne pH und c(OH−).
pH = −lg(10−3) = 3
pOH = 14 − 3 = 11
c(OH−) = 10−11 mol/L
Weiter im Kapitel Säure-Base
↑ Übersicht Säure-Base ← Kap. 1: Autoprotolyse → Kap. 3: Protolyse-Reaktionen → Kap. 4: pK-Werte
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Chlorwasserstoff-Gas (HCl) reagiert mit Wasser zu Oxonium- und Chlorid-Ionen – das ist eine Protolyse-Reaktion nach Brønsted. Du lernst den Springbrunnenversuch zu erklären, Reaktionsgleichungen in Summenformel- und Lewis-Schreibweise aufzustellen und das Protolysen-Schema (Bergab-Reaktion) zu lesen und anzuwenden.
3 Protolyse-Reaktionen
3.1 Chlorwasserstoff-Gas und Wasser (Springbrunnen)
Chlorwasserstoff: Summenformel HCl · polare Atombindung · Gas · stechender Geruch
Wasser: Summenformel H2O · polare Atombindung · Flüssigkeit · geruchslos
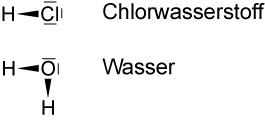
Lewis-Formeln
| H — Cl: | Chlorwasserstoff |
| H — O: | Wasser |
| | | |
| H |
a) Versuch:
↑ Zum Vergrößern klicken
✕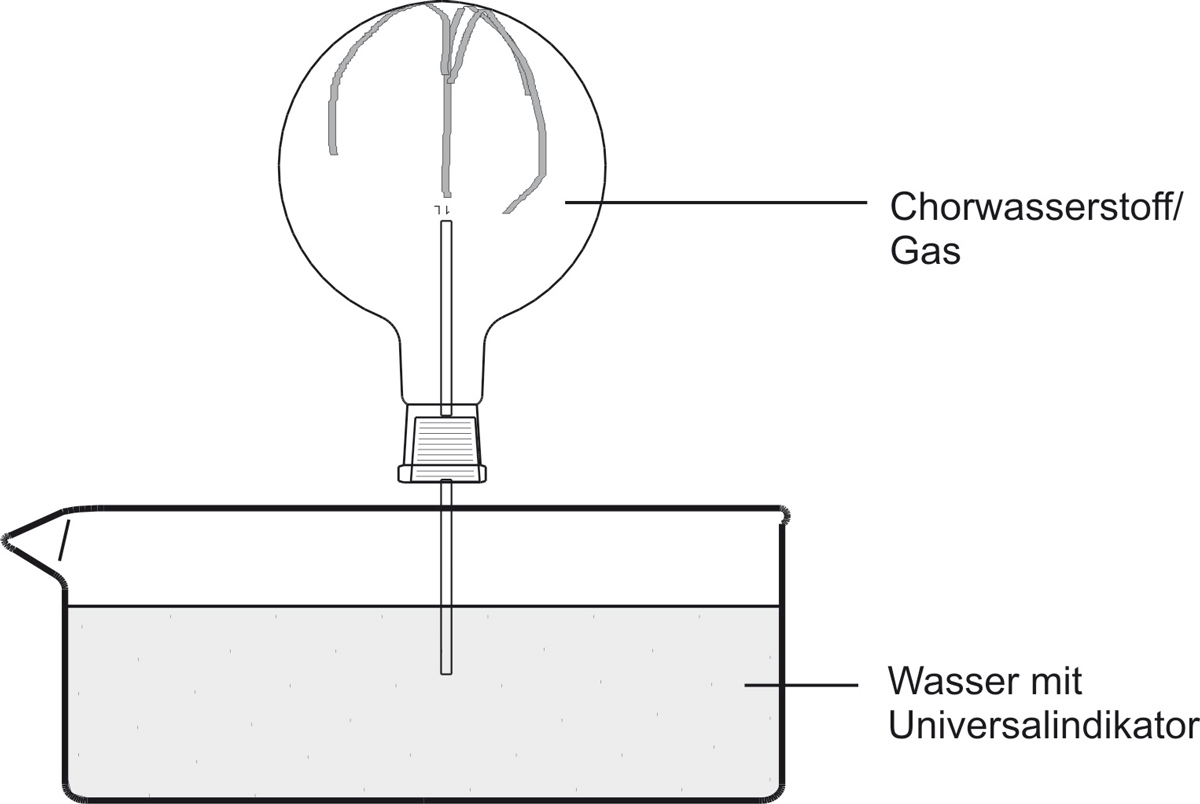
⚠️ Hinweis: Im Bild steht „Chorwasserstoff" – korrekte Schreibweise: Chlorwasserstoff.
b) Beobachtung:
Das Wasser „schießt" bergauf in den Rundkolben. Die Indikatorfarbe schlägt nach rot/gelb um. Die rote wässrige Lösung ist geruchlos.
c) Reaktionsgleichung – Struktur/Lewisformel:
Es gibt zwei mögliche Reaktionsgleichungen (wenn man zunächst die Säurestärke vernachlässigt). Welche zwei Reaktionsgleichungen sind das?
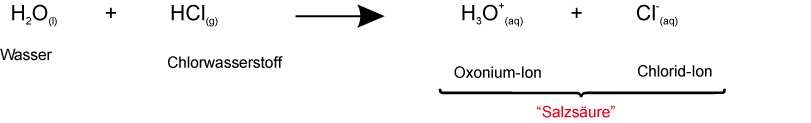
{slider title="Lösung" open="false" class="icon"}1. Möglichkeit – HCl als Säure, H2O als Base (korrekte Reaktion):
H2O(l) + HCl(g) ⟶ H3O+(aq) + Cl−(aq)
Wasser Chlorwasserstoff Oxonium-Ion Chlorid-Ion
⇒ bildet zusammen: „Salzsäure"
2. Möglichkeit – H2O als Säure, HCl als Base:
↑ Zum Vergrößern klicken
✕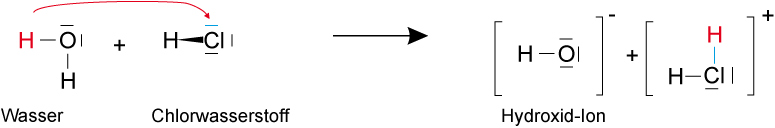
Chlorwasserstoff ist die stärkere Säure, Hydroxid-Ion (OH−) wäre eine sehr starke Base. Durch Elektrolyse wird die 1. Möglichkeit bestätigt: HCl wirkt als Säure.
{/sliders}Nachweis der gebildeten Ionen:
- Leitfähigkeitsmessung: Die Lösung leitet elektrischen Strom → Ionen sind vorhanden.
- Elektrolyse: An der Anode (Pluspol) entsteht Cl2-Gas → Chlorid-Ionen (Cl−) müssen vorliegen.
↑ Zum Vergrößern klicken
✕
- Indikator: Bromthymolblau färbt gelb → Oxonium-Ionen (H3O+) sind vorhanden.
Komplette Lösung:
{slider title="Lösung" open="false" class="icon"}Reaktionsgleichung (Lewis-Formel):
↑ Zum Vergrößern klicken
✕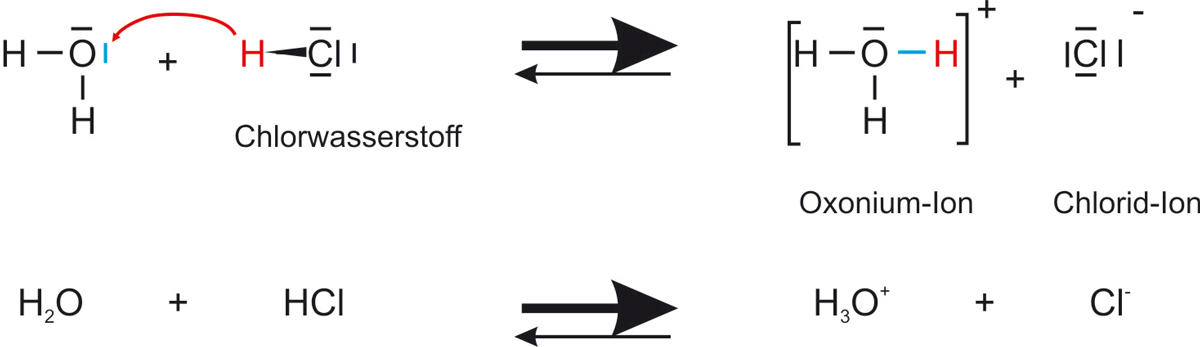
Reaktionsgleichung (Summenformel):
H2O(l) + HCl(g) ⇌ H3O+(aq) + Cl−(aq)
Wasser Chlorwasserstoff Oxonium-Ion Chlorid-Ion
„Salzsäure"

Verdünnte Salzsäure enthält hydratisierte Oxonium- und Chlorid-Ionen sowie Wassermolekule.
d) Protolysen-Schema:
↗ Originalbild des Protolysen-Schemas ansehen
✕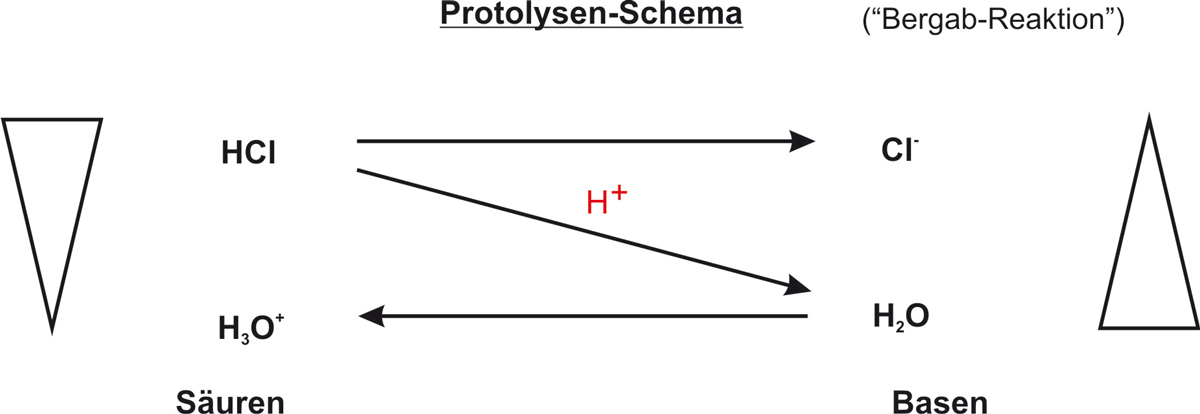 {/sliders}
{/sliders}
e) Erklärung:
Chlorwasserstoff-Gas reagiert mit Wasser zu Oxonium-Ionen (H3O+) und Chlorid-Ionen (Cl−). Im Kolben entsteht durch das vollständige Auflösen ein Unterdruck. Die H3O+-Ionen färben den Universalindikator bzw. Bromthymolblau rot/gelb.
Salzsäure = wässrige Lösung des Gases Chlorwasserstoff
Leitet man sehr viel HCl-Gas in Wasser ein, reagieren nicht mehr alle HCl-Moleküle mit H2O. Diese HCl-Moleküle liegen „gelöst" vor – es entsteht rauchende bzw. konzentrierte Salzsäure.
| Leitfähigkeit | Geruch | Indikatorpapier | Teilchen | |
|---|---|---|---|---|
| Verdünnte Salzsäure | + | − | rot | H2O, H3O+, Cl− |
| Rauchende Salzsäure | + | + | rot | H2O, H3O+, Cl−, HCl |
Auf einen Blick – die wichtigsten Aussagen
Protolyse (Brønsted)
Eine Protolyse ist die Übertragung eines Protons (H+) vom Protonendonator (Säure) auf den Protonenakzeptor (Base).
Springbrunnen
HCl löst sich vollständig in H2O auf → Ionen bilden sich → Unterdruck entsteht → Atmosphärendruck drückt Wasser hoch.
Bergab-Reaktion
Das Proton wandert von der stärkeren Säure (HCl) zur stärkeren Base (H2O) – immer zur schwächeren Säure/Base hin.
Salzsäure
Salzsäure = wässrige Lösung von HCl. Enthält H3O+, Cl− und H2O; konzentriert zusätzlich gelöstes HCl.
Häufige Fragen – Protolyse-Reaktionen
Warum schießt das Wasser beim Springbrunnenversuch in den Kolben?
HCl-Gas reagiert sofort mit dem eingetretenen Wasser zu H3O+- und Cl−-Ionen. Dadurch sinkt der Gasdruck im Kolben stark. Der Atmosphärendruck drückt das Wasser durch das Glasrohr nach oben – der „Springbrunnen-Effekt". Die Indikatorfarbe zeigt: die Lösung ist sauer (H3O+-Ionen).
Was ist der Unterschied zwischen Chlorwasserstoff und Salzsäure?
Chlorwasserstoff (HCl) ist ein farbloses Gas mit stechendem Geruch. Salzsäure ist die wässrige Lösung dieses Gases: HCl löst sich in H2O und bildet dabei Oxonium-Ionen (H3O+) und Chlorid-Ionen (Cl−). Verdünnte Salzsäure ist geruchlos, da kein HCl mehr als Gas vorliegt.
Was versteht man unter einer Protolyse nach Brønsted?
Nach Brønsted ist eine Säure ein Protonendonator (gibt H+ ab) und eine Base ein Protonenakzeptor (nimmt H+ auf). Eine Protolyse ist die Übertragung eines Protons. Das Protolysen-Schema zeigt: Die Reaktion läuft stets von der stärkeren Säure/Base zu den schwächeren Produkten – die sogenannte Bergab-Reaktion. Mehr dazu: Brønsted-Definition (Kl. 9).
Wie weist man Chlorid-Ionen in Salzsäure nach?
Durch Elektrolyse: An der Anode (Pluspol) entwickelt sich Chlorgas (Cl2), das durch Oxidation von Cl− entsteht – direkter Nachweis. Außerdem fällt bei Zugabe von Silbernitrat-Lösung (AgNO3) ein weißer Niederschlag aus Silberchlorid (AgCl) aus.
Was enthält rauchende Salzsäure im Vergleich zu verdünnter Salzsäure?
Verdünnte Salzsäure enthält nur H2O, H3O+ und Cl− – alles HCl hat mit Wasser reagiert. In konzentrierter (rauchender) Salzsäure ist so viel HCl gelöst, dass nicht mehr alle Moleküle mit H2O reagieren können. Sie liegen als undissoziiertes HCl vor → stechender Geruch, „Rauchen" an feuchter Luft. Mehr zur Konzentration: Konzentration von Lösungen (Kl. 9).
Lernkarten – Protolyse von Chlorwasserstoff
Klicke auf eine Karte, um die Antwort zu sehen.
Was ist eine Protolyse-Reaktion nach Brønsted?
Übertragung eines Protons (H+) vom Protonendonator (Säure) auf den Protonenakzeptor (Base).
Erkläre den Springbrunnenversuch mit HCl!
HCl löst sich schnell in H2O → Ionenbildung → Gasdruck sinkt → Atmosphärendruck drückt Wasser nach oben in den Kolben.
Warum wirkt HCl als Säure und H2O als Base?
HCl ist die stärkere Säure. Im Protolysen-Schema reagiert immer die stärkere Säure mit der stärkeren Base (Bergab-Reaktion).
Welche Teilchen enthält verdünnte vs. rauchende Salzsäure?
Verdünnt: H2O, H3O+, Cl−
Rauchend: zusätzlich gelöstes HCl → stechender Geruch
Berechne: Welche Masse HCl (M = 36,5 g/mol) steckt in 250 mL 0,2-mol/L-Salzsäure?
n = c · V = 0,2 mol/L · 0,25 L = 0,05 mol
m = n · M = 0,05 mol · 36,5 g/mol = 1,825 g
Weiter im Kapitel Säure-Base-Reaktionen
→ 3.2 Chlorwasserstoff und Ammoniak → Brønsted-Definition → Stärke von Säuren und Basen
🔗 Verwandte Themen: pH-Wert und Oxonium-Ionen · Konzentration von Lösungen · Neutralisation
ⓘ Die verlinkten Seiten wurden nicht gegen die aktuelle Sitemap verifiziert – bitte vor dem Veröffentlichen prüfen.
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Ammoniak ist ein Gas, das sich außergewöhnlich gut in Wasser löst – das zeigt der Springbrunnenversuch eindrucksvoll. Du lernst, wie Ammoniak mit Wasser nach der Brønsted-Theorie reagiert (Protolyse), warum dabei eine basische Lösung entsteht, und verstehst im Exkurs, warum Sprudelwasser sauer ist und wie man daraus den pH-Wert berechnet.
Grundlagen aus der 9. Klasse
Die Grundlagen zur Brønsted-Theorie (Protonendonator / Protonenakzeptor) hast du bereits in der 9. Klasse kennengelernt: → Brønsted-Theorie (Kl. 9) · → Säure-Base-Reaktionen (Kl. 9)
3.2 Ammoniak-Gas + Wasser (Springbrunnen 2)
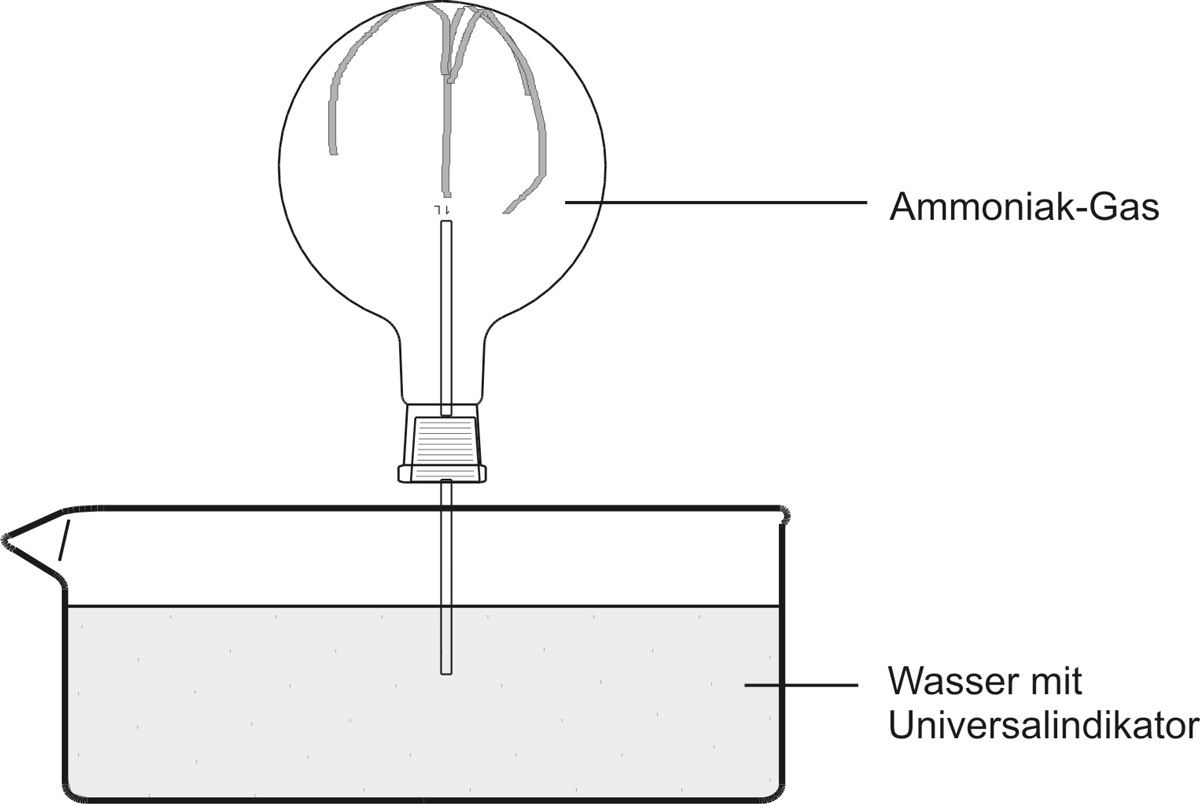
a) Versuch
↑ Zum Vergrößern klicken
✕
b) Beobachtung
Das Wasser „schießt" bergauf in den Rundkolben. Die Indikatorfarbe schlägt nach blau um. Die blaue wässrige Lösung riecht nach Ammoniak.
c) Erklärung
Ammoniak-Gas löst sich sehr gut in Wasser und reagiert teilweise mit Wasser. Im Kolben entsteht durch das Lösen des Gases ein starker Unterdruck. Die entstehenden Hydroxid-Ionen (OH⁻) färben den Universalindikator blau.
d) Reaktionsgleichung (mit Strukturformeln und Summenformeln)
Versuche die Gleichung erst selbst zu formulieren!
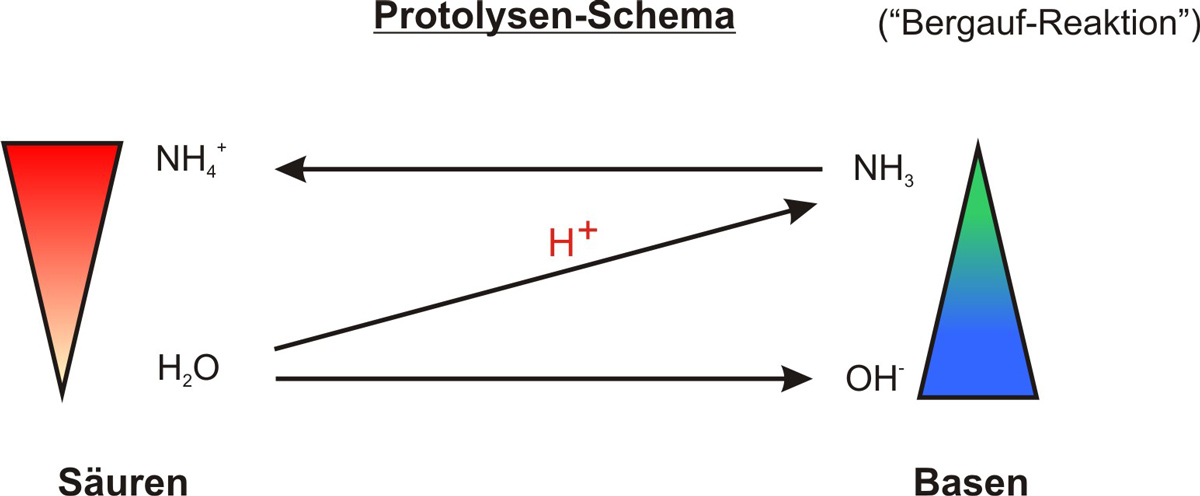
Formuliere nun das Protolyseschema:
Exkurs: Was macht den Sprudel sauer?
Kohlenstoffdioxid reagiert beim Lösen in Wasser im Gleichgewicht zu Kohlensäure:
CO₂ (g) + H₂O (l) ⇌ „H₂CO₃" (aq) – instabil (→ Erlenmeyer-Regel: zwei OH-Gruppen am selben C-Atom sind nicht beständig)
1. Protolysestufe: H₂CO₃ (aq) + H₂O (l) ⇌ HCO₃⁻ (aq) + H₃O⁺ (aq)
2. Protolysestufe: HCO₃⁻ (aq) + H₂O (l) ⇌ CO₃²⁻ (aq) + H₃O⁺ (aq)
Nachweis der H₃O⁺-Ionen durch:
- Geschmack (sauer)
- pH-Papier
- pH-Meter
Messwert: pH(Sprudel) = 5,1
Berechnung der Oxoniumionen-Konzentration:
pH = −lg c(H₃O⁺)
c(H₃O⁺) = 10−pH = 10−5,1 ≈ 7,9 · 10−6 mol/L
Auf einen Blick – die wichtigsten Aussagen
Springbrunneneffekt
NH₃ löst sich so gut in Wasser, dass im Kolben ein starker Unterdruck entsteht – das Wasser „schießt" nach oben in den Rundkolben.
Protolyse (Brønsted)
NH₃ + H₂O ⇌ NH₄⁺ + OH⁻. NH₃ ist Protonenakzeptor (Base), H₂O ist Protonendonator (Säure). Lösung basisch (pH > 7).
Erlenmeyer-Regel
H₂CO₃ ist instabil – zwei OH-Gruppen am selben C-Atom sind nicht beständig. H₂CO₃ zerfällt sofort in CO₂ und H₂O.
pH-Rechnung
pH = −lg c(H₃O⁺) · c(H₃O⁺) = 10−pH
Sprudel: pH 5,1 → c(H₃O⁺) ≈ 7,9 · 10−6 mol/L
Häufige Fragen – Ammoniak und Wasser
Warum steigt beim Springbrunnenversuch das Wasser von selbst auf?
Ammoniak löst sich außergewöhnlich gut in Wasser (ca. 700 Liter NH₃ in 1 Liter Wasser bei Raumtemperatur). Sobald Wasser mit dem Ammoniak-Gas in Berührung kommt, löst sich das Gas nahezu vollständig. Der Gasdruck im Kolben fällt schlagartig ab – es entsteht ein starker Unterdruck. Der Atmosphärendruck drückt daraufhin das Wasser durch die Glasspitze nach oben in den Kolben.
Ist NH₃ in Wasser eine Säure oder eine Base?
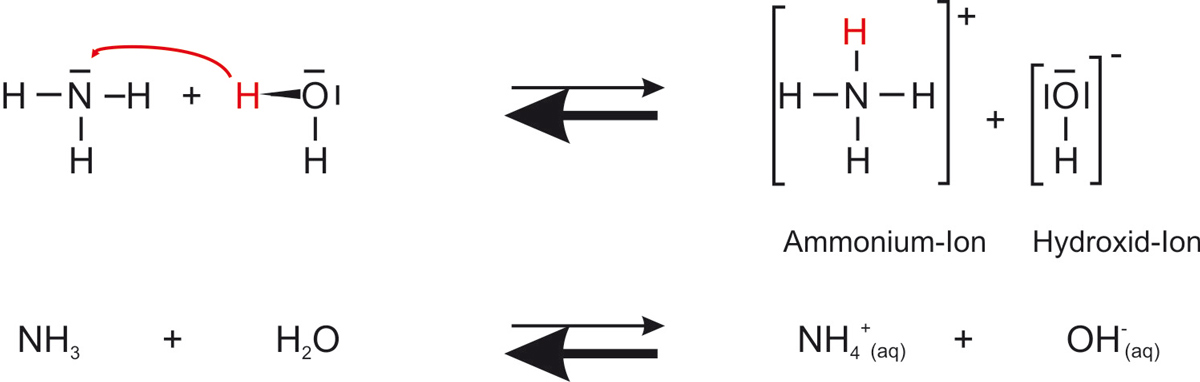
Nach Brønsted ist NH₃ eine Base: Es nimmt ein Proton (H⁺) vom Wasser auf und bildet das Ammoniumion NH₄⁺. Gleichzeitig gibt Wasser ein Proton ab und wird zur konjugierten Base OH⁻. Die Reaktion verläuft als Gleichgewicht:
NH₃ (aq) + H₂O (l) ⇌ NH₄⁺ (aq) + OH⁻ (aq)
Da OH⁻-Ionen entstehen, ist die Lösung basisch (pH > 7), was der Universalindikator durch Blaufärbung anzeigt.
Was bedeutet „konjugiertes Säure-Base-Paar"?
Ein konjugiertes Säure-Base-Paar unterscheidet sich nur um ein Proton H⁺. Bei der Ammoniak-Protolyse gibt es zwei solche Paare:
- NH₄⁺ / NH₃ – NH₄⁺ ist die Säure, NH₃ die konjugierte Base
- H₂O / OH⁻ – H₂O ist die Säure, OH⁻ die konjugierte Base
Das Protolyseschema stellt diese Paare mit Pfeilen dar und zeigt, in welche Richtung das Proton wandert. Mehr dazu auf der Seite → Brønsted-Theorie.
Was ist die Erlenmeyer-Regel und wozu braucht man sie?
Die Erlenmeyer-Regel besagt: Verbindungen, bei denen zwei Hydroxyl-Gruppen (OH) an demselben Kohlenstoffatom gebunden sind, sind instabil und wandeln sich spontan um. Kohlensäure H₂CO₃ hätte formal zwei OH-Gruppen am gleichen C-Atom – sie ist daher so instabil, dass sie sofort in CO₂ und H₂O zerfällt. Diese Regel erklärt, warum im Sprudelwasser kein stabiles H₂CO₃ vorliegt, sondern CO₂ im Gleichgewicht mit Wasser steht und dabei H₃O⁺-Ionen entstehen.
Wie berechnet man aus dem pH-Wert die Oxoniumionen-Konzentration?
Formel: pH = −lg c(H₃O⁺), umgestellt: c(H₃O⁺) = 10−pH
Beispiel Sprudel mit pH = 5,1:
c(H₃O⁺) = 10−5,1 ≈ 7,9 · 10−6 mol/L
Zum Vergleich: Reines Wasser hat c(H₃O⁺) = 10−7 mol/L (pH = 7). Weitere Berechnungen findest du auf der Seite → pH-Wert berechnen.
Lernkarten – Ammoniak und Wasser
Klicke auf eine Karte, um die Antwort zu sehen.
Warum entsteht beim Springbrunnenversuch ein Unterdruck im Kolben?
NH₃ löst sich extrem gut in Wasser → Gas verschwindet aus der Gasphase → Druck sinkt → Unterdruck → Atmosphärendruck drückt Wasser nach oben.
Formuliere die vollständige Protolysegleichung von NH₃ mit Wasser.
NH₃ (aq) + H₂O (l) ⇌ NH₄⁺ (aq) + OH⁻ (aq)
NH₃ = Base (Protonenakzeptor)
H₂O = Säure (Protonendonator)
Nenne die beiden konjugierten Säure-Base-Paare bei der Ammoniak-Protolyse.
Paar 1: NH₄⁺ (Säure) / NH₃ (Base)
Paar 2: H₂O (Säure) / OH⁻ (Base)
Warum ist Sprudelwasser sauer, obwohl H₂CO₃ instabil ist?
CO₂ reagiert im Gleichgewicht mit H₂O. Auch ohne stabiles H₂CO₃ entstehen durch Protolyse H₃O⁺-Ionen (Erlenmeyer-Regel) → saure Lösung (pH ≈ 5,1).
Berechne: Ein Sprudel hat pH = 4,5. Wie groß ist c(H₃O⁺)?
c(H₃O⁺) = 10−pH = 10−4,5 ≈ 3,2 · 10−5 mol/L
Weiter im Kapitel Säure-Base-Reaktionen
← 3 Protolyse-Reaktionen (Übersicht) → 3.3 Neutralisation
🔁 Grundlagen (Kl. 9): Säure-Base-Reaktionen (Kl. 9) · Brønsted-Theorie (Kl. 9) · Neutralisation (Kl. 9)
📈 Vertiefung: pH-Wert berechnen · pKB-Wert (Basestärke) · Pufferlösung
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Die Neutralisation ist eine der wichtigsten Säure-Base-Reaktionen: Säure und Base heben sich gegenseitig auf. Du lernst, was auf Ionenebene wirklich passiert, warum die Neutralisationsenthalpie immer −56 kJ/mol beträgt, und wie man den Reaktionsverlauf mit Hilfe der Leitfähigkeitsmessung verfolgen kann.
Grundlagen aus der 9. Klasse
Die Neutralisation hast du bereits in der 9. Klasse kenngelernt. Hier wird sie jetzt auf Ionenebene vertieft: → Neutralisation (Kl. 9) · → Brønsted-Theorie (Kl. 9)
3.3 Neutralisation
a) Versuch: Zu 10 ml 0,1 M Salzsäure (mit Universalindikator angefärbt) werden 10 ml 0,1 M Natronlauge zugegeben.
b) Beobachtung: Die Indikatorfarbe schlägt von rot nach grün um. Die Lösung erwärmt sich.
c) Erklärung: Es findet eine Protolyse-Reaktion statt; es handelt sich um eine exotherme Reaktion.
d) Reaktionsschema:
H₃O⁺ (aq) + Cl⁻ (aq) + Na⁺ (aq) + OH⁻ (aq) → Na⁺ (aq) + Cl⁻ (aq) + 2 H₂O (l) ΔRH < 0
verdünnte Salzsäure + verdünnte Natronlauge → Kochsalzlösung
Eigentliche Reaktion:
H₃O⁺ (aq) + OH⁻ (aq) → 2 H₂O (l) ΔRHm° = −56 kJ/mol
Bei der Reaktion zwischen verdünnter Salzsäure und verdünnter Natronlauge entsteht eine Kochsalzlösung – der „Nudelwasser der Chemiker".
Der Verlauf der Neutralisation lässt sich durch Leitfähigkeitsmessung verfolgen: Zu Beginn ist die Leitfähigkeit hoch (viele Ionen in Lösung). Am Äquivalenzpunkt – wenn genau gleich viele Mol H₃O⁺ und OH⁻ vorhanden sind – erreicht die Leitfähigkeit ihr Minimum, da die reaktiven Ionen fast vollständig zu Wasser reagiert haben. Danach steigt die Leitfähigkeit wieder an.
Die eigentliche Reaktion bei dieser Neutralisation besteht in der Protonenübertragung von Oxonium-Ionen auf Hydroxid-Ionen, wobei aus beiden Ionenarten Wassermoleküle entstehen. Die in den Lösungen vorhandenen Begleitionen (hier: Na⁺ und Cl⁻) bleiben unverändert in der Lösung – sie werden auch als Spektatorionen bezeichnet.
💡 Hinweis: Die Neutralisationsenthalpie ΔRHm° = −56 kJ/mol gilt für die Neutralisation aller starken Säuren und starken Basen, weil die eigentliche Reaktion stets H₃O⁺ + OH⁻ → 2 H₂O ist. Die Begleitionen tragen nichts zur Reaktionsenthalpie bei. Mehr zur experimentellen Bestimmung: → Bestimmung der Neutralisationsenthalpie (Energetik).
Auf einen Blick – die wichtigsten Aussagen
Eigentliche Reaktion
H₃O⁺ (aq) + OH⁻ (aq) → 2 H₂O (l). Säure und Base reagieren stets über ihre Ionen – nicht als Moleküle.
Neutralisationsenthalpie
ΔRHm° = −56 kJ/mol – gilt für alle starken Säuren und Basen, da immer die gleiche Ionenreaktion stattfindet.
Spektatorionen
Na⁺ und Cl⁻ sind Begleitionen: Sie reagieren nicht und bleiben unverändert in Lösung. In der Ionengleichung werden sie gekürzt.
Leitfähigkeit
Minimum am Äquivalenzpunkt: Fast alle H₃O⁺- und OH⁻-Ionen sind zu Wasser reagiert → wenige Ladungsträger übrig.
Häufige Fragen – Neutralisation
Was passiert bei einer Neutralisation auf Ionenebene?
Bei der Neutralisation reagieren H₃O⁺-Ionen (von der Säure) mit OH⁻-Ionen (von der Base) zu Wassermolekülen:
H₃O⁺ (aq) + OH⁻ (aq) → 2 H₂O (l)
Die Begleitionen – bei HCl + NaOH sind das Na⁺ und Cl⁻ – sind an der Reaktion nicht beteiligt. Sie bleiben unverändert in Lösung und werden als Spektatorionen bezeichnet. Die vollständige Ionengleichung lässt sich daher zur Kurzgleichung (Netto-Ionengleichung) vereinfachen.
Warum ist die Neutralisationsenthalpie bei allen starken Säuren und Basen gleich?
Weil die eigentliche Reaktion immer dieselbe ist: H₃O⁺ + OH⁻ → 2 H₂O. Starke Säuren (wie HCl, HNO₃, H₂SO₄) und starke Basen (wie NaOH, KOH) sind in Wasser vollständig dissoziiert – es liegen also nur freie Ionen vor. Die Begleitionen reagieren nicht und leisten keinen Energiebeitrag. Daher gilt für alle Kombinationen starker Säure + starke Base: ΔRHm° = −56 kJ/mol.
Mehr dazu: → Bestimmung der Neutralisationsenthalpie
Wie kann man den Verlauf einer Neutralisation experimentell verfolgen?
Drei Methoden:
- Leitfähigkeitsmessung: Die Leitfähigkeit sinkt bis zum Äquivalenzpunkt auf ein Minimum (wenige reaktive Ionen) und steigt dann wieder an.
- Indikator: Ein Farbumschlag zeigt den Äquivalenzpunkt an (z. B. Universalindikator: rot → grün → blau).
- pH-Meter: Am Äquivalenzpunkt zeigt das pH-Meter pH = 7 (bei starker Säure + starke Base).
Die Leitfähigkeitsmessung hat den Vorteil, dass sie auch bei farblosen oder gefärbten Lösungen funktioniert.
Mehr zur Titration: → Titration und Pufferlösung
Was sind Begleitionen und warum reagieren sie nicht?
Begleitionen (Spektatorionen) sind Ionen, die bei einer Reaktion unverändert bleiben, weil sie kein stabiles Produkt miteinander bilden. Bei der Neutralisation von Salzsäure mit Natronlauge sind das Na⁺ und Cl⁻ – sie bilden zusammen Natriumchlorid (NaCl), das in Wasser aber vollständig dissoziiert vorliegt. Da kein stabiles Produkt entsteht, findet keine Reaktion statt.
In der vereinfachten Ionengleichung (Netto-Ionengleichung) werden Spektatorionen auf beiden Seiten gestrichen: Es bleibt nur H₃O⁺ + OH⁻ → 2 H₂O übrig.
Ist der pH-Wert nach einer Neutralisation immer genau 7?
Nur bei der Kombination starke Säure + starke Base in gleicher Stoffmenge gilt pH = 7. Bei schwachen Säuren oder schwachen Basen liegt am Äquivalenzpunkt kein neutraler pH vor:
- Schwache Säure + starke Base (z. B. Essigsäure + NaOH): Salzlösung ist leicht basisch (pH > 7) durch Hydrolyse des Acetat-Ions.
- Starke Säure + schwache Base (z. B. HCl + NH₃): Salzlösung ist leicht sauer (pH < 7) durch Hydrolyse des Ammoniumions.
Mehr dazu: → pH-Wert berechnen
Lernkarten – Neutralisation
Klicke auf eine Karte, um die Antwort zu sehen.
Schreibe die vollständige Ionengleichung für HCl + NaOH in Wasser.
H₃O⁺ (aq) + Cl⁻ (aq) + Na⁺ (aq) + OH⁻ (aq) →
Na⁺ (aq) + Cl⁻ (aq) + 2 H₂O (l)
Wie lautet die Netto-Ionengleichung (eigentliche Reaktion) jeder Neutralisation?
H₃O⁺ (aq) + OH⁻ (aq) → 2 H₂O (l)
ΔRHm° = −56 kJ/mol
Was sind Spektatorionen? Nenne ein Beispiel aus der Neutralisation von HCl + NaOH.
Ionen, die an der Reaktion nicht beteiligt sind und unverändert in Lösung bleiben.
Beispiel: Na⁺ und Cl⁻
Warum zeigt die Leitfähigkeit ein Minimum beim Äquivalenzpunkt der Neutralisation?
Am Äquivalenzpunkt sind fast alle H₃O⁺- und OH⁻-Ionen zu Wasser reagiert. Es gibt kaum noch reaktive Ladungsträger → Leitfähigkeit minimal.
Berechne: 0,5 mol H₃O⁺ reagiert mit 0,5 mol OH⁻. Wie viel Energie wird freigesetzt?
ΔRHm° = −56 kJ/mol
Q = 0,5 mol × 56 kJ/mol = 28 kJ
(freigesetzte Wärme, exotherm)
Weiter im Kapitel Säure-Base-Reaktionen
← 3.2 Ammoniak + Wasser → 3.4 Mehrprotonige Säuren
🔁 Grundlagen (Kl. 9): Neutralisation (Kl. 9) · Brønsted-Theorie (Kl. 9)
📈 Vertiefung: pH-Wert berechnen · Pufferlösung · Neutralisationsenthalpie (Energetik)
- Details
- Geschrieben von: Wolfram Hölzel