Was du auf dieser Seite lernst
Am Beispiel der Benzoesäure lernst du, wie chemische Gleichgewichte in der Säure-Base-Chemie konkret aussehen. Du verstehst, warum schwache Säuren nicht vollständig reagieren, warum Benzoesäure sich kaum in Wasser löst – und wie die Zugabe einer starken Base oder starken Säure das Gleichgewicht vollständig auf eine Seite verschiebt.
Grundlagen aus der 9. Klasse
Die Grundlagen zu Säure-Base-Reaktionen hast du bereits in der 9. Klasse kennengelernt: → Säure-Base-Definition nach Brønsted (Kl. 9) · → Stärke von Säuren und Basen (Kl. 9)
2.8 Allgemeines Zahlenbeispiel
| A | + | B | ⇌ | C | + | D | |
| Vorher | 1000 | 1000 | 0 | 0 | |||
| Nachher | 1000 − X | 1000 − X | X | X | |||
| z.B. im GG | 800 | 800 | 200 | 200 |
2.9 Säure-Base-Reaktionen mit Benzoesäure
↑ Zum Vergrößern klicken
✕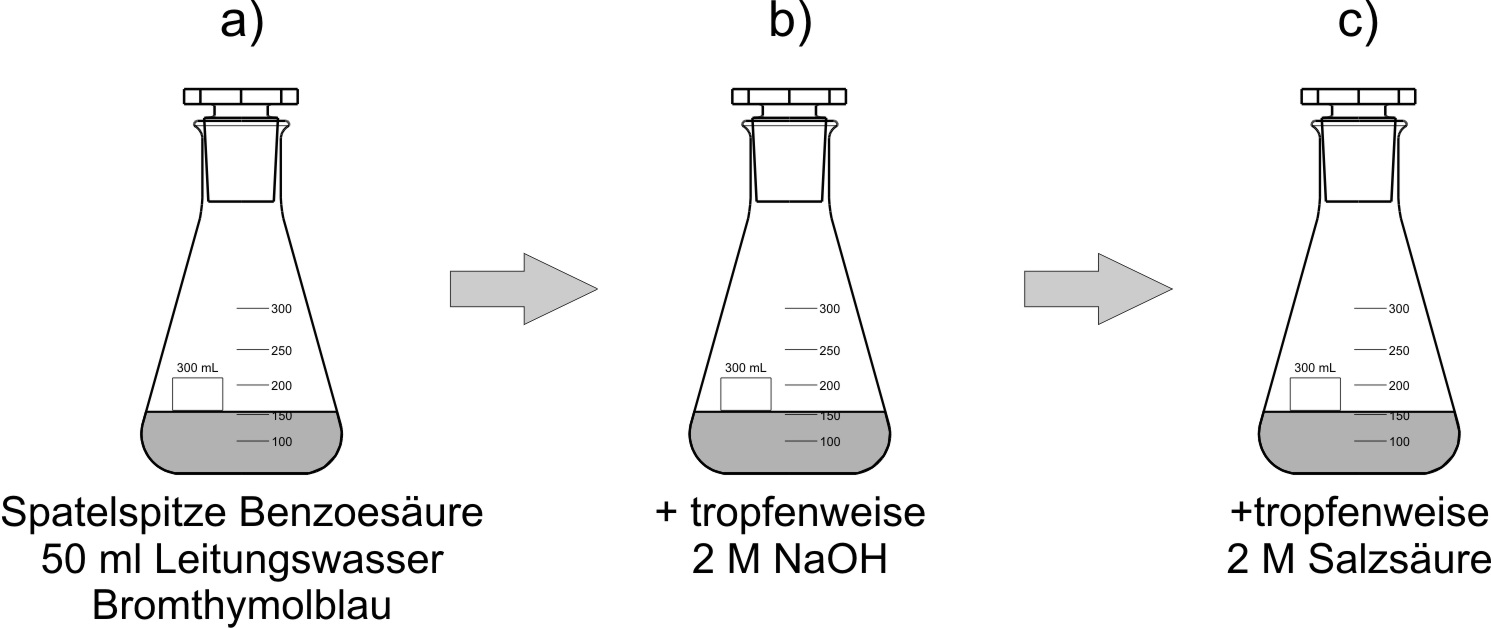
a) Benzoesäure + Wasser
Man gibt feste Benzoesäure in Wasser. Dabei beobachtet man, dass die Benzoesäure als weiße Substanz oben auf dem Wasser schwimmt. Auch mit Schütteln löst sie sich nicht auf.
Frage: Warum löst sich Benzoesäure nicht in Wasser? Dafür muss man sich einmal Benzoesäure anschauen (Hinweis: Benzoesäure ist noch vereinfacht „falsch" geschrieben, da wir die Aromaten erst später genauer betrachten).
↑ Zum Vergrößern klicken
✕
Erklärt, warum Benzoesäure nur schlecht in Wasser löslich ist!
Lösung: Löslichkeit der Benzoesäure
Bei Benzoesäure ist ein großer Teil unpolar (der Benzolring). Der polare Teil (die –COOH-Gruppe) ist kleiner. Die Benzoesäure kann zwar mit Wasser H-Brücken ausbilden, aber der große unpolare Rest sorgt für eine schlechte Löslichkeit.
↑ Zum Vergrößern klicken
Hinweis: Ähnliches löst sich in Ähnlichem.

Zusammenfassung Beobachtung: wenig löslich in Wasser; die Lösung reagiert schwach sauer.
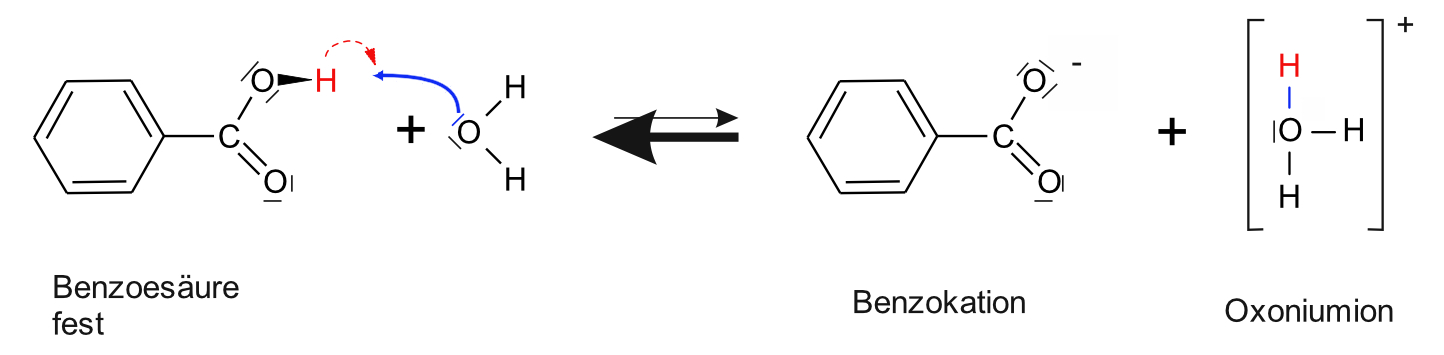
Formuliert die Reaktionsgleichung für die Reaktion von Benzoesäure mit Wasser mit bindenden und nichtbindenden Elektronenpaaren (Hinweis: Benzoesäure ist jetzt schon etwas vereinfacht geschrieben, indem die H-Atome am Ring weggelassen wurden).
Lösung: Reaktionsgleichung Benzoesäure + Wasser
↑ Zum Vergrößern klicken
Es findet nur eine schwache Reaktion mit H2O statt. Es reagieren nur wenige Benzoesäuremoleküle. Das Gleichgewicht liegt links.
b) Benzoesäure + Natronlauge (Neutralisation)
Man gibt vorsichtig Natronlauge zu und schüttelt die Lösung, bis die Benzoesäure vollständig
aufgelöst ist.
Beobachtung: Es entsteht eine klare Lösung.
Formuliert hierfür auch wieder eine Reaktionsgleichung mit bindenden und nichtbindenden Elektronenpaaren.
✕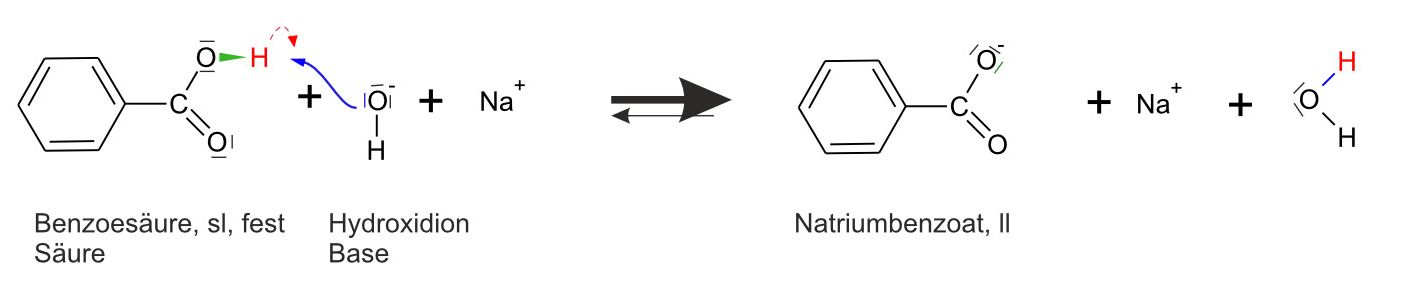
Die Benzoesäuremoleküle reagieren praktisch vollständig (das Gleichgewicht liegt weit auf der rechten Seite).
c) Gelöstes Natriumbenzoat + verd. Salzsäure
Die klare Natriumbenzoat-Lösung wird mit verdünnter Salzsäure versetzt.
Beobachtung: Die klare Lösung wird trübe. Eine weiße, pulverartige Substanz
schwimmt wieder auf der Oberfläche.
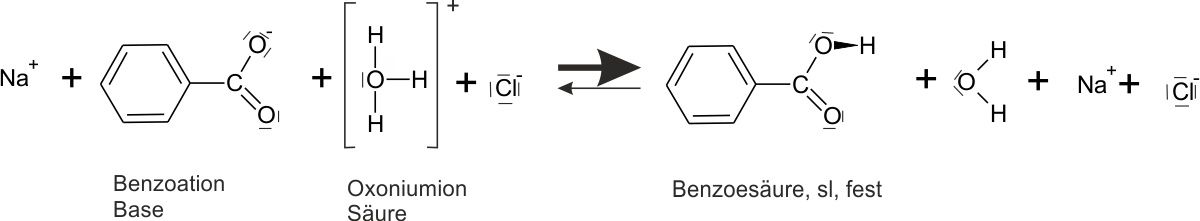
Feste Benzoesäure scheidet sich ab; die Benzoat-Anionen reagieren praktisch vollständig.
Auf einen Blick – die wichtigsten Aussagen
SCHWACHE SÄURE
Benzoesäure ist eine schwache Säure: das Gleichgewicht mit Wasser liegt links – es reagieren nur wenige Moleküle.
LÖSLICHKEIT
Der große unpolare Benzolring überwiegt die polare –COOH-Gruppe: Benzoesäure ist deshalb wenig wasserlöslich.
STARKE BASE
Natronlauge (starke Base) lässt Benzoesäure vollständig reagieren → klare Natriumbenzoat-Lösung entsteht.
STARKE SÄURE
Salzsäure (starke Säure) verdrängt Benzoesäure aus dem Benzoat-Salz → weißer Feststoff fällt wieder aus.
Häufige Fragen – Benzoesäure-Gleichgewicht
Warum löst sich Benzoesäure kaum in Wasser?
Benzoesäure besteht aus einem großen unpolaren Benzolring und einer kleineren polaren Carboxylgruppe (–COOH). Da „Ähnliches Ähnliches löst", ist der unpolare Anteil so dominant, dass die Wasserlöslichkeit sehr gering bleibt – obwohl die –COOH-Gruppe H-Brücken zu Wasser ausbilden kann. Mehr zur Struktur von Benzol und seinen Derivaten: → Aromaten (Kursstufe).
Warum liegt das Gleichgewicht von Benzoesäure + Wasser auf der linken Seite?
Benzoesäure ist eine schwache Säure: Sie gibt Protonen nur in geringem Umfang an Wasser ab. Im Gleichgewicht überwiegen daher die Edukte (undissoziierte Benzoesäure + Wasser) gegenüber den Produkten (Benzoat-Ion + Hydronium-Ion). Man sagt: das Gleichgewicht liegt links. Ein kleiner Kc-Wert (Ks ≈ 6,3 · 10−5) bestätigt das. Grundlagen zur Gleichgewichtslage: → Merkmale eines chemischen Gleichgewichts.
Was geschieht, wenn man Benzoesäure mit Natronlauge versetzt?
Natronlauge enthält OH−-Ionen (eine starke Base). Diese reagieren mit der Benzoesäure vollständig zu Natriumbenzoat (C6H5COO− Na+) und Wasser. Das Benzoat-Ion ist gut wasserlöslich → die zuvor trübe Suspension wird klar. Diese vollständige Reaktion ist möglich, weil NaOH eine viel stärkere Base ist als Wasser. Verwandte Grundlagen: → Neutralisation (Kl. 9).
Was passiert beim Ansäuern von Natriumbenzoat-Lösung mit Salzsäure?
Salzsäure (HCl) ist eine starke Säure und gibt bereitwillig Protonen an das Benzoat-Ion ab. Dabei wird Benzoesäure zurückgebildet, die sich wegen ihrer geringen Wasserlöslichkeit sofort als weißer Feststoff abscheidet (Lösung wird trüb). Stärkere Säuren verdrängen schwächere Säuren aus ihren Salzen – ein direktes Anwendungsbeispiel des Stärke-Prinzips von Säuren und Basen (Kl. 9).
Wie berechnet man Kc für das allgemeine Zahlenbeispiel A + B ⇌ C + D?
Im Zahlenbeispiel liegen im Gleichgewicht vor: A = 800, B = 800, C = 200, D = 200 (gleiche Einheit, z. B. mmol/L). Das Massenwirkungsgesetz ergibt:
Kc = [C] · [D] / ([A] · [B]) = 200 · 200 / (800 · 800) = 40.000 / 640.000 ≈ 0,0625
Ein Kc < 1 zeigt: die Edukte überwiegen im Gleichgewicht (Gleichgewicht liegt links). Mehr dazu: → Massenwirkungsgesetz (MWG).
Lernkarten – Benzoesäure-Gleichgewicht
Klicke auf eine Karte, um die Antwort zu sehen.
Was versteht man unter einer schwachen Säure – und wo liegt ihr Gleichgewicht?
Eine schwache Säure gibt Protonen nur in geringem Umfang ab. Das Gleichgewicht liegt auf der Seite der Edukte (undissoziierte Säure überwiegt). Ks ist klein (≪ 1).
Warum ist Benzoesäure nur wenig in Wasser löslich?
Der große unpolare Benzolring überwiegt die polare –COOH-Gruppe. Da ähnliches ähnliches löst, bleibt Benzoesäure in Wasser weitgehend unlöslich.
Was beobachtet man beim Zugeben von Natronlauge zur Benzoesäure-Suspension?
Die trübe Suspension wird klar. Benzoesäure reagiert vollständig mit OH− zu gut löslichem Natriumbenzoat. Die starke Base verschiebt das Gleichgewicht vollständig nach rechts.
Was passiert, wenn man Natriumbenzoat-Lösung mit verdünnter Salzsäure ansäuert?
Die klare Lösung wird trübe: Benzoesäure wird zurückgebildet und fällt als weißer Feststoff aus. HCl (starke Säure) verdrängt Benzoesäure (schwache Säure) aus ihrem Salz.
Rechenaufgabe: A + B ⇌ C + D. Im GG: [A] = [B] = 0,80 mol/L, [C] = [D] = 0,20 mol/L. Berechne Kc und gib die Gleichgewichtslage an.
Kc = (0,20 · 0,20) / (0,80 · 0,80) = 0,04 / 0,64 ≈ 0,0625
Kc < 1 → Gleichgewicht liegt links (Edukte überwiegen).
Weiter im Kapitel Gleichgewichtsreaktionen
← 2.6/2.7 Schreibweise und Kollisionsmodell → 2.10 Verschiebung des Gleichgewichts
← 2.5 Estergleichgewicht → 2.12 Massenwirkungsgesetz
🔁 Grundlagen: Brønsted-Definition (Kl. 9) · Stärke von Säuren und Basen (Kl. 9) · Neutralisation (Kl. 9)
🔗 Weiterführend: Aromaten – Benzol und Derivate (Kursstufe) · Autoprotolyse und pH-Wert (Kursstufe)
