1 Systeme
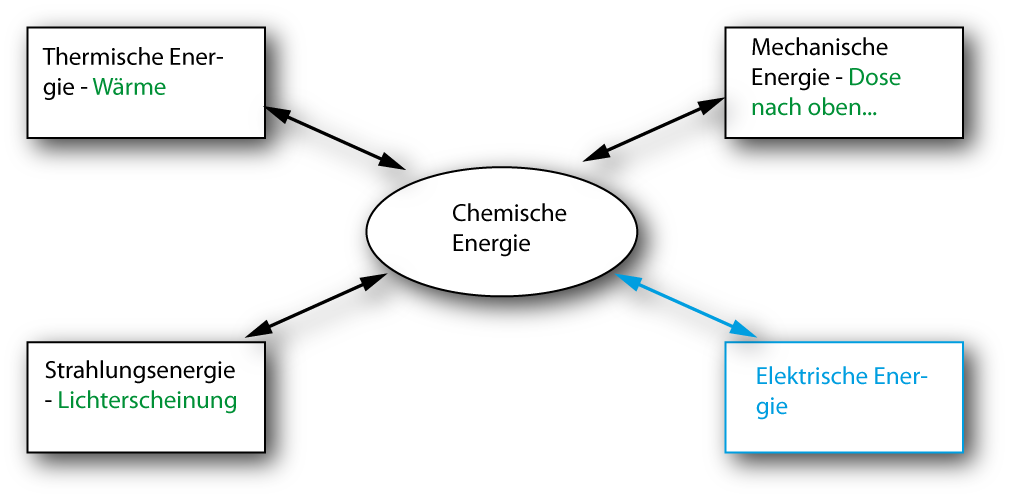
Abb. 1: Bei chemischen Reaktionen wie 2 H₂ + O₂ → 2 H₂O wird Energie in verschiedenen Formen freigesetzt oder aufgenommen.
Was ist ein thermodynamisches System?
In der Thermodynamik und Chemie nennt man einen begrenzten Ausschnitt des Universums, den man gezielt untersucht, ein System (griech. systema – „das Zusammengestellte, Verbundene"). Alles, was außerhalb des Systems liegt, wird als Umgebung bezeichnet.
Die gedachte Grenze zwischen System und Umgebung heißt Systemgrenze. Sie kann realer Natur sein (z. B. die Wand eines Reagenzglases) oder gedanklich festgelegt werden. Entscheidend ist, was über diese Grenze ausgetauscht werden kann: Energie, Teilchen (Materie) – oder beides nicht.
Je nach Art des möglichen Austauschs unterscheidet die Thermodynamik drei grundlegende Systemtypen.
Die drei Systemtypen im Überblick
| Offenes System | Geschlossenes System | Abgeschlossenes (isoliertes) System | |
|---|---|---|---|
| Austausch von … | ✓ Energie ✓ Teilchen (Materie) |
✓ Energie ✗ Teilchen |
✗ Energie ✗ Teilchen |
| Kein Austausch von … | – | Teilchen | Energie und Teilchen |
| Konsequenz | Masse und Energie des Systems können sich ändern | Masse des Systems bleibt konstant; Energie kann fließen | Gesamtenergie des Systems ist konstant (1. Hauptsatz der Thermodynamik) |
| Idealisiertes Beispiel | Kochtopf (offen, auf Herd) | Dampfkochtopf (geschlossen, aber wärmeleitend) | Thermoskanne (näherungsweise isoliert) |
| Reales Beispiel in der Chemie | Reagenzglas über Flamme (offen) | Verschlossener Erlenmeyerkolben beim Erhitzen | Kalorimeter (idealisiert) |
Offenes System
Bei einem offenen System können sowohl Energie als auch Materie (Teilchen) die Systemgrenze überschreiten. Ein alltägliches Beispiel ist ein offener Kochtopf mit kochendem Wasser: Wärme wird vom Herd zugeführt (Energieaustausch), und gleichzeitig entweicht Wasserdampf in die Umgebung (Teilchenaustausch). Die meisten biologischen Systeme – etwa eine Zelle oder ein ganzer Organismus – sind ebenfalls offene Systeme.
Geschlossenes System
Ein geschlossenes System lässt nur Energieaustausch (z. B. Wärme oder Arbeit) zu, nicht jedoch den Austausch von Materie. Die Masse des Systems bleibt daher konstant. Ein Dampfkochtopf veranschaulicht diesen Typ: Der Deckel verhindert den Austritt von Dampf (keine Materie verlässt das System), aber Wärme kann über die Metallwände zugeführt werden.
In der praktischen Laborchemie ist ein verschlossener Erlenmeyerkolben ein gebräuchliches Beispiel – er nimmt Wärme aus dem Wasserbad auf, aber keine Stoffe gelangen hinein oder hinaus.
Abgeschlossenes (isoliertes) System
Das abgeschlossene System (auch: isoliertes System) ist der theoretische Extremfall: Weder Energie noch Materie werden mit der Umgebung ausgetauscht. Dadurch gilt der erste Hauptsatz der Thermodynamik in seiner reinsten Form: die Gesamtenergie des Systems bleibt konstant.
Eine Thermoskanne nähert sich diesem Ideal an – sie minimiert Wärmeleitung und Konvektion. In der Praxis gibt es kein perfekt abgeschlossenes System; das Universum als Ganzes wird in der Kosmologie jedoch als abgeschlossenes System betrachtet.

Abb. 2: Schematische Darstellung der drei Systemtypen anhand von Reagenzgläsern.
Bedeutung der Systemdefinition für chemische Reaktionen
Die Wahl des Systems ist in der Thermodynamik keine Nebensächlichkeit – sie bestimmt, welche Größen man messen und berechnen kann. Beim Kalorimetrie-Experiment etwa (→ 7 Kalorimetrie) wird das Reaktionsgefäß näherungsweise als abgeschlossenes System behandelt, damit die freigesetzte Wärme vollständig gemessen werden kann.
Für das Verständnis der inneren Energie U (→ 3 Innere Energie) und der Enthalpie H (→ 8 Enthalpie) ist die Systemdefinition ebenso grundlegend: Welche Energie gehört „zum System"? Was wird zur Umgebung abgegeben oder von ihr aufgenommen?
Auch der Energieerhaltungssatz (→ 2 Energieerhaltungssatz) und das Konzept der Entropie (→ 11 Entropie) bauen direkt auf dem Systembegriff auf.
Häufige Fragen zu thermodynamischen Systemen
Was unterscheidet ein offenes von einem geschlossenen System?
Bei einem offenen System können Energie und Materie (Teilchen) die Systemgrenze passieren. Beim geschlossenen System ist nur ein Energieaustausch möglich – Materie bleibt im System eingeschlossen. Ein Beispiel: Ein offener Kochtopf ist ein offenes System (Dampf entweicht), ein Dampfkochtopf ist ein geschlossenes System (kein Dampf entweicht, aber Wärme wird übertragen).
Warum gibt es in der Realität kein perfekt abgeschlossenes System?
Jedes reale Material leitet Wärme in gewissem Maße. Eine Thermoskanne minimiert diesen Effekt durch Vakuumisolierung, kommt dem Ideal aber nur nahe. Ein perfekt isoliertes System würde keinerlei Wärmekontakt mit der Umgebung haben – das ist technisch nicht vollständig realisierbar. Für praktische Berechnungen in der Chemie wird das idealisierte abgeschlossene System jedoch als Näherung genutzt (z. B. im Kalorimeter).
Ist ein lebender Organismus ein offenes oder geschlossenes System?
Ein lebender Organismus ist stets ein offenes System: Er nimmt Nahrung und Sauerstoff auf (Materie), gibt Kohlendioxid, Wasser und Wärme ab (Energie und Materie). Nur weil ständig Energie und Materie ausgetauscht werden, kann Leben überhaupt aufrechterhalten werden. Das steht im Einklang mit dem zweiten Hauptsatz der Thermodynamik und dem Konzept der Entropie.
Wie hängt der Systembegriff mit dem Energieerhaltungssatz zusammen?
Der Energieerhaltungssatz gilt in seiner einfachsten Form für das abgeschlossene System: Die Gesamtenergie bleibt konstant, sie kann nur umgewandelt, nicht erzeugt oder vernichtet werden. Bei offenen und geschlossenen Systemen muss man den Energieaustausch mit der Umgebung in die Bilanz einbeziehen – die Energie des Systems allein ist dann nicht konstant.
Welche Systemtypen kommen in Abituraufgaben vor?
In Prüfungsaufgaben der Oberstufe (Baden-Württemberg) wird häufig verlangt, ein beschriebenes Experiment einem Systemtyp zuzuordnen und die Begründung anzugeben. Typische Formulierungen: „Begründe, warum der verwendete Kalorimeter näherungsweise als abgeschlossenes System gilt." Oder: „Warum ist ein lebender Organismus kein geschlossenes System?" – Die Antwort dreht sich immer um den möglichen oder nicht möglichen Austausch von Energie und/oder Materie.
Lernkarten – Systeme in der Thermodynamik
Klicke auf eine Karte, um die Antwort zu sehen.
Was versteht man in der Thermodynamik unter einem System?
Ein System ist ein begrenzter Ausschnitt des Universums, den man gezielt untersucht. Alles andere ist die Umgebung. Dazwischen liegt die Systemgrenze.
Was kann beim offenen System die Systemgrenze passieren?
Beim offenen System können Energie UND Teilchen (Materie) ausgetauscht werden. Beispiel: offener Kochtopf – Dampf und Wärme entweichen.
Was ist der Unterschied zwischen einem geschlossenen und einem abgeschlossenen System?
Geschlossen: Nur Energie kann ausgetauscht werden, keine Materie.
Abgeschlossen (isoliert): Weder Energie noch Materie werden
ausgetauscht – die Gesamtenergie ist konstant.
Welcher Hauptsatz der Thermodynamik gilt direkt für das abgeschlossene System?
Der 1. Hauptsatz der Thermodynamik (Energieerhaltungssatz): Die Gesamtenergie eines abgeschlossenen Systems bleibt konstant. Energie kann nur umgewandelt, nicht erzeugt oder vernichtet werden.
Ordne zu: Die gemeine Fichte · Thermoskanne · Heizungssystem – welcher Systemtyp ist jeweils gemeint?
🟢 Die gemeine Fichte → offenes System (Energie + Materie)
🟡 Heizungssystem → geschlossenes System (nur Energie)
🔵 Thermoskanne → abgeschlossenes System (näherungsweise)
Weiter im Kapitel Energetik
→ 2 Energieerhaltungssatz → 3 Innere Energie U → 8 Enthalpie H → 11 Entropie S → 7 Kalorimetrie
¹ System (v. griech. systema, „das Gebilde, Zusammengestellte, Verbundene") – grundlegender Begriff der klassischen Thermodynamik. Lehrplan Chemie Baden-Württemberg, 1./2. Jahrgangsstufe.
- Details
- Geschrieben von: Wolfram Hölzel
2 Energieerhaltungssatz (Energieprinzip)
Er besagt, dass in einem abgeschlossenen (isolierten) System die Summe der Energien konstant ist. (von Mayer, Joule, Helmholtz)
1. Hauptsatz der Thermodynamik:
Es kann bei keinem physikalischen und chemischen Vorgang Energie neu entstehen oder vergehen, nur die Form der Energie (z.B. mechanische, thermische, elektrische, chemische,...) kann sich ändern.
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Jeder Stoff trägt Energie in sich – als Schwingungs-, Bindungs- oder Kernenergie. Diese innere Energie U ist eine Zustandsgröße: ihr aktueller Wert hängt nicht davon ab, wie das System in diesen Zustand gelangte. Messbar ist nur die Änderung ΔU = Q + W (Wärme + Arbeit).
3 Innere Energie – U
Jeder Stoff hat in sich Energie in irgendeiner Form gespeichert = Innere Energie U,
äußere Energie = potenzielle Energie (wie z.B. Bügeleisen auf dem Schrank) + kinetische Energie (z.B. das Bügeleisen fliegt runter) ⇨ spielt keine Rolle für chemische Reaktionen.
Man unterscheidet vereinfacht:
- den physikalisch-thermischen (Bsp.: Rotationsenergie, Schwingungsenergie), Uth
- den chemischen (die potentielle Energie der Bindungskräfte bzw. die Bindungsenergie) Uch und
- den kernphysikalischen (potentielle Energie, die in den Atomkernen vorhanden) UK
.....Anteil der inneren Energie (U = UK + Uch + Uth)
Es lässt sich kein Absolutbetrag U stofflicher Systeme angeben, da sich kein Energienullpunkt festlegen lässt. Bestimmbar sind nur Änderungen der inneren Energie ΔU
↑ Zum Vergrößern klicken
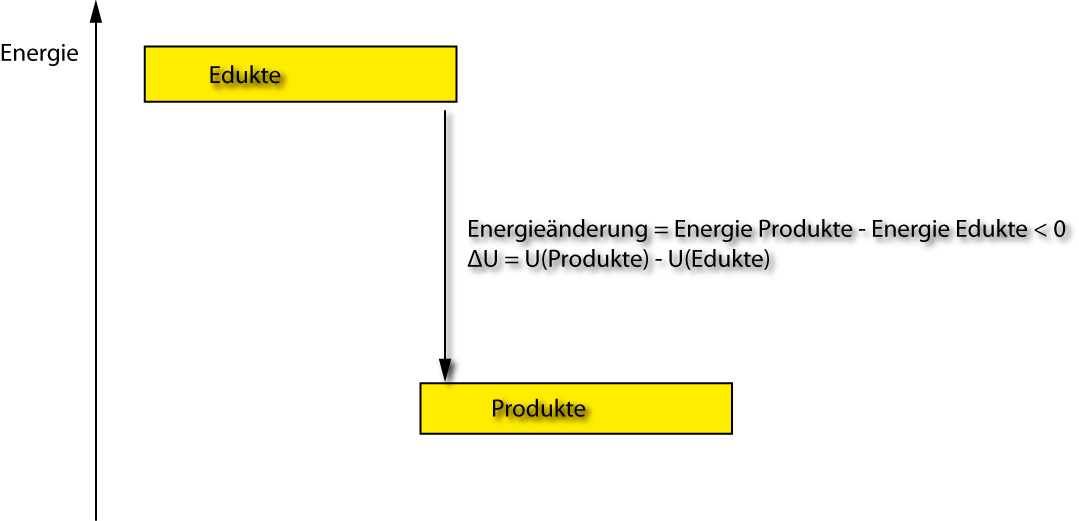
ΔU = U₂ – U₁
ΔU > 0 : Energie wird aufgenommen
ΔU < 0 : Energie wird abgegeben
U₂: Summe der inneren Energien der Produkte
U₁: Summe der inneren Energien der Reaktanden (Edukte)
Änderung der inneren Energie = Wärme + Arbeit
ΔU = U₂ – U₁ = Q + W
Innere Energie = Zustandsgröße
Zustandsgrößen: in einem bestimmten Zustand hat die Zustandsgröße einen bestimmten Wert. Dabei ist es egal, wie man diesen Zustand erreicht hat, also welchen Weg dafür beschritten hat.
Bsp.: Für die momentane potentielle Energie einer Person auf einem Berggipfel (Zustandsgröße) ist es gleichgültig, auf welchem Weg die Person den Gipfel erreicht hat. Die aufgewendete Arbeit hingegen, die die Person aufbringen muss, um diese potentielle Energie zu erreichen, hängt natürlich vom zurückgelegten Weg ab.
Zustandsgrößen: Volumen, Druck, Temperatur sind unabhängig von der Vorgeschichte des Systems (ob es vorher 50°C oder 20°C war).
Die Arbeit ist bei chemischen Reaktionen meistens Volumenarbeit.
Auf einen Blick – die wichtigsten Aussagen
Definition
U = gesamte gespeicherte Energie eines Stoffes: UK + Uch + Uth
Messbarkeit
Kein Absolutwert messbar – nur die Änderung ΔU ist bestimmbar.
Formel
ΔU = Q + W
Wärme + Arbeit (meist Volumenarbeit)
Zustandsgröße
Der Wert von U hängt nur vom aktuellen Zustand ab – nicht vom Weg dorthin.
Häufige Fragen zur inneren Energie
Was genau ist die innere Energie U?
Die innere Energie U ist die gesamte in einem Stoff gespeicherte Energie. Sie setzt sich zusammen aus dem thermischen Anteil Uth (Schwingungs- und Rotationsbewegungen der Teilchen), dem chemischen Anteil Uch (Bindungsenergie der Moleküle) und dem kernphysikalischen Anteil UK (Energie der Atomkerne). Bei chemischen Reaktionen ist vor allem Uch relevant.
Warum lässt sich kein Absolutwert von U angeben?
Es gibt keinen festlegbaren Energienullpunkt für ein Stoffsystem. Man kann nicht sagen, wie viel Energie ein Stoff „insgesamt" enthält – nur wie viel sich ändert, wenn der Stoff an einer Reaktion beteiligt ist. Deshalb arbeitet die Thermodynamik stets mit der Änderung ΔU = U₂ − U₁.
Was bedeutet ΔU > 0 bzw. ΔU < 0?
Ist ΔU > 0, nimmt das System Energie auf. Ist ΔU < 0, gibt das System Energie ab. Die Vorzeichen-Konvention folgt dem System: Energie hinein ist positiv, Energie heraus ist negativ. Achtung: Den Begriff exotherm verknüpft man in der Chemie üblicherweise mit ΔH < 0 (Enthalpie bei konstantem Druck) – nicht direkt mit ΔU.
Was ist eine Zustandsgröße?
Eine Zustandsgröße hat in einem bestimmten Zustand einen eindeutigen Wert – unabhängig davon, wie dieser Zustand erreicht wurde. Beispiele: Druck, Volumen, Temperatur, innere Energie U. Im Gegensatz dazu sind Wärme Q und Arbeit W Prozessgrößen: sie hängen vom Weg ab.
Wie hängen ΔU, Wärme Q und Arbeit W zusammen?
Nach dem ersten Hauptsatz der Thermodynamik gilt: ΔU = Q + W. Die Änderung der inneren Energie ist die Summe aus zugeführter Wärme Q und geleisteter Arbeit W. Bei chemischen Reaktionen in offenen Gefäßen ist W meist die Volumenarbeit (→ 4 Volumenarbeit).
Lernkarten – Innere Energie U
Klicke auf eine Karte, um die Antwort zu sehen.
Aus welchen drei Anteilen setzt sich die innere Energie U zusammen?
U = UK (kernphysikalisch)
+ Uch (chemisch / Bindungsenergie)
+ Uth (thermisch / Schwingung, Rotation)
Warum kann man den Absolutwert der inneren Energie nicht angeben?
Es gibt keinen festlegbaren Energienullpunkt. Messbar ist nur die Änderung ΔU.
Was bedeuten die Vorzeichen von ΔU?
ΔU > 0 → System nimmt Energie auf
ΔU < 0 → System gibt Energie ab
Achtung: „exotherm/endotherm" bezieht sich auf ΔH (bei konstantem Druck), nicht auf ΔU!
Nenne die Grundformel für die Änderung der inneren Energie.
ΔU = Q + W
(Wärme + Arbeit)
Bei chem. Reaktionen: W meist = Volumenarbeit
Warum ist die innere Energie eine Zustandsgröße?
Weil ihr Wert nur vom aktuellen Zustand des Systems abhängt – nicht davon, auf welchem Weg dieser Zustand erreicht wurde.
Weiter im Kapitel Energetik
← 2 Energieerhaltungssatz → 4 Volumenarbeit W → 8 Enthalpie H ← 1 Systeme
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Chemische Reaktionen laufen meist bei konstantem Druck ab – dabei verrichtet das System Volumenarbeit gegen den Atmosphärendruck. Die Formel W = −p · ΔV beschreibt, wie viel Energie dabei übertragen wird, und warum das Vorzeichen negativ ist. Diese Arbeit geht direkt in die Energiebilanz ΔU = Q − p · ΔV ein.
4 Volumenarbeit - W
Def.:
- isobar = gleicher Druck [gr. isos = gleich; barys = schwer]
- isotherm = gleiche Temperatur;
- isochor = gleiches Volumen
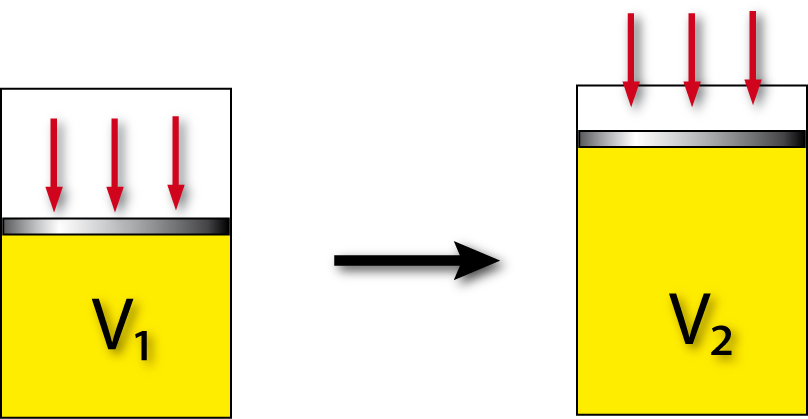
Volumenänderung bei konstanten Druck (= isobar : p = const.):
ΔV = V₂ – V₁
↑ Zum Vergrößern klicken
Ein externer Druck übt eine der Ausdehnung entgegengesetzte Kraft aus. Für uns ist das i.d.R. der Atmosphärendruck (= Konstant) (für ein sich ändernder Außendruck = reversibler Vorgang ist dann die UNI zuständig).
Ist der externe Druck 0 (= Vakuum), wir keine Arbeit verrichtet!
Allgemein:
Vom System abgegebene Energie ⇨ negatives Vorzeichen
Da bei Volumenvergrößerung V₂ – V₁ > 0 vom System Volumenarbeit an die Umgebung abgeführt wird, wird die Volumenarbeit mit einem negativen Vorzeichen definiert.
W = Wmech = - p • ΔV
Bei Volumenabnahme wird dem System Volumenarbeit zugeführt (von der Umgebung)
Herleitung:
Querschnitt des Kolbens: A
Von außen auf den Kolben wirkende Kraft: F = A · p
Wenn der Kolben um eine Wegstrecke s nach außen geschoben wird: ΔV = V₂ – V₁ = A ∙ s
Geleistete Arbeit = Kraft x Strecke = Fläche x Druck x Strecke = Fläche x Strecke x Druck = Volumenänderung x Druck
W = F ∙ s = A ∙ p ∙ s = ΔV ∙ p
ΔU = Q – p ∙ ΔV
Gegendruck = Atmosphärendruck:
101325 Pa = 1013,25 hPa (Hektopascal) = 1,01325 bar = 1013,25 mbar
(= Normalbedingung (T = 0°C); = Standardbedingung (T=25 °C))
1 atm = 1,01325 • 10⁵ Pa = 101 325 Pa
SI-Einheiten:
Druck: 1 Pa (=1 kg/(m•s²) = 1 N/m²)
Auf einen Blick – die wichtigsten Aussagen
Formel
W = −p · ΔV
gilt bei konstantem Druck (isobar)
Vorzeichen
Ausdehnung (ΔV > 0) → System gibt Energie ab → W negativ
Sonderfall Vakuum
p = 0 → W = 0
Keine Arbeit wird verrichtet
Energiebilanz
ΔU = Q − p · ΔV
Wärme minus Volumenarbeit
Häufige Fragen zur Volumenarbeit
Was ist Volumenarbeit und wann tritt sie auf?
Volumenarbeit tritt auf, wenn ein System sein Volumen gegen einen äußeren Druck ändert – z. B. wenn bei einer chemischen Reaktion Gase entstehen und den Kolben eines Gefäßes nach außen drücken. In der Laborchemie ist dieser äußere Druck meist der konstante Atmosphärendruck (isobarer Prozess). Die geleistete Arbeit ergibt sich aus Kraft mal Strecke, was sich vereinfacht zu W = −p · ΔV zusammenfassen lässt.
Warum ist das Vorzeichen der Volumenarbeit negativ?
Die Vorzeichen-Konvention folgt dem System: Energie, die das System abgibt, erhält ein negatives Vorzeichen. Bei einer Ausdehnung (ΔV > 0) drückt das System den Kolben nach außen und leistet dabei Arbeit an der Umgebung – es verliert also Energie. Daher: W = −p · ΔV < 0. Umgekehrt gilt: Bei Kompression (ΔV < 0) wird dem System von außen Arbeit zugeführt, W wird positiv.
Was passiert bei Außendruck = 0 (freie Expansion ins Vakuum)?
Ist der äußere Druck null – zum Beispiel bei Expansion in ein Vakuum – dann gilt W = −0 · ΔV = 0. Es wird keine Arbeit verrichtet, egal wie groß die Volumenänderung ist. Das System dehnt sich aus, ohne Energie abzugeben. Dieser Sonderfall spielt in der Laborpraxis kaum eine Rolle, ist aber für das konzeptionelle Verständnis wichtig.
Was bedeuten isobar, isotherm und isochor?
Isobar (p = const.) bedeutet konstanter Druck – der häufigste Fall im Labor, da man meist gegen den Atmosphärendruck arbeitet. Isotherm (T = const.) bedeutet konstante Temperatur. Isochor (V = const.) bedeutet konstantes Volumen – in diesem Fall ist ΔV = 0, also W = 0, und die gesamte Energieänderung entspricht der Wärme: ΔU = Q.
Wie hängt Volumenarbeit mit der inneren Energie zusammen?
Aus dem ersten Hauptsatz der Thermodynamik (→ 3 Innere Energie) gilt allgemein ΔU = Q + W. Setzt man die Volumenarbeit W = −p · ΔV ein, ergibt sich ΔU = Q − p · ΔV. Diese Beziehung ist die Grundlage für den Begriff der Enthalpie H, die bei isobaren Prozessen besonders praktisch ist (→ 8 Enthalpie).
Lernkarten – Volumenarbeit W
Klicke auf eine Karte, um die Antwort zu sehen.
Wie lautet die Formel der Volumenarbeit bei konstantem Druck?
W = −p · ΔV
mit ΔV = V₂ − V₁
gilt für isobare Prozesse (p = const.)
Warum trägt die Formel ein negatives Vorzeichen?
Bei Ausdehnung (ΔV > 0) gibt das System Energie an die Umgebung ab.
Energieabgabe = negativ (Systemsicht).
Was bedeutet isobar, isotherm, isochor?
🔵 isobar → p = const. (gleicher Druck)
🟡 isotherm → T = const. (gleiche Temperatur)
🟢 isochor → V = const. (gleiches Volumen)
Wie viel Volumenarbeit wird bei Expansion ins Vakuum verrichtet?
W = 0
Da p = 0: W = −0 · ΔV = 0
Keine Arbeit trotz Volumenänderung.
Wie lautet ΔU, wenn Volumenarbeit berücksichtigt wird?
ΔU = Q − p · ΔV
(Wärme minus Volumenarbeit)
Bei isochorem Prozess (ΔV=0): ΔU = Q
Weiter im Kapitel Energetik
← 3 Innere Energie U → 5 Reaktionswärme Q → 8 Enthalpie H ↑ 1 Systeme
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Wie viel Wärme wird bei einer chemischen Reaktion freigesetzt – und warum hängt das davon ab, ob das Gefäß offen oder geschlossen ist? Bei konstantem Volumen gilt QV = ΔU, bei konstantem Druck gilt Qp = ΔH = ΔU + p·ΔV. Der Unterschied ist die Volumenarbeit, die das entstehende Gas gegen den Atmosphärendruck verrichtet.
5 Reaktionswärme – Q
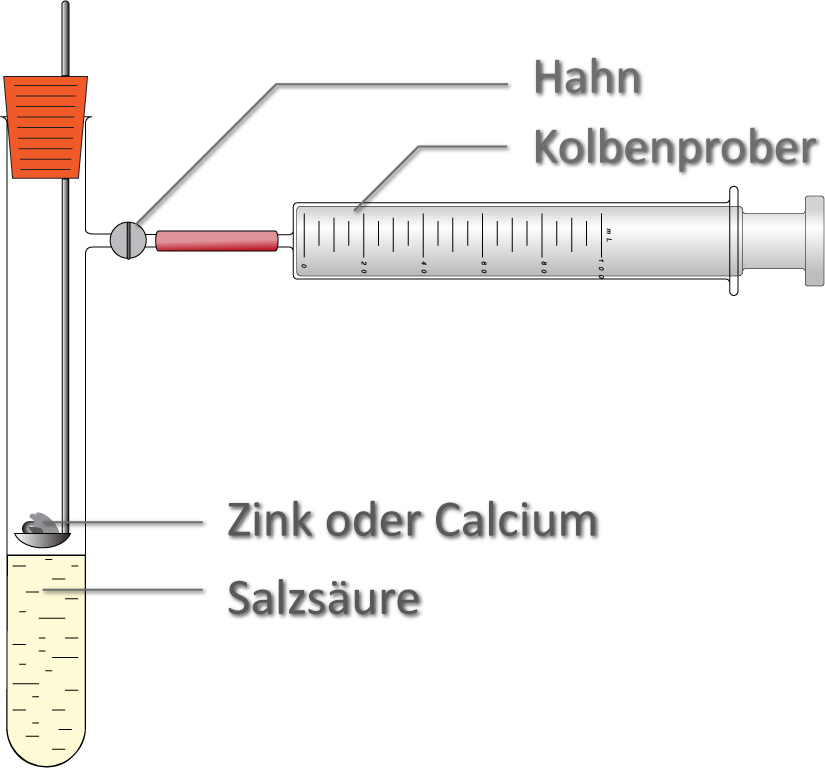
Bestimmung der Reaktionswärme – Q.
Bsp: Quantitative Umsetzung von Zink (n(Zn) = 1 mol, M(Zn) = 65,4 g/mol).
Bildung eines gasförmigen Reaktionsproduktes
- bei konstantem Volumen = Hahn geschlossen
- bei konstantem Druck = Hahn geöffnet
↑ Zum Vergrößern klicken
Teilchengleichung:
Zn + 2 H₃O⁺ (aq) + 2 Cl⁻ (aq) → Zn²⁺ (aq) + 2 Cl⁻ (aq) + 2 H₂O + H₂
Freigesetzte Reaktionswärme:
bei konstantem Volumen: QV = -156,5 kJ/mol = ΔU
Änderung der Inneren Energie = Reaktionswärme + Volumenarbeit
ΔU = QV + W
ΔU = QV - p ∙ ΔV
QV = ΔU + p ∙ 0
QV = ΔU
bei konstantem Druck: Qp = -154,0 kJ/mol = ΔH
Bei konstantem Druck gilt:
ΔU = Qp + W
ΔU = Qp – p ∙ ΔV Umstellen nach Q:
Qp = ΔU + p ∙ ΔV (= Qp = [U₂ + p ∙ V₂] – [U₁ + p ∙ V₁] )
Enthalpie H ist die spezielle Wärmeenergie bei konstantem Druck
(H von „heat"; Enthalpie: griech: En = darin; thalpos = Wärme)
Definition der Enthalpie: H = U + p ∙ V
→ Qp = H₂ – H₁ = ΔH
Prozessgrößen: Sind vom Weg abhängig (Bsp. Arbeit und Wärme) ⇨ unterschiedliche Werte, je nachdem ob man isobar oder isochor arbeitet.
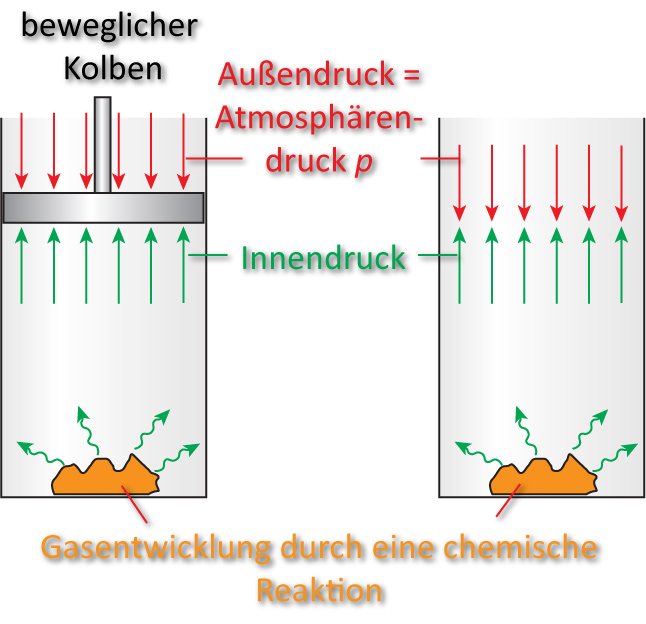
a) Offene Systeme
- die meisten chemischen Reaktionen
- Volumenarbeit
- nicht alles fällt als Wärmeenergie an:
↑ Zum Vergrößern klicken
Das entstehende Gas leistet mech. Arbeit gegen den Atmosphärendruck. Die gleiche Arbeit wird auch geleistet, wenn der Kolben fehlt (Außenluft wird verdrängt).
Die Arbeit des Kolbens beträgt: p ∙ ΔV = Volumenarbeit
Änderung Reaktionsenthalpie = Änderung Reaktionsenergie + Volumenarbeit
ΔH = ΔU + p ∙ ΔV
Beispiel:
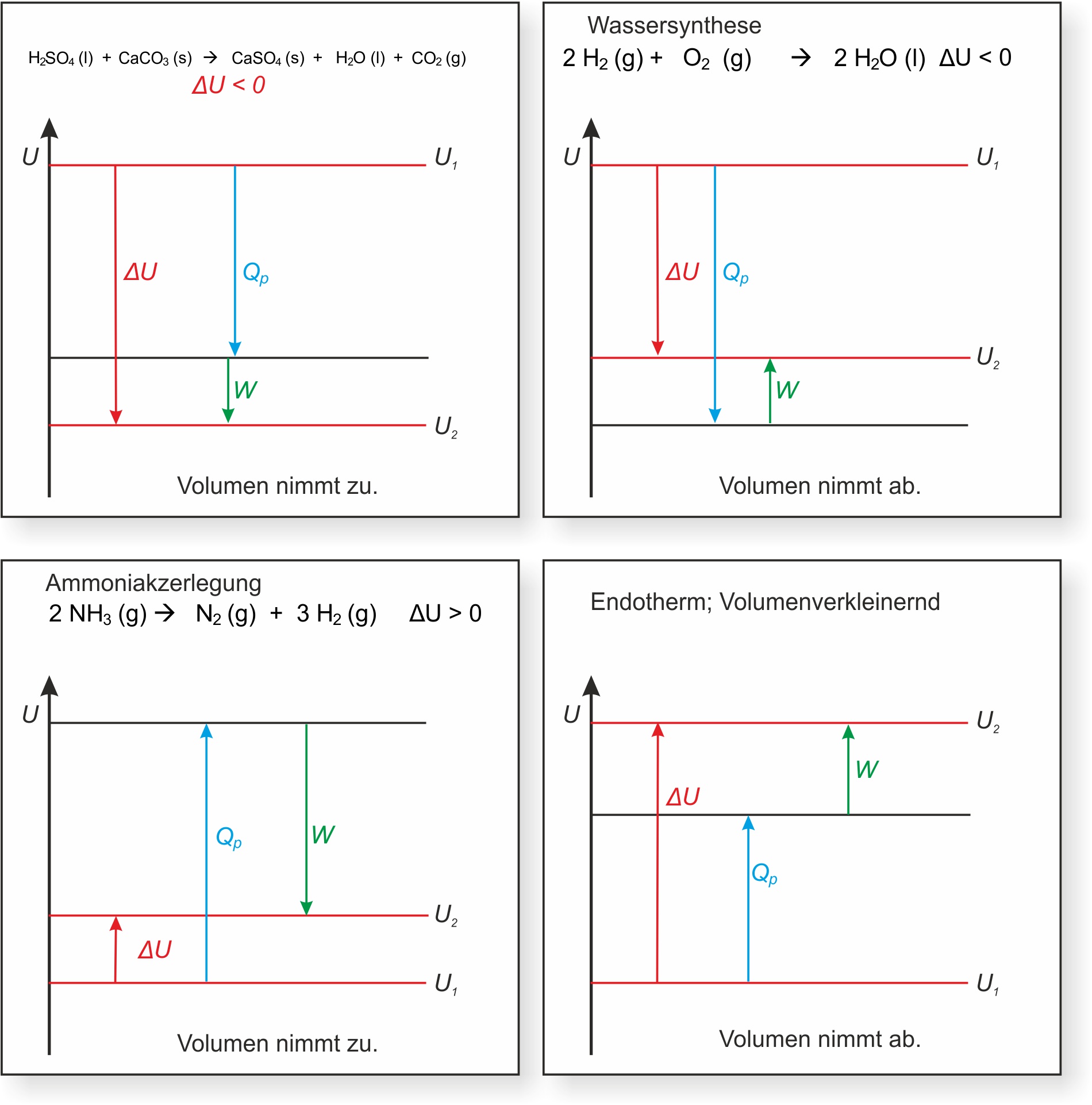
H₂SO₄ (l) + CaCO₃ (s) → CaSO₄ (s) + H₂O (l) + CO₂ (g)
Vm (CO₂) = 24,5 L/mol (bei 25 °C und 101,3 kPa = 101 300 N/m²);
ΔU = -96,1 kJ/mol
Bei der Reaktion von 1 mol Schwefelsäure:
p ∙ ΔV = 101 ∙ 10³ N/m² ∙ 24,5 ∙ 10⁻³ m³/mol
= 2,5 ∙ 10³ J/mol ( J = N ∙ m )
= 2,5 kJ/mol
ΔH = ΔU + p ∙ ΔV
= -96,1 kJ/mol + 2,5 kJ/mol
= -93,6 kJ/mol
b) Geschlossene Systeme
• keine mechanische Arbeit ⇨ ΔV = 0
• Die bei einer chemischen Reaktion gesamte freigesetzte Energie kann als Wärmeenergie anfallen (Ausnahme: z.B. Lichtenergie)
• Gesamtenergie = Reaktionsenergie ΔU (vgl. oben)
Q = ΔU + p ∙ 0
Q = ΔU
Merke: Die Energiemenge, die ein System bei konstantem Druck als Wärme an die Umgebung abgibt oder von ihr aufnimmt, wird Reaktionsenthalpie ΔH genannt.
Beispiele für chemische Reaktionen mit Volumenarbeit:
↑ Zum Vergrößern klicken
Auf einen Blick – die wichtigsten Aussagen
Isochor (V = const.)
QV = ΔU
Keine Volumenarbeit, gesamte Energie als Wärme
Isobar (p = const.)
Qp = ΔH
Wärme + Volumenarbeit p·ΔV
Enthalpie
H = U + p·V
→ ΔH = ΔU + p·ΔV
Prozessgrößen
Q und W sind wegabhängig – kein Δ-Symbol, kein fester Zustandswert
Häufige Fragen zur Reaktionswärme
Was ist der Unterschied zwischen QV und Qp?
QV ist die Reaktionswärme bei konstantem Volumen (isochor, z. B. im verschlossenen Bombenkalorimeter). Dabei ist keine Volumenarbeit möglich, daher gilt QV = ΔU. Qp ist die Reaktionswärme bei konstantem Druck (isobar, z. B. im offenen Laborgefäß). Hier wird zusätzlich Volumenarbeit geleistet, wenn Gase entstehen oder verbraucht werden. Deshalb gilt Qp = ΔH = ΔU + p·ΔV.
Warum ist Q keine Zustandsgröße und warum schreibt man kein ΔQ?
Wärme Q ist eine Prozessgröße – ihr Wert hängt davon ab, auf welchem Weg ein Zustandsübergang stattfindet (isobar oder isochor liefern verschiedene Q-Werte für dieselbe Reaktion). Zustandsgrößen wie U, H oder T beschreiben den aktuellen Zustand unabhängig vom Weg – sie erhalten daher das Δ-Symbol. Q selbst ist kein Zustand, sondern eine übertragene Energiemenge – daher schreibt man Q, nicht ΔQ.
Warum unterscheiden sich QV und Qp beim Zink-Versuch?
Bei der Reaktion Zn + 2 HCl → ZnCl₂ + H₂ entsteht 1 mol H₂-Gas. Dieses Gas dehnt sich aus und verrichtet Volumenarbeit gegen den Atmosphärendruck: p·ΔV ≈ 2,5 kJ/mol. Diese Energie steht nicht als Wärme zur Verfügung – daher ist Qp = −154,0 kJ/mol betragsmäßig kleiner als QV = −156,5 kJ/mol. Die Differenz beträgt genau 2,5 kJ/mol.
Was ist die Definition der Enthalpie H?
Die Enthalpie ist definiert als H = U + p·V. Sie fasst innere Energie und den Druckterm p·V zusammen. Bei isobaren Prozessen gilt ΔH = ΔU + p·ΔV. Die Enthalpieänderung ΔH entspricht genau der bei konstantem Druck messbaren Reaktionswärme Qp. Deshalb ist ΔH die in der Laborchemie gebräuchlichste thermodynamische Größe (→ 8 Enthalpie).
In welchem System gilt Q = ΔU, und warum?
Im geschlossenen (isochoren) System gilt ΔV = 0, daher ist die Volumenarbeit W = −p·ΔV = 0. Aus ΔU = Q + W folgt dann ΔU = Q. Die gesamte Energieänderung des Systems tritt als Wärme in Erscheinung – nichts geht als mechanische Arbeit verloren. Das ist der Messprinzip des Bombenkalorimeters.
Lernkarten – Reaktionswärme Q
Klicke auf eine Karte, um die Antwort zu sehen.
Was gilt für QV bei konstantem Volumen (isochor)?
QV = ΔU
ΔV = 0 → keine Volumenarbeit →
gesamte Reaktionsenergie als Wärme messbar
Was gilt für Qp bei konstantem Druck (isobar)?
Qp = ΔH = ΔU + p·ΔV
Ein Teil der Energie geht als Volumenarbeit ab –
Qp ≠ ΔU
Wie lautet die Definition der Enthalpie H?
H = U + p·V
→ ΔH = ΔU + p·ΔV
→ Qp = H₂ − H₁ = ΔH
Warum ist Q eine Prozessgröße und warum schreibt man kein ΔQ?
Q ist wegabhängig – isobar und isochor geben verschiedene Q-Werte.
Nur Zustandsgrößen erhalten ein Δ.
Richtig: Q, nicht ΔQ!
QV = −156,5 kJ/mol bei Zn + 2 HCl.
Wie groß ist Qp?
p·ΔV (1 mol H₂) ≈ 2,5 kJ/mol
Qp = ΔU + p·ΔV
= −156,5 + 2,5 = −154,0 kJ/mol
Weiter im Kapitel Energetik
← 4 Volumenarbeit W → 6 Wärmekapazität → 8 Enthalpie H ↑ 3 Innere Energie U
- Details
- Geschrieben von: Wolfram Hölzel