Was du auf dieser Seite lernst
Am Beispiel des Ammoniumchlorids lernst du, was eine umkehrbare Reaktion ist: NH₃ und HCl bilden NH₄Cl (Hinreaktion), und beim Erhitzen zerfällt NH₄Cl wieder in NH₃ und HCl (Rückreaktion). Das Protolysenschema zeigt, welche Stoffe als Säure und welche als Base wirken – und warum Protonenübertragungen immer „bergab" verlaufen.
Grundlagen aus der 9. Klasse
Die Brønsted-Definition von Säuren und Basen sowie korrespondierende Paare kennst du bereits aus der 9. Klasse: → Säure-Base-Definition nach Brønsted · → Reaktion HCl + NH₃ (Kl. 9)
1 Umkehrbare Reaktionen
1.1 Beispiel: Ammoniumchlorid
a) Bildung von Ammoniumchlorid
Über ein geöffnetes Schnappdeckelglas mit konzentriertem Ammoniak stellt man ein umgekehrtes Becherglas, in dessen Innenwand sich mit konzentrierter Salzsäure getränktes Filterpapier befindet.
↑ Zum Vergrößern klicken
✕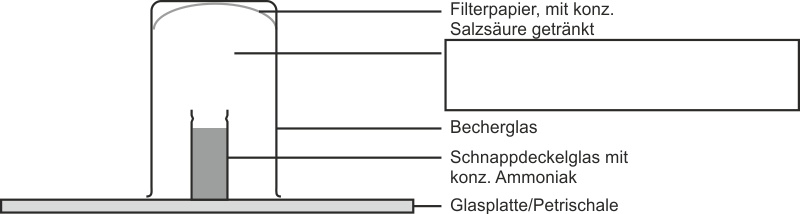
Beobachtung: Im Raum zwischen Schnappdeckelglas und Filterpapier bildet sich weißer Rauch. Auf der Glasplatte entsteht eine Schicht mit einem kristallinen weißen Feststoff.
Auswertung:
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕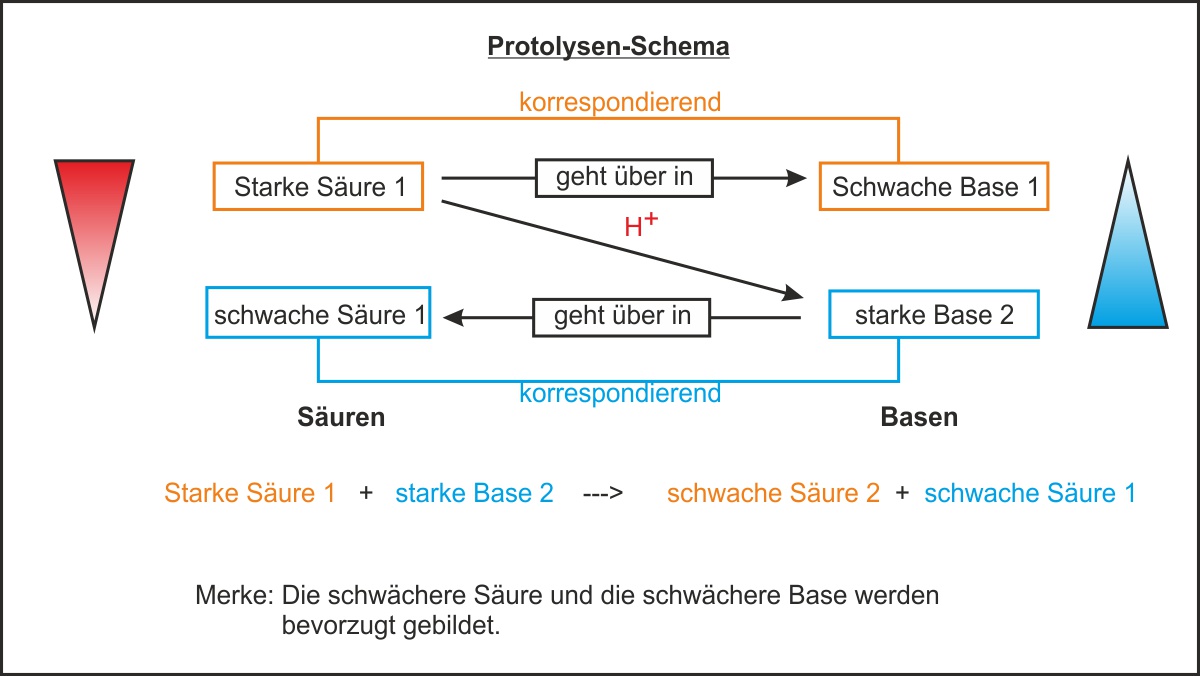
⚠️ Korrektur zum Tafelbild (untere Zeile):
Die untere Zeile des obigen Schemas enthält einen Druckfehler. Richtig lautet sie:
Starke Säure 1
+
starke Base 2
→
schwache Base 1
+
schwache Säure 2
(Dank an Fiona Ulrich für die Korrektur.)
↑ Zum Vergrößern klicken
✕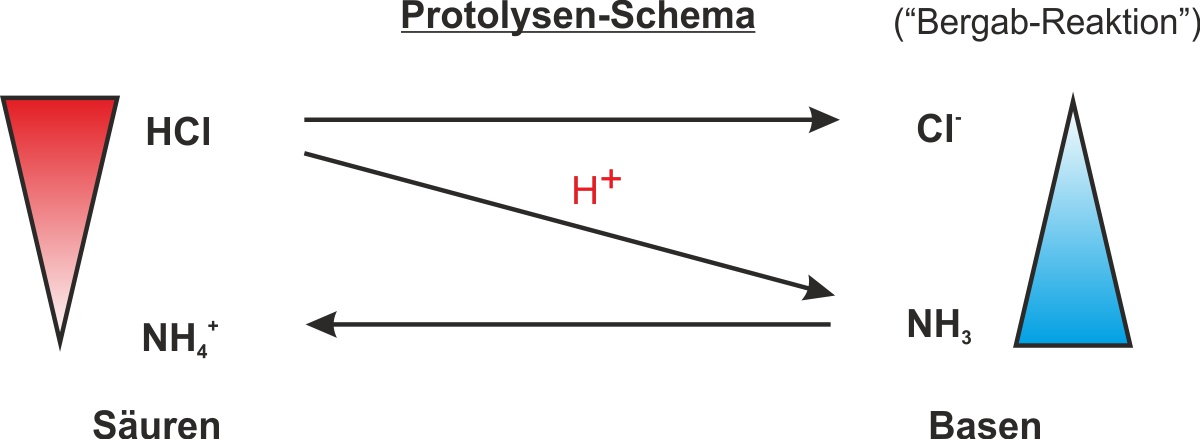
Bergab-Reaktion: Die Protolyse verläuft freiwillig von der stärkeren Säure zur schwächeren Säure – also „bergab" im Protolyseschema (vom großen roten Dreieck zum kleinen Dreieck).
b) Zerlegung von Ammoniumchlorid (Thermolyse)
Experiment: Man erhitzt in einem senkrecht eingespannten Reagenzglas festes Ammoniumchlorid.
↑ Zum Vergrößern klicken
✕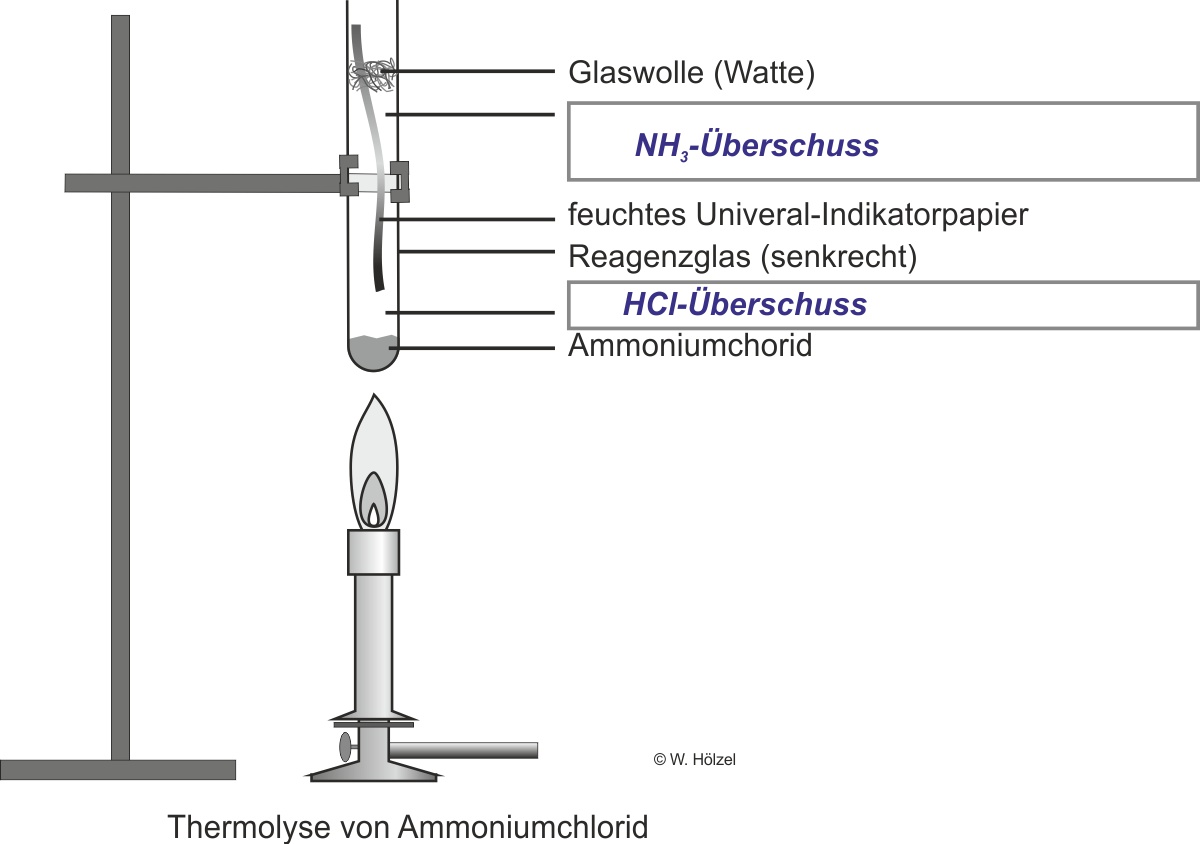
Beobachtung: Das feuchte pH-Papier färbt sich sowohl rot (Hinweis auf eine Säure – HCl-Überschuss unten) als auch blau (Hinweis auf eine Base – NH₃-Überschuss oben).
Erklärung: NH₃ diffundiert schneller (leichteres Molekül) und sammelt sich oben im Rohr, während HCl sich am Boden anreichert. Beide Gase entstehen gleichzeitig durch die Thermolyse.
Auswertung:
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕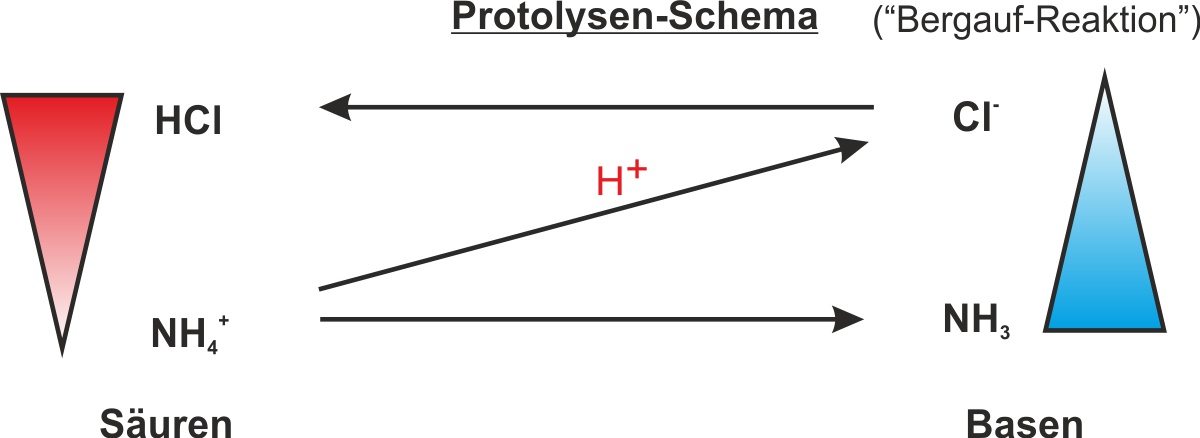
Bergauf-Reaktion: Die Thermolyse (Rückreaktion) verläuft erzwungen von der schwächeren Säure NH₄+ zur stärkeren Säure HCl – also „bergauf" im Protolyseschema. Sie benötigt Energie (ΔH > 0, endotherm).
c) Bildung und Zerlegung von Ammoniumchlorid – Zusammenfassung
Ammoniak + Chlorwasserstoff ⇌ Ammoniumchlorid
Der Doppelpfeil ⇌ zeigt: Es handelt sich um eine umkehrbare Reaktion, die in beide Richtungen ablaufen kann.
Hinweis – Reaktionen auf dem feuchten Indikatorpapier:
HCl + H2O → H3O+ + Cl−
(sauer → rot)
NH3 + H2O → NH4+ + OH−
(basisch → blau)
Auf einen Blick – die wichtigsten Aussagen
Umkehrbare Reaktion
NH₃ + HCl ⇌ NH₄Cl
Hin- und Rückreaktion sind möglich → ⇌-Pfeil
Bergab = freiwillig
Starke Säure + starke Base →
schwache Base + schwache Säure
ΔH < 0 (exotherm)
Bergauf = erzwungen
Schwache Säure + schwache Base →
starke Base + starke Säure
ΔH > 0 (endotherm) – braucht Energie
Korrespondierendes Paar
HCl / Cl⁻ und NH₄⁺ / NH₃ sind je ein korrespondierendes Säure-Base-Paar
Häufige Fragen – Umkehrbare Reaktionen / Ammoniumchlorid
Warum bildet sich beim Versuch weißer Rauch?
Gasförmiges Ammoniak (NH₃) aus dem Schnappdeckelglas und gasförmiger Chlorwasserstoff (HCl) aus dem Filterpapier treffen in der Luft aufeinander. Sie reagieren unmittelbar zu festem Ammoniumchlorid (NH₄Cl), das als winzige weiße Kristalle sichtbar wird – das nennt man weißen Rauch. Diese Reaktion ist exotherm (ΔH < 0) und verläuft freiwillig (→ Bergab-Reaktion im Protolyseschema).
Was bedeutet „Bergab-Reaktion" im Protolyseschema?
Im Protolyseschema werden Säuren von oben nach unten nach ihrer Stärke geordnet (starke Säure oben = großes umgekehrtes Dreieck). Eine Protolyse verläuft freiwillig immer von der stärkeren Säure zur schwächeren Säure – also „bergab". Im Beispiel HCl + NH₃: HCl (stärkere Säure, oben) überträgt H⁺ auf NH₃ (stärkere Base, oben) → Produkte Cl⁻ und NH₄⁺ befinden sich auf niedrigerem Niveau → Bergab-Reaktion, freiwillig. Mehr dazu: Brønsted-Definition (Kl. 9).
Warum färbt sich das Indikatorpapier sowohl rot als auch blau?
Beim Erhitzen von NH₄Cl entstehen gleichzeitig NH₃ (Gas, basisch) und HCl (Gas, sauer). Da NH₃ als leichteres Molekül schneller diffundiert, sammelt es sich im oberen Teil des Reagenzglases und färbt das Indikatorpapier dort blau (basisch). HCl reichert sich im unteren Teil an und färbt es rot (sauer). Das Indikatorpapier muss feucht sein, damit die Gase reagieren können: HCl + H₂O → H₃O⁺ + Cl⁻ und NH₃ + H₂O → NH₄⁺ + OH⁻.
Was ist der Unterschied zwischen NH₃ und NH₄⁺?
NH₃ (Ammoniak) ist eine schwache Base: Es nimmt ein Proton auf → NH₄⁺ (Ammonium-Ion, schwache Säure). NH₃ und NH₄⁺ bilden ein korrespondierendes Säure-Base-Paar. NH₃ hat keine Ladung und ist gasförmig, NH₄⁺ ist ein Ion und liegt in Salzen wie NH₄Cl als Feststoff vor.
Warum ist die Zerlegung von NH₄Cl eine „Bergauf-Reaktion"?
Die Thermolyse NH₄Cl → NH₃ + HCl läuft von der schwächeren Säure NH₄⁺ zur stärkeren Säure HCl – also „bergauf" im Protolyseschema. Sie verläuft nicht freiwillig, sondern muss durch Wärmezufuhr erzwungen werden (ΔH > 0, endotherm). Das ist möglich, weil beide Produkte gasförmig sind und das Gleichgewicht durch Entweichen der Gase auf die Produktseite gezogen wird.
Lernkarten – Umkehrbare Reaktionen
Klicke auf eine Karte, um die Antwort zu sehen.
Was beobachtet man, wenn NH₃ und HCl-Gas aufeinandertreffen?
Bildung von weißem Rauch (festes NH₄Cl): NH₃ + HCl → NH₄Cl (exotherm, ΔH < 0)
Was bedeutet ⇌ in einer Reaktionsgleichung?
Die Reaktion ist umkehrbar – sie kann sowohl in Hin- als auch in Rückrichtung ablaufen.
Was ist das korrespondierende Paar zur Säure HCl?
HCl (Säure) / Cl⁻ (konjugierte Base)
HCl gibt H⁺ ab → Cl⁻ entsteht.
Warum verläuft die Bildung von NH₄Cl „bergab"?
HCl ist eine stärkere Säure als NH₄⁺.
Protolyse läuft freiwillig von stärkerer → schwächerer Säure,
d. h. „bergab" im Protolyseschema.
Aufgabe: Ordne zu – Bergab oder Bergauf?
a) NH₄Cl → NH₃ + HCl (Thermolyse)
b) HCl + NH₃ → NH₄Cl (Bildung)
a) Bergauf (erzwungen, endotherm, ΔH > 0)
b) Bergab (freiwillig, exotherm, ΔH < 0)
Weiter im Kapitel Gleichgewichtsreaktionen
← Übersicht Gleichgewichtsreaktionen → 1.2 Beispiel: Calciumhydroxid
🔁 Grundlagen (Kl. 9): Brønsted-Definition · Reaktion HCl + NH₃
📌 Weiterführend: Prinzip von Le Chatelier · Massenwirkungsgesetz
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Am zweiten Beispiel Calciumhydroxid vertiefst du das Prinzip der umkehrbaren Reaktionen: Calciumoxid (gebrannter Kalk) reagiert mit Wasser exotherm zu Calciumhydroxid (Löschkalk). Beim Erhitzen läuft die Rückreaktion ab. Du lernst das Protolyseschema für diesen Vorgang und die wichtigsten Anwendungen von Kalk in Alltag und Technik.
Vorheriges Beispiel
Das Prinzip der umkehrbaren Reaktion und das Protolyseschema (Bergab/Bergauf) wurden am ersten Beispiel eingeführt: → 1.1 Beispiel: Ammoniumchlorid
1.2 Beispiel: Calciumhydroxid
Calciumoxid
„gebrannter Kalk"
Calciumhydroxid
„gelöschter Kalk" / „Löschkalk"
Kalkwasser
gesättigte wässrige Lösung
a) Bildung von Calciumhydroxid – „Löschen von gebranntem Kalk"
↑ Zum Vergrößern klicken
✕
Experiment: Man gibt destilliertes Wasser auf Calciumoxid (CaO, gebrannter Kalk).
Beobachtung:
- Die Reaktion verläuft stark exotherm – der Feststoff wird sehr heiß, zischt und dampft.
- Das Calciumoxid bläht sich auf und zerfällt zu einem weißen, krümeligen Pulver.
- Eine wässrige Lösung (Kalkwasser) ist alkalisch (pH > 7).
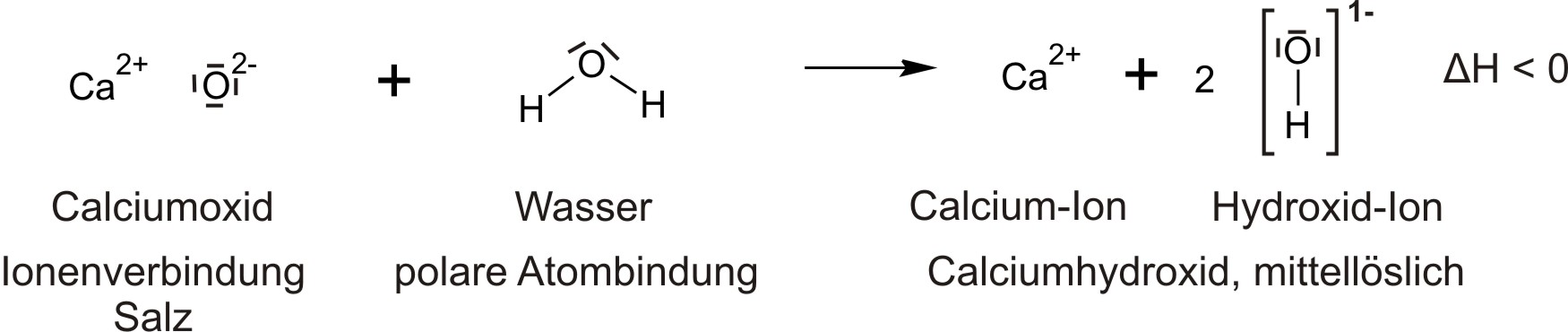
Auswertung:
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕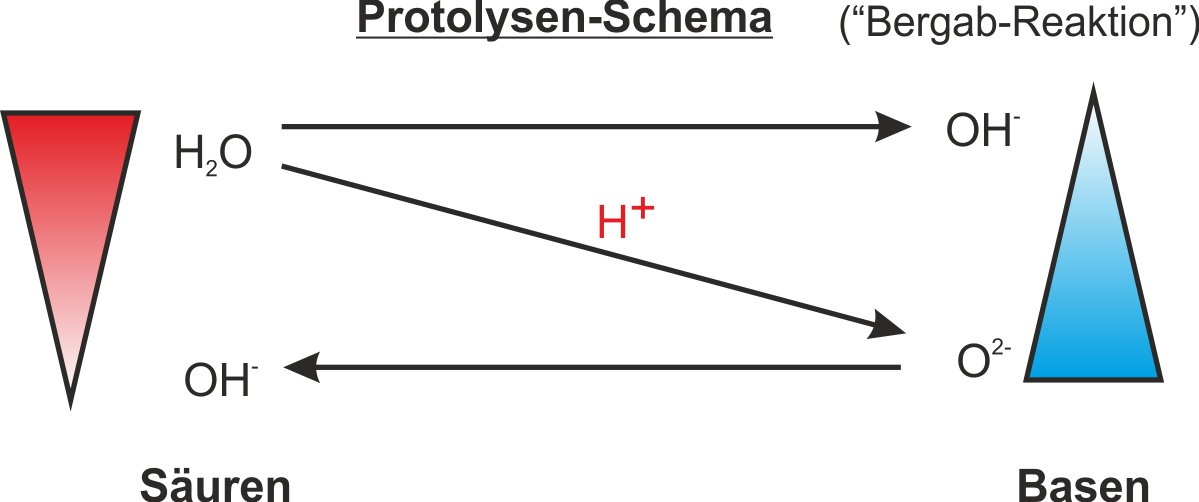
Bergab-Reaktion: Das Oxid-Ion O2− ist eine sehr starke Base – stärker als OH−. Daher überträgt H2O (Säure) ein Proton auf O2− (stärkere Base) → freiwillige, exotherme Reaktion (ΔH < 0).
b) Erhitzen von Calciumhydroxid
Experiment: Man erhitzt festes Calciumhydroxid Ca(OH)₂ stark.
Beobachtung:
- Das Calciumhydroxid zerfällt bei starkem Erhitzen (ab ca. 512 °C) wieder in CaO und H₂O.
- Wasserdampf entweicht.
- Es bleibt weißes Calciumoxid zurück.
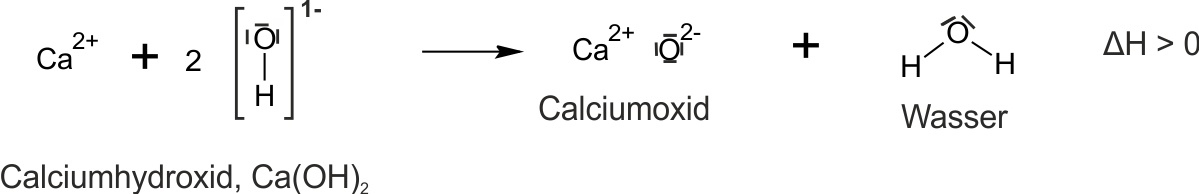
Auswertung:
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕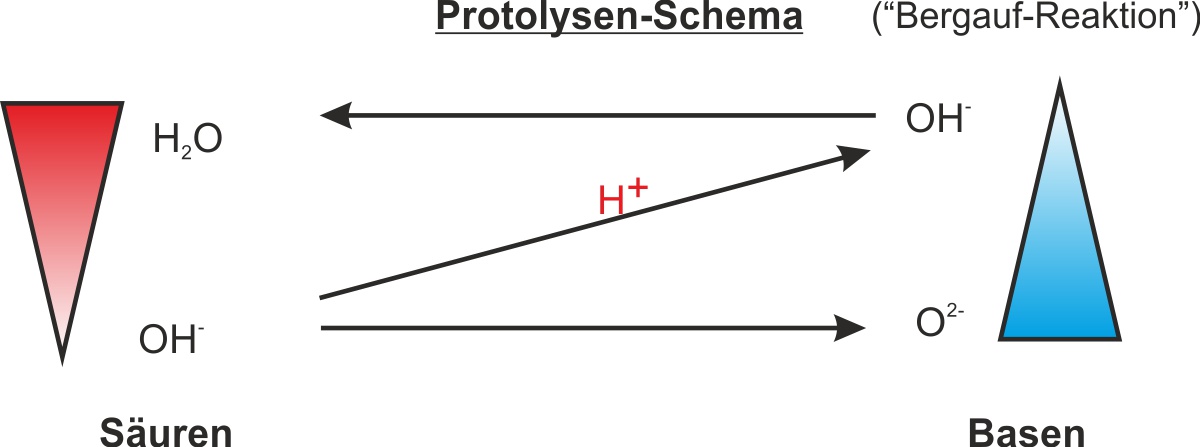
Bergauf-Reaktion: OH− ist eine schwächere Säure als H2O. Um H+ auf ein O2− zu übertragen und so H2O und CaO zurückzubilden, muss Energie (Wärme) zugeführt werden – erzwungene, endotherme Reaktion (ΔH > 0).
c) Bildung und Zerlegung – Zusammenfassung
Calciumoxid + Wasser ⇌ Calciumhydroxid
Anwendungen von Kalk
Calciumoxid und Calciumhydroxid spielen in Technik und Alltag eine große Rolle. Das Verständnis der umkehrbaren Reaktion CaO + H₂O ⇌ Ca(OH)₂ ist der Schlüssel zu diesen Anwendungen.
🏗️ Bauindustrie – Kalkputz & Mörtel
Ca(OH)₂ (Löschkalk) wird zu Mörtel und Kalkputz verarbeitet.
Beim Abbinden reagiert Ca(OH)₂ mit CO₂ der Luft zu festem Calciumcarbonat:
Ca(OH)₂ + CO₂ → CaCO₃ + H₂O
Das ist der „Carbonatisierungsprozess" (Ca(OH)₂ „erhärtet").
🧪 CO₂-Nachweis – Kalkwasser
Kalkwasser (gesättigte Ca(OH)₂-Lösung) trübt sich durch CO₂-Einleiten weiß:
Ca(OH)₂ + CO₂ → CaCO₃↓ + H₂O
CaCO₃ ist schwer löslich und fällt als weißer Feststoff aus.
Klassischer Nachweisreaktion für CO₂!
🌱 Landwirtschaft – Kalkung des Bodens
Saure Böden werden mit gebranntem Kalk (CaO) oder Löschkalk (Ca(OH)₂) gekalkt, um den pH-Wert anzuheben und Nährstoffe verfügbar zu machen.
⚠️ Sicherheitshinweis
Das Löschen von Kalk erzeugt sehr hohe Temperaturen (bis ~300 °C an der Oberfläche). CaO und Ca(OH)₂ sind stark basisch (pH ≈ 12,5) und reizen Augen und Haut – Schutzausrüstung verwenden!
Auf einen Blick – die wichtigsten Aussagen
Kalklöschen
CaO + H2O → Ca(OH)2
Stark exotherm (ΔH ≪ 0), freiwillig
Erhitzen
Ca(OH)2 → CaO + H2O
Endotherm (ΔH > 0), braucht Energie
CO₂-Nachweis
Ca(OH)2 + CO2 → CaCO3↓ + H2O
Kalkwasser trübt sich weiß
O²⁻ – stärkste Base
O2− ist stärkere Base als OH− → Bergab-Protolyse durch H2O
Häufige Fragen – Calciumhydroxid / Kalk
Warum ist die Bildung von Ca(OH)₂ so stark exotherm?
Das Oxid-Ion O2− im CaO ist eine außerordentlich starke Base – stärker als OH−. Es zieht Protonen regelrecht aus Wassermolekülen heraus: O2− + H₂O → 2 OH−. Da diese Protolyse sehr weit „bergab" geht (von einer sehr starken Base zu einer deutlich schwächeren), wird viel Energie frei (ΔH ≪ 0). Sichtbar: Die Masse wird sehr heiß, Wasserdampf entweicht.
Wie unterscheiden sich gebrannter Kalk, Löschkalk und Kalkwasser?
Gebrannter Kalk (Branntkalk, Ätzkalk): CaO – weißer Feststoff, entsteht durch
Brennen von Kalkstein (CaCO₃) bei ca. 900 °C.
Löschkalk (gelöschter Kalk): Ca(OH)₂ – weißes Pulver, entsteht durch Löschen
(Zugabe von Wasser zu CaO).
Kalkwasser: Ca(OH)₂ (aq) – gesättigte wässrige Lösung von Calciumhydroxid,
schwach basisch (pH ≈ 12,5). Dient als CO₂-Nachweis.
Wie funktioniert der CO₂-Nachweis mit Kalkwasser?
Leitet man CO₂ in Kalkwasser ein, entsteht schwer lösliches Calciumcarbonat: Ca(OH)₂ + CO₂ → CaCO₃↓ + H₂O. Das ausgefallene CaCO₃ macht die Lösung milchig trüb – ein einfacher, sicherer Nachweis für Kohlenstoffdioxid. Bei zu viel CO₂ löst sich das CaCO₃ wieder auf (CaCO₃ + CO₂ + H₂O → Ca(HCO₃)₂), die Lösung wird wieder klar.
Warum ist die Zerlegung von Ca(OH)₂ eine Bergauf-Reaktion?
OH− ist eine schwächere Säure als H₂O. Um OH− zur Protonenabgabe zu zwingen und O2− zurückzubilden, muss man Energie (Wärme) zuführen – die Reaktion läuft bergauf im Protolyseschema und ist endotherm (ΔH > 0). Erst oberhalb von ca. 512 °C wird Ca(OH)₂ thermisch zersetzt.
Warum verwendet man Kalk im Bau?
Ca(OH)₂ (Löschkalk) wird mit Sand zu Kalkputz oder -mörtel gemischt. Beim Abbinden (Trocknen) reagiert Ca(OH)₂ mit CO₂ der Luft: Ca(OH)₂ + CO₂ → CaCO₃ + H₂O. Festes Calciumcarbonat (CaCO₃) ist hart und druckfest. Kalkputz ist dampfdiffusionsoffen (reguliert Feuchtigkeit) und fungizid (hemmt Schimmel) durch seinen hohen pH-Wert. Mehr zur Reaktion Säure-Base: Neutralisation (Kursstufe).
Lernkarten – Calciumhydroxid
Klicke auf eine Karte, um die Antwort zu sehen.
Welche Reaktionsgleichung beschreibt das Löschen von Kalk?
CaO + H2O → Ca(OH)2
(stark exotherm, ΔH ≪ 0, freiwillig = Bergab)
Warum reagiert CaO so heftig mit Wasser?
O2− ist eine sehr starke Base – stärker als OH−. Protolyse verläuft sehr weit bergab → große Energiefreisetzung.
Wie weist man CO₂ mit Kalkwasser nach?
Ca(OH)2 + CO2 → CaCO3↓ + H2O
Kalkwasser trübt sich weiß → CO₂ nachgewiesen.
Nenne drei Anwendungen von Kalk.
1. Kalkputz/Mörtel (Bau)
2. CO₂-Nachweis (Kalkwasser)
3. Bodenkalkung (Landwirtschaft)
Aufgabe: Bergab oder Bergauf?
a) CaO + H₂O → Ca(OH)₂
b) Ca(OH)₂ →(Δ) CaO + H₂O
a) Bergab – freiwillig, exotherm, ΔH < 0
b) Bergauf – erzwungen durch Wärme, endotherm, ΔH > 0
Weiter im Kapitel Gleichgewichtsreaktionen
← 1.1 Beispiel: Ammoniumchlorid → 2. Das chemische Gleichgewicht
📌 Weiterführend: Prinzip von Le Chatelier · Säure-Base-Reaktionen in Salzlösungen
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Konzentrierte Schwefelsäure ist hygroskopisch – sie nimmt begierig Wasser aus der Luft auf. Auf dieser Seite untersuchst du, wie sich dabei ein dynamisches Gleichgewicht einstellt, und lernst die zweistufige Protolyse der Schwefelsäure mit Wasser kennen.
Grundlagen aus der 9. Klasse
Die Grundlagen zu Säure-Base-Reaktionen und der Bronsted-Definition hast du bereits in der 9. Klasse kennengelernt: → Säure-Base-Definition nach Brønsted (Kl. 9)
2.1 Schwefelsäure – Wasserdampf – Gleichgewicht
a) konzentrierte Schwefelsäure (H2SO4)
- enthält Schwefelsäuremoleküle
- zeichnet einmal die Strukturformel(n) (unter Berücksichtigung, dass die Edelgas-Regel erfüllt sein muss):
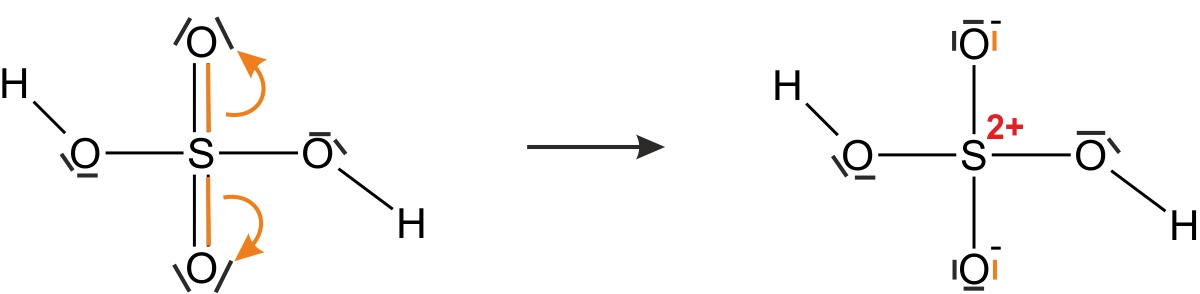
- Konzentrierte Schwefelsäure ist geruchlos.
- Siedetemperatur beträgt 300 °C.
- Konzentrierte Schwefelsäure reagiert heftig mit Wasser unter Ionenbildung (Protolyse-Reaktion).
Formuliert für die Reaktion der Schwefelsäure mit Wasser in zwei Stufen die Reaktionsgleichung in Summenformeln:
Lösung: Reaktionsgleichungen (zweistufige Protolyse)
H2SO4 + H2O → HSO4− + H3O+
HSO4− + H2O → SO42− + H3O+
b) Verdünnte Schwefelsäure
Verdünnte Schwefelsäure enthält folgende Ionen und Moleküle; nennt diese:
Lösung: Bestandteile verdünnter Schwefelsäure
- H3O+ (Oxonium-Ion; früher Hydronium-Ion oder „Hydroxonium-Ion")
- HSO4− (Hydrogensulfat-Ion)
- SO42− (Sulfat-Ion; in geringer Konzentration)
- H2O (Wasser; in großer Menge vorhanden)
2.2 Langzeitversuch: Konzentrierte Schwefelsäure
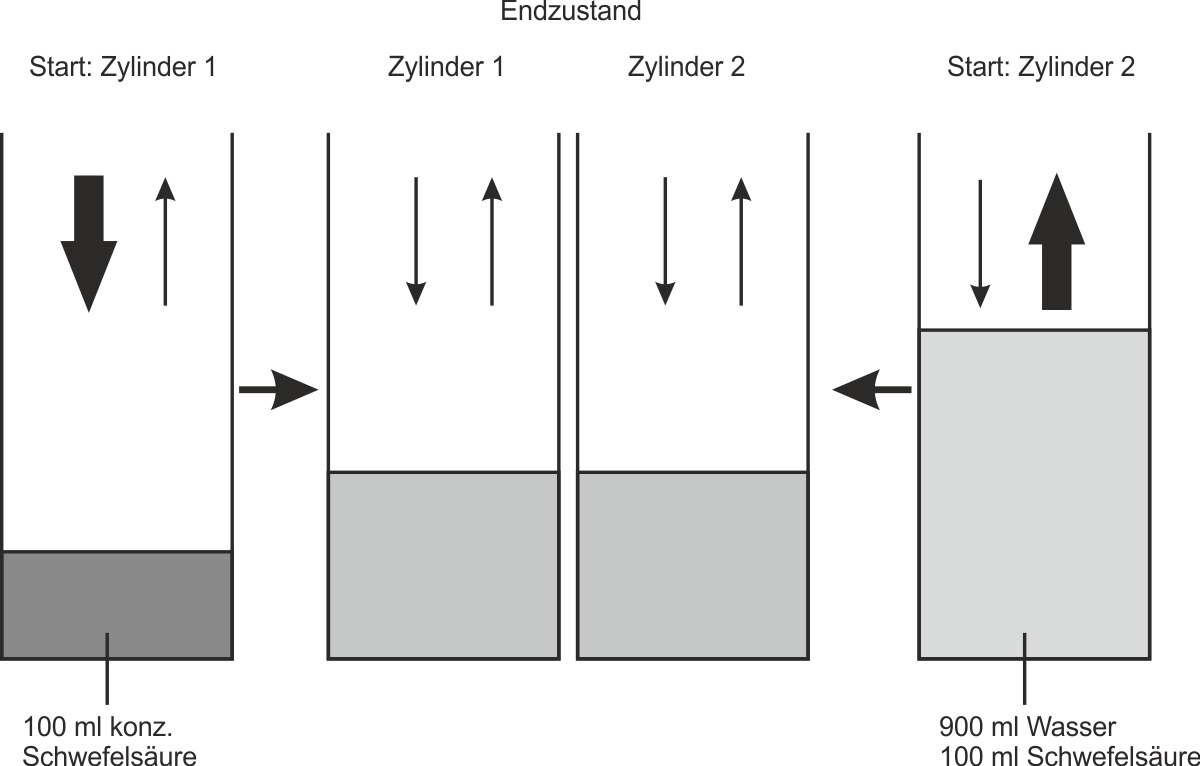
Versuchsdurchführung: In einen Zylinder 1 werden 100 ml konzentrierte Schwefelsäure gegeben. In einen Zylinder 2 werden zunächst 900 ml Wasser und dann vorsichtig 100 ml konzentrierte Schwefelsäure gegeben. Beide Zylinder werden mehrere Jahre offen im gleichen Zimmer stehengelassen.
↑ Zum Vergrößern klicken
✕
Versucht eine Deutung dieses Versuchs:
Lösung: Deutung des Langzeitversuchs
- Zylinder 1 (konz. H2SO4) nimmt mehr H2O-Moleküle aus der Umgebungsluft auf, als er abgibt.
- Zylinder 2 (verdünnte H2SO4) gibt mehr H2O-Moleküle an die Umgebungsluft ab, als er aufnimmt.
- Nach einigen Jahren hat sich ein Gleichgewichtszustand eingestellt: Pro Zeiteinheit werden gleich viele H2O-Moleküle an die Umgebung abgegeben wie H2O-Moleküle in die Lösung aufgenommen werden.
Auf einen Blick – die wichtigsten Aussagen
Hygroskopie
Konzentrierte H2SO4 ist hygroskopisch – sie zieht Wasser aus der Luft an. Je konzentrierter die Lösung, desto stärker diese Eigenschaft.
Dynamisches Gleichgewicht
Im Gleichgewicht sind Auf- und Abgabe von H2O-Molekülen gleich groß – es herrscht mikroskopische Aktivität bei makroskopischer Konstanz.
Zweistufige Protolyse
H2SO4 gibt in zwei Stufen je ein Proton ab. Im zweiten Schritt ist HSO4− eine schwächere Säure als H2SO4.
Siedepunkt 300 °C
Der hohe Siedepunkt von 300 °C erklärt sich durch starke zwischenmolekulare Kräfte (Wasserstoffbrücken und van-der-Waals-Kräfte).
Häufige Fragen – Schwefelsäure-Gleichgewicht
Was bedeutet „hygroskopisch" und warum ist konzentrierte Schwefelsäure so wassergierig?
Als hygroskopisch bezeichnet man Stoffe, die Wasser aus der Umgebungsluft aufnehmen. Konzentrierte H2SO4 reagiert heftig mit Wasser unter starker Wärmefreisetzung (Protolyse). Da diese Reaktion sehr exotherm ist, liegt das Gleichgewicht stark auf der Seite der Produkte – die Säure „zieht" Wassermoleküle regelrecht aus der Luft, bis sich ein dynamisches Gleichgewicht eingestellt hat.
Warum gibt verdünnte Schwefelsäure Wasser an die Luft ab, konzentrierte aber nicht?
Der entscheidende Faktor ist der Wasserdampfdruck der Lösung. Verdünnte Schwefelsäure hat einen höheren Wasserdampfdruck als die Umgebungsluft → H2O-Moleküle verdunsten. Konzentrierte H2SO4 hat dagegen einen sehr niedrigen Wasserdampfdruck → sie nimmt Wasser auf. Im Langzeitversuch gleichen sich beide Zylinder auf einen gemeinsamen Gleichgewichtszustand an. Mehr dazu auf der Seite Verschiebung des Gleichgewichts.
Was ist ein chemisches Gleichgewicht und woran erkennt man es?
Ein chemisches Gleichgewicht liegt vor, wenn Hin- und Rückreaktion gleich schnell ablaufen. Äußerlich scheint die Reaktion zum Stillstand gekommen zu sein (makroskopische Konstanz), auf molekularer Ebene laufen aber ständig beide Richtungen ab (dynamisches Gleichgewicht). Im Langzeitversuch erkennt man das Gleichgewicht daran, dass sich die Füllhöhen der Zylinder nicht mehr verändern. Weitere Merkmale findest du auf der Seite Merkmale eines chemischen Gleichgewichts.
Wie läuft die zweistufige Protolyse der Schwefelsäure mit Wasser ab?
H2SO4 ist eine zweiprotonige Säure und gibt ihre Protonen in zwei Schritten ab:
1. Stufe (vollständig):
H2SO4 + H2O → HSO4− + H3O+
2. Stufe (unvollständig):
HSO4− + H2O ⇌ SO42− + H3O+
Da HSO4− eine schwächere Säure ist, läuft die zweite Stufe nicht vollständig ab → daher enthält verdünnte Schwefelsäure sowohl SO42−- als auch HSO4−-Ionen. Die Grundlagen zur Protolyse hast du in der 9. Klasse kennengelernt: Bronsted-Definition (Kl. 9).
Warum darf man niemals Wasser zu konzentrierter Schwefelsäure geben?
Die Reaktion von konz. H2SO4 mit Wasser ist stark exotherm. Gibt man Wasser zu Säure, kann sich das Wasser an der Oberfläche spontan in Dampf verwandeln, was zu einem explosionsartigen Verspritzen der Säure führt. Richtig ist daher: immer Säure langsam in Wasser geben, nie umgekehrt! Die thermodynamischen Hintergründe (Reaktionsenthalpie) findest du in der Einheit Enthalpie H (Energetik).
Lernkarten – Schwefelsäure-Gleichgewicht
Klicke auf eine Karte, um die Antwort zu sehen.
Was bedeutet „hygroskopisch" und welcher bekannte Stoff zeigt diese Eigenschaft besonders stark?
Hygroskopisch = Wasser aus der Luft aufnehmend. Konzentrierte H2SO4 ist ein typisches Beispiel: Sie kann sogar organische Stoffe durch Wasserentzug verkohlen.
Nenne die vier Teilchenarten, die in verdünnter Schwefelsäure vorhanden sind.
H3O+ (Oxonium-Ion) · HSO4− (Hydrogensulfat-Ion) · SO42− (Sulfat-Ion, wenig) · H2O (viele Wassermoleküle)
Was passiert mit Zylinder 1 (konz. H2SO4) und Zylinder 2 (verd. H2SO4) im Langzeitversuch?
Zylinder 1 nimmt H2O auf → Füllstand steigt. Zylinder 2 gibt H2O ab → Füllstand sinkt. Nach Jahren: gleiche Konzentration → dynamisches Gleichgewicht.
Schreibe die zweistufige Protolyse von H2SO4 mit Wasser auf.
H2SO4 + H2O → HSO4− + H3O+
HSO4− + H2O ⇌ SO42− + H3O+
(Stufe 1 vollständig, Stufe 2 unvollständig)
Berechne die Stoffmenge H2SO4 in 100 ml konz. Schwefelsäure (ρ = 1,84 g/ml; w = 98 %; M = 98 g/mol).
m(Lösung) = 100 ml · 1,84 g/ml = 184 g
m(H2SO4) = 184 g · 0,98 = 180,3 g
n = 180,3 g ÷ 98 g/mol ≈ 1,84 mol
Weiter im Kapitel Gleichgewichtsreaktionen
← Calciumhydroxid-Gleichgewicht → Modellexperiment: Stechheberversuch
🔁 Verwandte Seiten: Merkmale eines chemischen Gleichgewichts · Prinzip von Le Chatelier · Brønsted-Definition (Kl. 9)
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Der Stechheberversuch ist ein mechanisches Modell für chemische Gleichgewichte. Du erkennst, warum Hin- und Rückreaktion gleichzeitig ablaufen, warum beide Startbedingungen zum selben Gleichgewichtszustand führen – und wie sich das in Diagrammen zeigt.
Grundlagen aus diesem Kapitel
Den Begriff der umkehrbaren Reaktion hast du auf der vorherigen Seite kennengelernt: → Umkehrbare Reaktionen
2.3 Modellexperiment – Stechheberversuch
Vergleiche dazu auch das ausgeteilte Arbeitsblatt zum Experiment.
↑ Zum Vergrößern klicken
✕
Versuch 1: Flüssigkeit gelangt von A nach B. Die reversible Reaktion setzt mit der „Hinreaktion" ein. Anschließend gelangt auch Flüssigkeit von B zurück nach A – es findet also auch eine „Rückreaktion" statt. Nach einiger Zeit sind die in den Rohren im gleichen Takt beförderten Flüssigkeitsportionen gleich groß geworden.
Wie könnten die Endzustände bei den Experimenten 1 und 2 aussehen?
Lösung: Endzustand Versuch 1 und 2
Versuch 1 und Versuch 2 führen zum gleichen Ergebnis – dem Gleichgewichtszustand. Unabhängig von der Startbedingung (ob die Flüssigkeit zunächst in A oder in B ist) stellt sich dieselbe Gleichgewichtsverteilung ein:
↑ Zum Vergrößern klicken
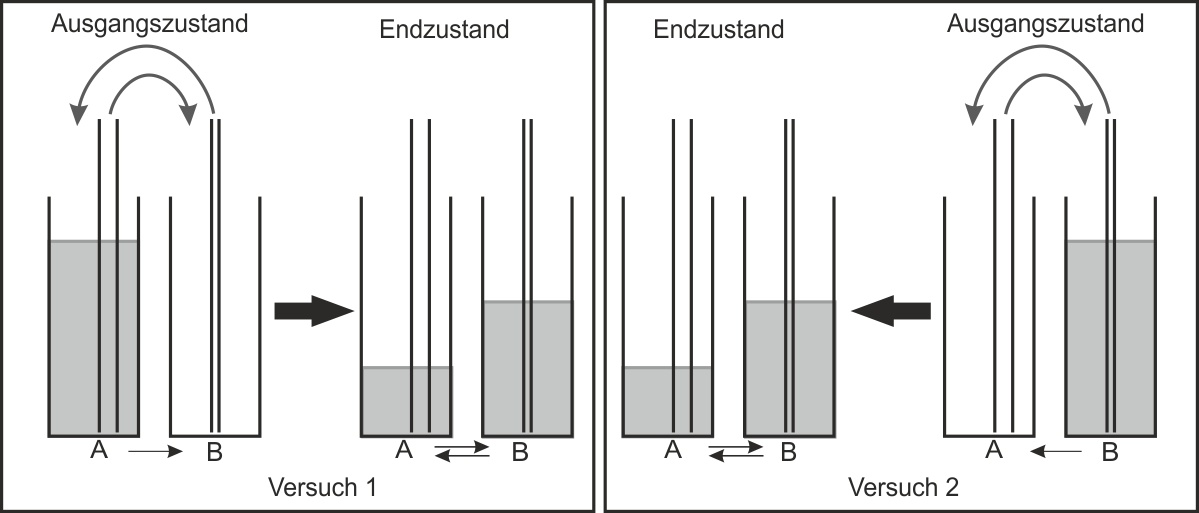
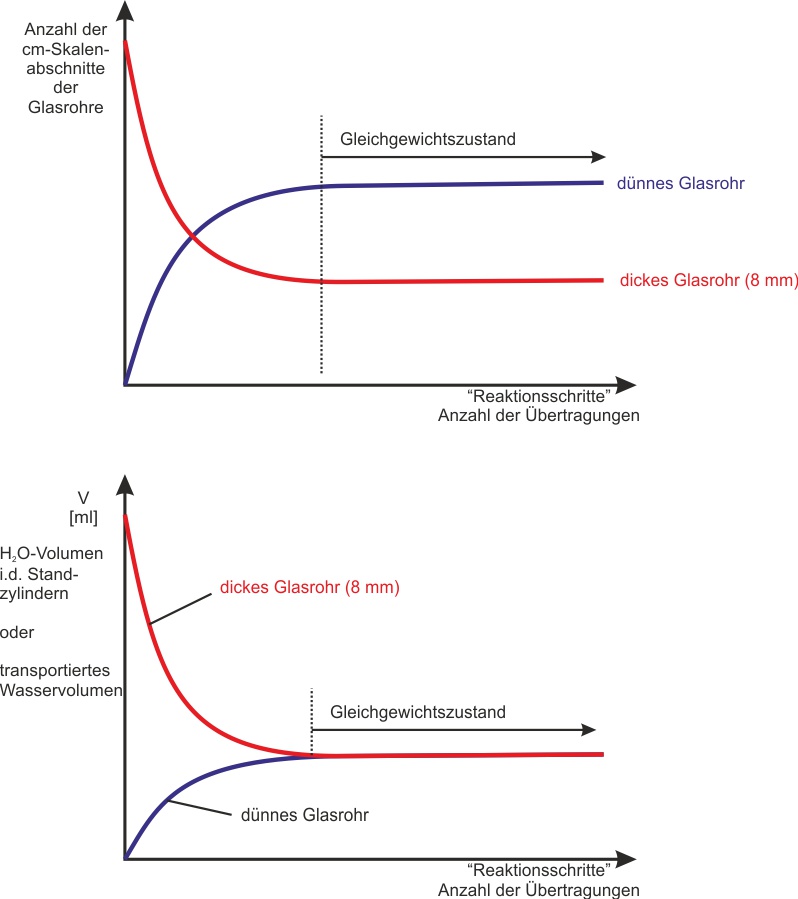
Was für ein Diagramm bekommt man, wenn man das Volumen in den Standzylindern gegen die Anzahl der Übertragungen aufträgt? Und wie sieht das Diagramm aus, wenn man das transportierte Volumen innerhalb der Glasrohre gegen die Zeit aufträgt?
✕
Auf einen Blick – die wichtigsten Aussagen
Gleiches Ergebnis
Versuch 1 und Versuch 2 führen zum selben Gleichgewichtszustand – unabhängig davon, von welcher Seite der Prozess startet.
Dynamisch
Im Gleichgewicht fließt noch immer Flüssigkeit in beide Richtungen – nur die transportierten Portionen sind gleich groß. Äußerlich: Stillstand. Innerlich: Aktivität.
Diagrammform
Die Kurven nähern sich asymptotisch einem konstanten Wert. Das gilt für das Volumen in den Zylindern ebenso wie für das transportierte Volumen in den Rohren.
Modellcharakter
Der Versuch ist eine mechanische Analogie. Die „Rohrdurchmesser" entsprechen den unterschiedlichen Reaktionsgeschwindigkeiten von Hin- und Rückreaktion.
Häufige Fragen – Stechheberversuch
Was zeigt der Stechheberversuch über chemische Gleichgewichte?
Der Stechheberversuch ist ein Modellexperiment: Zwei Standzylinder (A und B) sind über Glasrohre verbunden. Flüssigkeit wird abwechselnd von A nach B und von B nach A transportiert – analog zu Hin- und Rückreaktion. Nach einigen Schritten sind die transportierten Portionen gleich groß: Das Modell hat das dynamische Gleichgewicht erreicht. Die eigentlichen Merkmale eines chemischen Gleichgewichts findest du auf der Seite Merkmale eines chemischen Gleichgewichts.
Warum führen Versuch 1 und Versuch 2 zum gleichen Endzustand?
In Versuch 1 ist zu Beginn alles in A, in Versuch 2 alles in B. Trotzdem endet beides in derselben Gleichgewichtsverteilung. Das zeigt ein zentrales Merkmal chemischer Gleichgewichte: Der Gleichgewichtszustand ist unabhängig vom Startpunkt – er hängt nur von den Reaktionsbedingungen (Temperatur, Konzentration) ab, nicht davon, von welcher Seite man startet.
Was bedeutet „dynamisch" beim Gleichgewicht – ist da wirklich noch etwas in Bewegung?
Ja! Im Gleichgewicht hört der Transport nicht auf. Pro Schritt fließt weiterhin Flüssigkeit von A nach B und von B nach A – nur die Mengen sind gleich groß. Makroskopisch sieht es aus wie Stillstand (die Füllhöhen ändern sich nicht mehr), mikroskopisch ist das System aktiv. Deshalb: dynamisches Gleichgewicht, nicht statisches. Dasselbe Prinzip gilt für chemische Reaktionen: Hin- und Rückreaktion laufen gleichzeitig mit gleicher Geschwindigkeit ab.
Was zeigen die zwei Diagramme des Stechheberversuchs?
Diagramm 1 (oben): Anzahl der gefüllten cm-Skalenabschnitte in den Glasrohren. Das dünne Rohr (langsamere Reaktionsrichtung) startet niedrig und steigt; das dicke Rohr (schnellere Richtung) startet hoch und fällt. Beide Kurven nähern sich asymptotisch einem gemeinsamen Plateau – dem Gleichgewichtszustand.
Diagramm 2 (unten): Das transportierte Volumen pro Schritt. Das dicke Rohr transportiert anfangs viel, das dünne wenig. Im Gleichgewicht transportieren beide pro Schritt gleich viel – die Kurven treffen sich.
Welche Grenzen hat der Stechheberversuch als Modell für chemische Gleichgewichte?
Jedes Modell hat Grenzen. Beim Stechheberversuch sind das vor allem: Die Rohrdurchmesser sind fest – in echten Reaktionen können die Reaktionsgeschwindigkeiten durch Konzentration, Temperatur oder Katalysatoren verändert werden (siehe Prinzip von Le Chatelier). Außerdem ist der Stechheberversuch diskret (schrittweise), während chemische Reaktionen kontinuierlich ablaufen. Das Modell eignet sich gut zur Veranschaulichung des dynamischen Gleichgewichts, nicht aber zur quantitativen Beschreibung.
Lernkarten – Stechheberversuch
Klicke auf eine Karte, um die Antwort zu sehen.
Wofür stehen im Stechheberversuch: die Standzylinder, die Glasrohre und der Flüssigkeitstransport?
Standzylinder A/B → Edukt- und Produktseite · Glasrohre → Reaktionswege (Hin- / Rückreaktion) · Flüssigkeitstransport → Stoffumsatz pro Zeiteinheit
Warum führen Versuch 1 (Start: alles in A) und Versuch 2 (Start: alles in B) zum gleichen Gleichgewicht?
Der Gleichgewichtszustand hängt nur von den Bedingungen (Rohrdurchmesser = Geschwindigkeit) ab, nicht vom Startpunkt. Das gilt ebenso für chemische Gleichgewichte.
Erkläre: Im Gleichgewicht des Stechheberversuchs bewegen sich die Füllhöhen nicht mehr – und trotzdem ist das Gleichgewicht „dynamisch". Wie passt das zusammen?
Makroskopisch: Füllhöhen konstant. Mikroskopisch: Flüssigkeit fließt weiterhin in beide Richtungen, aber in gleich großen Portionen. → dynamisch = gleichzeitig aktiv in beide Richtungen.
Beschreibe die Form der Kurven im Diagramm „transportiertes Volumen gegen Reaktionsschritte".
Dickes Rohr: startet hoch, fällt exponentiell. Dünnes Rohr: startet niedrig, steigt. Beide nähern sich asymptotisch einem gemeinsamen Wert → Gleichgewichtszustand.
Im GG-Zustand transportiert das dünne Rohr pro Schritt 2 ml. Das dicke Rohr hat doppelten Durchmesser. Wie viel ml transportiert es pro Schritt und wie viel insgesamt in 10 Schritten?
Im GG gilt: Transport Hin = Transport Rück. Dickes Rohr transportiert ebenfalls 2 ml pro Schritt. In 10 Schritten: 10 · 2 ml = 20 ml in jede Richtung.
Weiter im Kapitel Gleichgewichtsreaktionen
← Schwefelsäure-Gleichgewicht → Merkmale eines chemischen Gleichgewichts
🔁 Verwandte Seiten: Umkehrbare Reaktionen · Prinzip von Le Chatelier · Massenwirkungsgesetz
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Du lernst die drei zentralen Merkmale eines chemischen Gleichgewichts kennen und wiederholst den Systembegriff (offen / geschlossen / abgeschlossen). Diese Grundlagen brauchst du für alle weiteren Themen rund um Gleichgewichtsreaktionen.
Grundlagen aus diesem Kapitel
Das dynamische Gleichgewicht hast du am Modell des Stechheberversuchs kennengelernt: → Modellexperiment Stechheberversuch · Den Systembegriff aus der Energetik: → Thermodynamische Systeme (Energetik)
2.4 Merkmale eines chemischen Gleichgewichts
⚑ Merksatz – Chemisches Gleichgewicht
- Im abgeschlossenen System stellt sich das Gleichgewicht von beiden Seiten her ein.
- Im Gleichgewicht (Endzustand) erfolgen gleich viele Hin- wie Rückreaktionen pro Zeiteinheit.
- Im Gleichgewicht liegen meist nicht gleich viele Anfangs- wie Endstoffe vor.
Wiederholung: Systemtypen in der Chemie
| Offenes System | Geschlossenes System | Abgeschlossenes System (= isoliertes System) |
|
|---|---|---|---|
| Austausch von … |
✔ Energie ✔ Teilchen |
✔ Energie | — |
| Kein Austausch von … | — | ✘ Teilchen |
✘ Energie ✘ Teilchen |
| Besonderheit |
Gesamtenergie konstant i. d. R. idealisiertes System |
||
| Beispiele |
„Kochtopf" Mensch |
„Dampfkochtopf" Reagenzglas mit Stopfen |
„Thermoskanne" Universum (idealisiert) |
ℹ Den Systembegriff aus der Perspektive der Thermodynamik findest du hier: Thermodynamische Systeme (Energetik)
Auf einen Blick – die wichtigsten Aussagen
Merkmal 1 – Startpunkt
Das Gleichgewicht stellt sich von beiden Seiten her ein – ob man mit Edukten, Produkten oder einem Gemisch startet, spielt keine Rolle.
Merkmal 2 – Dynamik
Im Gleichgewicht laufen Hin- und Rückreaktion mit gleicher Geschwindigkeit ab. Äußerlich: Stillstand. Innerlich: ständige Aktivität.
Merkmal 3 – Stoffmengen
Edukte und Produkte liegen im GG meist in ungleichen Mengen vor. Das Verhältnis beschreibt die Gleichgewichtskonstante Kc.
Voraussetzung
Ein stabiles Gleichgewicht kann sich nur in einem abgeschlossenen oder geschlossenen System einstellen – Teilchen dürfen nicht entweichen.
Häufige Fragen – Merkmale des chemischen Gleichgewichts
Was sind die drei wichtigsten Merkmale eines chemischen Gleichgewichts?
Ein chemisches Gleichgewicht ist durch drei Merkmale gekennzeichnet: (1) Es stellt sich von beiden Seiten ein – unabhängig vom Startpunkt. (2) Hin- und Rückreaktion laufen im Gleichgewicht gleich schnell ab (dynamisches Gleichgewicht). (3) Die Konzentrationen von Edukten und Produkten sind im Gleichgewicht konstant, aber i. d. R. verschieden.
Was bedeutet „das Gleichgewicht stellt sich von beiden Seiten ein"?
Ganz gleich, ob man mit reinen Edukten, reinen Produkten oder einem beliebigen Gemisch startet – das System strebt immer denselben Gleichgewichtszustand an (bei gleichen Bedingungen). Das zeigt der Stechheberversuch modellhaft: Versuch 1 (Start: alles in A) und Versuch 2 (Start: alles in B) enden im selben Endzustand.
Sind im Gleichgewicht immer gleich viele Edukte wie Produkte vorhanden?
Nein – das ist ein häufiges Missverständnis. Im Gleichgewicht sind die Konzentrationen konstant, aber nicht notwendigerweise gleich groß. Wie das Verhältnis aussieht, beschreibt die Gleichgewichtskonstante Kc. Liegt Kc ≫ 1, überwiegen die Produkte; liegt Kc ≪ 1, überwiegen die Edukte.
Warum braucht man ein abgeschlossenes (oder geschlossenes) System für ein Gleichgewicht?
Wenn Teilchen das System verlassen können (offenes System), kann sich kein stabiles Gleichgewicht einstellen – z. B. entweicht CO2 beim Erhitzen von CaCO3 im offenen Reagenzglas, und die Rückreaktion findet praktisch nicht statt. Im geschlossenen System (Stopfen drauf) bleibt das CO2 im System, die Rückreaktion läuft ab, und es stellt sich ein Gleichgewicht ein.
Was ist der Unterschied zwischen offenem, geschlossenem und abgeschlossenem System?
Offenes System: Austausch von Energie und Teilchen mit der Umgebung (z. B. Kochtopf ohne Deckel, lebender Organismus). Geschlossenes System: Nur Energieaustausch, keine Teilchen (z. B. Reagenzglas mit Stopfen, Dampfkochtopf). Abgeschlossenes System: Weder Energie- noch Teilchenaustausch (Thermoskanne, Universum – idealisiert). Alle drei Typen sind detailliert auf der Seite Thermodynamische Systeme (Energetik) beschrieben.
Lernkarten – Merkmale des chemischen Gleichgewichts
Klicke auf eine Karte, um die Antwort zu sehen.
Nenne die drei Merkmale eines chemischen Gleichgewichts.
① Stellt sich von beiden Seiten ein · ② Hin- = Rückreaktion pro Zeiteinheit (dynamisch) · ③ Meist ungleiche Mengen von Edukten und Produkten
Warum ist ein chemisches Gleichgewicht „dynamisch" und nicht „statisch"?
Weil Hin- und Rückreaktion weiterhin ablaufen – nur mit gleicher Geschwindigkeit. Makroskopisch: Konzentrationen konstant. Mikroskopisch: ständige Reaktionsaktivität.
Ordne zu: Kochtopf (offen) · Reagenzglas mit Stopfen · Thermoskanne → welcher Systemtyp?
Kochtopf ohne Deckel → offenes System · Reagenzglas mit Stopfen → geschlossenes System · Thermoskanne → abgeschlossenes System
Stimmt es, dass im GG immer [Edukt] = [Produkt] gilt? Begründe.
Nein. Im GG sind die Konzentrationen konstant, aber nicht notwendigerweise gleich. Das Verhältnis hängt von Kc ab: Kc ≫ 1 → Produkte überwiegen; Kc ≪ 1 → Edukte überwiegen.
Für A ⇌ B gilt Kc = 4. Im Gleichgewicht beträgt [A] = 0,5 mol/L. Berechne [B].
Kc = [B] / [A]
[B] = Kc · [A]
[B] = 4 · 0,5 mol/L
[B] = 2,0 mol/L
Weiter im Kapitel Gleichgewichtsreaktionen
← Stechheberversuch → Estergleichgewicht
🔁 Verwandte Seiten: Prinzip von Le Chatelier · Massenwirkungsgesetz · Thermodynamische Systeme (Energetik)
- Details
- Geschrieben von: Wolfram Hölzel
