Was du in diesem Kapitel lernst
Dieses Kapitel fasst die wichtigsten Grundlagen der 9. Klasse Chemie zusammen – von den Elementarteilchen über die Atommodelle, das Periodensystem und die chemischen Bindungstypen bis zu den zwischenmolekularen Kräften (ZMK). Die Seiten dienen als ergänzendes Angebot zum Unterricht und ermöglichen schnelles Wiederholen und Festigen. Modelle werden bewusst vereinfacht dargestellt (z. B. Kugelwolkenmodell).
Grundlagen aus der 8. Klasse
Den ersten Einstieg in den Atombau und das Dalton-Modell hast du bereits in der 8. Klasse kennengelernt: → Atombau und weitere Kapitel (Kl. 8)
Chemie – die wichtigsten Grundlagen
Die folgenden Seiten fassen die Grundlagen der 9. Klasse Chemie vereinfacht zusammen. Sie geben dir die Möglichkeit, die wichtigsten Inhalte schnell zu wiederholen und zu festigen. Diese Seiten sind ein zusätzliches Angebot zum Heftaufschrieb und erheben keinen Anspruch auf Vollständigkeit. Die vorgestellten Modelle sind bewusst vereinfacht – insbesondere das Kugelwolkenmodell (KWM).
An wen richtet sich diese Seite?
Diese Seite richtet sich vor allem an Schülerinnen und Schüler, die mit der Chemie Schwierigkeiten haben. Deshalb werden möglichst einfache Erklärungen vorgestellt und nach jeder kleinen Lerneinheit Wiederholungsschritte und Übungen eingebaut.
Kapitelübersicht – Vom Atombau bis ZMK
Kapitel 1
1. Elementarteilchen – Protonen, Elektronen, Neutronen
Aufbau des Atoms aus Protonen, Neutronen und Elektronen; Atommasse und Ordnungszahl.
⚠️ Joomla-Seite in Vorbereitung (Migration aus basischemie)
Kapitel 2
2. Atommodelle – von Demokrit bis Dalton
Historische Entwicklung der Atommodelle; Kugelmodell nach Dalton als erste quantitative Beschreibung.
Kapitel 3
3. Atomkern und Atomhülle – Rutherford-Modell
Rutherfords Streuversuch; Kern-Hülle-Modell; Aufbau des Atomkerns.
Kapitel 4
4. Schalenmodell der Elektronenhülle – Bohr
Energieniveaus und Schalen; Elektronenkonfiguration; Hauptquantenzahl.
Kapitel 5
5. Das Kugelwolkenmodell (KWM)
Orbitale und Feinstruktur der Elektronenhülle; s- und p-Orbitale.
Kapitel 6
6. Edelgasregel (Oktettregel)
Stabile Edelgaskonfiguration als Grundlage aller chemischen Bindungen.
Kapitel 7
7. Atombindung = Elektronenpaarbindung
Kapitel 8
8. Ionenbindung
- 8.1 Elektroneutralität
- 8.2 Bindungsart und Elektronegativität (in Vorbereitung)
- 8.3 Spaltung einer Atombindung (in Vorbereitung)
Kapitel 9
9. Zwischenmolekulare Kräfte (ZMK) und Hydratation
⚠️ Joomla-Seiten in Vorbereitung (Migration aus basischemie)
- 9.1 Dipol-Dipol-Wechselwirkungen
- 9.2 Van-der-Waals-Kräfte
- 9.3 Wasserstoffbrückenbindungen
- 9.4 Zusammenfassung ZMK
- 9.5 Hydration / Hydratation (Solvatation)
Auf einen Blick – die wichtigsten Aussagen
ATOMMODELLE
Die Modelle von Dalton → Rutherford → Bohr → KWM beschreiben den Atomaufbau mit zunehmender Genauigkeit. Jedes Modell hat seine Grenzen.
BINDUNGSTYPEN
Atombindung (gemeinsame Elektronenpaare zwischen Nichtmetallen) und Ionenbindung (Elektronenübertragung, Metall + Nichtmetall) sind die zwei zentralen Bindungstypen der Klasse 9.
EDELGASREGEL
Atome streben nach der stabilen Edelgaskonfiguration mit 8 Außenelektronen (Oktettregel). Diese Triebkraft erklärt alle Bindungstypen im Kapitel.
ZMK
Zwischenmolekulare Kräfte (Van-der-Waals, Dipol-Dipol, Wasserstoffbrücken) wirken zwischen Molekülen und bestimmen Siedepunkte und Löslichkeit von Stoffen.
Häufige Fragen – Atombau bis ZMK (Kl. 9)
Warum gibt es verschiedene Atommodelle?
Kein Atommodell ist „richtig" oder „falsch" – jedes beschreibt bestimmte Phänomene gut, hat aber auch Grenzen. Das Dalton-Modell erklärt chemische Reaktionen, versagt aber bei Spektren. Das Bohr-Modell erklärt Linienspektren, nicht aber die Feinstruktur. Das Kugelwolkenmodell (KWM) ist das modernste Schulmodell und beschreibt Aufenthaltswahrscheinlichkeiten von Elektronen in Orbitalen.
Was sind Elementarteilchen und welche gibt es?
Atome bestehen aus drei Elementarteilchen: Protonen (positiv geladen, im Kern), Neutronen (neutral, im Kern) und Elektronen (negativ geladen, in der Hülle). Die Ordnungszahl gibt die Protonenanzahl an und bestimmt die Stellung im PSE. Die Massenzahl ist die Summe aus Protonen und Neutronen.
Was ist der Unterschied zwischen Atombindung und Ionenbindung?
Bei der Atombindung teilen sich zwei Nichtmetallatome gemeinsame Elektronenpaare – beide Atome erreichen so die Edelgaskonfiguration. Bei der Ionenbindung überträgt ein Metallatom Elektronen auf ein Nichtmetallatom. Es entstehen positiv geladene Kationen und negativ geladene Anionen, die sich im Ionengitter anziehen. Die Elektronegativitätsdifferenz entscheidet: groß → Ionenbindung, klein → Atombindung.
Was besagt die Edelgasregel (Oktettregel)?
Atome streben danach, eine vollständig besetzte Außenschale mit 8 Elektronen zu besitzen – wie die stabilen Edelgase (Ausnahme: Helium mit 2 Elektronen). Dieses Bestreben nach der stabilen Edelgaskonfiguration ist die Triebkraft hinter Atombindungen, Ionenbindungen und der Bildung von Ionen.
Welche zwischenmolekularen Kräfte (ZMK) gibt es und was bewirken sie?
Es gibt drei Typen von ZMK: Van-der-Waals-Kräfte wirken zwischen allen Molekülen (temporäre Dipole); Dipol-Dipol-Kräfte zwischen permanenten Dipolen; Wasserstoffbrücken zwischen Molekülen mit O–H-, N–H- oder F–H-Gruppen. Stärkere ZMK bedeuten höhere Siedepunkte und bessere Mischbarkeit mit polaren Lösungsmitteln wie Wasser.
Lernkarten – Atombau bis ZMK
Klicke auf eine Karte, um die Antwort zu sehen.
Welche drei Elementarteilchen bauen ein Atom auf? Wo befinden sie sich?
Protonen (+, im Kern) · Neutronen (0, im Kern) · Elektronen (−, in der Hülle). Ordnungszahl = Protonenanzahl.
Was beschreibt das Kugelwolkenmodell (KWM) im Unterschied zum Bohr-Modell?
Statt fester Bahnen (Bohr) gibt das KWM Aufenthaltswahrscheinlichkeiten von Elektronen in räumlichen Orbitalen (s, p, d) an.
Was besagt die Edelgasregel? Nenne ein Beispiel.
Atome streben nach 8 Außenelektronen (Oktettregel). Beispiel: Chlor (7 Außenelektronen) reagiert mit Natrium (1 Außenelektron) → NaCl; beide erreichen Edelgaskonfiguration.
Nenne die drei Typen zwischenmolekularer Kräfte in aufsteigender Stärke.
1. Van-der-Waals-Kräfte (temporäre Dipole, schwächste) · 2. Dipol-Dipol-Kräfte (permanente Dipole) · 3. Wasserstoffbrücken (O–H, N–H, F–H; stärkste ZMK)
Schwefel hat die Ordnungszahl 16. Wie viele Protonen, Neutronen (Massenzahl 32) und Elektronen hat ein neutrales Schwefelatom? Auf welche Schalen verteilen sich die Elektronen (Bohr-Modell)?
Protonen: 16 · Neutronen: 32 − 16 = 16 ·
Elektronen: 16
Schalenbesetzung: K(2) L(8) M(6) →
6 Außenelektronen → braucht 2 weitere → Edelgasregel erfüllt bei S²⁻
Weiter in Klasse 9
→ Redoxreaktionen (Kl. 9) → Säure-Base-Reaktionen (Kl. 9)
🔁 Grundlagen: Atombau (Kl. 8)
- Details
- Geschrieben von: Wolfram Hölzel
Im folgenden befindet sich hier der Tafelanschrieb für Klassenstufe 8 oder 9 mit dem Thema PSE - Atombau - Molekül-/Ionenbindung und Zwischenmolekulare Bindungen
Begleitet wird dieses Kapitel durch eine interaktive (technische vielleicht etwas veraltete) Seiten. In den Kapiteln wird auf konkrete Seiten verlinkt, diese können aber auch für sich gesehen werden.
Einleitung und Erklärung der interaktiven Seite
1 Das Periodensystem der Elemente (Teil I)
Ein Periodensystem kann von dieser Seite heruntergeladen werden: Beispiele von Periodensystemen (PSE)
Ordnungsprinzipien
Ursprünglich nach steigender Atommasse geordnet, dann nach der Ordnungszahl und nach periodisch wiederkehrenden Ähnlichkeiten in den Eigenschaften.
Das Kurzperiodensystem enthält nur die Hauptgruppenelemente.
Die Hauptgruppen des PSE
I. Hauptgruppe: Alkalimetalle
II. Hauptgruppe: Erdalkalimetalle
III. Hauptgruppe: Borgruppe
IV. Hauptgruppe: Kohlenstoffgruppe
V. Hauptgruppe: Stickstoffgruppe
VI. Hauptgruppe: Chalkogene (Erzbildner)
VII. Hauptgruppe: Halogene (Salzbildner)
VIII. Hauptgruppe: Edelgase
Aussage
- Anordnung nach steigender Atommasse (Ausnahmen: K – Ar; Co – Ni; Te – J; Th – Pa).
- In jeder Hauptgruppe stehen verwandte Elemente.
- Metallischer Charakter nimmt nach links unten zu!
- Nichtmetallischer Charakter nimmt nach rechts oben zu!
- Halbmetalle stehen diagonal dazwischen.
Bedeutung
- Voraussage damals unbekannter Elemente (z. B. Germanium).
- Ablesen von physikalischen und chemischen Eigenschaften aus der Stellung im PSE.
- Details
- Geschrieben von: Wolfram Hölzel
2 Atommodelle:
Wiederholung aus der 8. Klasse:
2.1 Demokrit:
Atome sind die kleinsten, unteilbare Einheiten
2.2 Dalton: Kugelteilchenmodell
- Atome = unveränderlich, unsichtbar und unzerstörbar
- Atome eines Elementes sind untereinander gleich
- Sie unterscheiden sich von den Atomen anderer Elemente in ihrer Masse
- Bei chemischen Reaktionen werden Atome nicht verändert, sondern miteinander verknüpft oder getrennt.
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Atome bestehen aus einem winzigen, positiv geladenen Atomkern und einer negativ geladenen Elektronenhülle. Du lernst die drei Elementarteilchen (Proton, Neutron, Elektron) kennen, verstehst elektrische Anziehungs- und Abstoßungskräfte im Atom und lernst die chemische Schreibweise mit Nukleonenzahl, Kernladungszahl und Massenzahl.
Grundlagen aus der 8. Klasse
Das erste Atommodell hast du bereits in der 8. Klasse kennengelernt: → Atommodell nach Dalton – Kugelteilchenmodell
Elektrische Anziehungskräfte im Atom
Sehr vereinfacht können wir sagen, dass jede Anziehungskraft der Chemie auf der Anziehung zwischen positiver und negativer Ladung beruht.
Kurz: Plus + Minus ziehen sich an; gleiche Ladungen stoßen sich ab.
⚡ Anziehung und Abstoßung – ausprobieren!
Aufbau des Atoms: Atomkern und Elektronenhülle
Atome bestehen aus:
- einem sehr kleinen, positiv geladenen Kern
- einer negativen, kugelförmigen Elektronenhülle
- Elektronen, die sich mit hoher Geschwindigkeit um den Kern bewegen
Ein Atommodell, das zwischen Atomkern und Elektronenhülle unterscheidet, wird als Kern-Hülle-Modell bezeichnet.
Vereinfachtes Kern-Hülle-Modell eines Atoms (nicht maßstabsgerecht)
Größenverhältnis: Atomkern und Atomhülle
⚠️ Wichtig: Der Durchmesser der Atomhülle ist etwa 10 000-mal größer als der Durchmesser des Atomkerns. Die Hülle ist kein fester Bereich – es ist nur der Bereich, in dem sich die Elektronen aufhalten.
Wenn der Atomkern so groß wie eine Kirsche wäre, hätte das gesamte Atom einen Durchmesser von etwa einem Fußballfeld.
2.3.1 Der Atomkern – Elementarteilchen und Schreibweise
Die Teilchen, aus denen ein Atom besteht, bezeichnet man als Elementarteilchen: Protonen, Neutronen und Elektronen.
↑ Zum Vergrößern klicken
✕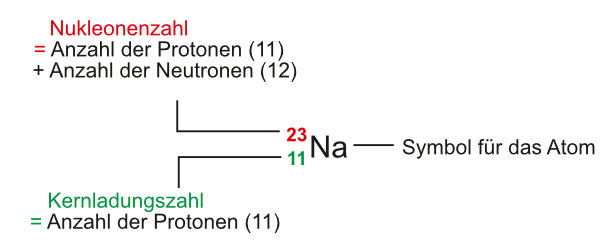
Aus dem Tafelbild ergeben sich folgende Definitionen:
- Der Atomkern ist aus Protonen und Neutronen aufgebaut.
- Die Protonenzahl stimmt mit der Ordnungszahl eines Elements und der
Kernladungszahl überein.
Beispiel: Fluor = ₉F: 9 Protonen → Ordnungszahl = Kernladungszahl = 9, Elektronenanzahl = 9. - Nukleonenzahl = Anzahl der Protonen + Anzahl der Neutronen im Atomkern.
Beispiel: ¹⁹F: Nukleonenzahl = 19 → 9 Protonen und 10 Neutronen. - Massenzahl: Die Atommasse ist angenähert die Summe der Protonen- und Neutronenmasse. Die Masse der Elektronen ist außerordentlich klein.
Übungsaufgabe: Elementarteilchen
Kannst du die Tabelle selbst ausfüllen? Klicke dann auf „Lösung anzeigen".
↑ Zum Vergrößern klicken
✕
Auf einen Blick – die wichtigsten Aussagen
Kern-Hülle-Modell
Atome bestehen aus einem winzigen, positiv geladenen Atomkern und einer negativ geladenen Elektronenhülle.
Elementarteilchen
Im Kern: Protonen (1 u, +1) und Neutronen (1 u, 0). In der Hülle: Elektronen (≈0 u, −1).
Nukleonenzahl
Nukleonenzahl = Anzahl Protonen + Anzahl Neutronen = Massenzahl. Die Kernladungszahl = Protonenzahl = Ordnungszahl.
Elektrische Kräfte
Ungleiche Ladungen ziehen sich an, gleiche stoßen sich ab. Protonen (+) und Elektronen (−) halten das Atom zusammen.
Häufige Fragen – Kern-Hülle-Modell und Elementarteilchen
Was sind Elementarteilchen und welche gibt es?
Elementarteilchen sind die Bausteine eines Atoms. Es gibt drei: Protonen (Masse 1 u, Ladung +1, im Kern), Neutronen (Masse 1 u, Ladung 0, im Kern) und Elektronen (Masse ≈ 0 u, Ladung −1, in der Elektronenhülle). Protonen und Neutronen heißen zusammen auch Nukleonen.
Was ist der Unterschied zwischen Kernladungszahl, Ordnungszahl und Massenzahl?
Die Kernladungszahl = Anzahl der Protonen im Kern = Ordnungszahl des Elements im Periodensystem. Die Massenzahl (= Nukleonenzahl) = Anzahl Protonen + Anzahl Neutronen. Beim Aluminium ²⁷₁₃Al: Kernladungszahl = Ordnungszahl = 13 (Protonen), Massenzahl = 27 (13 Protonen + 14 Neutronen).
Warum ist der Atomkern so viel kleiner als das Atom?
Der Durchmesser der Atomhülle beträgt etwa 10 000-mal den Durchmesser des Atomkerns. Der Kern enthält fast die gesamte Masse des Atoms, aber fast kein Volumen. Die Hülle ist kein festes Objekt – sie ist lediglich der Bereich, in dem sich die Elektronen aufhalten. Der übrige Teil des Atoms ist „leer".
Warum brechen nicht alle Protonen im Kern auseinander?
Auf sehr kurze Abstände wirkt die sogenannte starke Kernkraft (Kernbindungskraft), die stärker ist als die elektrische Abstoßung zwischen den positiv geladenen Protonen. Neutronen helfen dabei, diese Kraft zu vermitteln und den Kern zusammenzuhalten. Die starke Kernkraft ist Thema der Physik – in der Chemie arbeiten wir vereinfachend mit dem Kern-Hülle-Modell.
Welche Weiterentwicklung des Kern-Hülle-Modells gibt es?
Rutherford beschrieb erstmals den Aufbau aus Kern und Hülle. Niels Bohr erweiterte dieses Modell: Elektronen bewegen sich auf bestimmten Bahnen (Energiestufen, Schalen) um den Kern – man spricht vom Bohrschen Schalenmodell. Das modernste Modell für die Schule ist das Kugelwolkenmodell (KWM), das die Aufenthaltswahrscheinlichkeit der Elektronen beschreibt.
Lernkarten – Kern-Hülle-Modell und Elementarteilchen
Klicke auf eine Karte, um die Antwort zu sehen.
Aus welchen drei Elementarteilchen besteht ein Atom? Nenne Symbol, Masse und Ladung.
Proton (p⁺, 1 u, +1) – im Kern
Neutron (n, 1 u, 0) – im Kern
Elektron (e⁻, ≈0 u, −1) – Elektronenhülle
Was ist die Kernladungszahl und womit stimmt sie überein?
Die Kernladungszahl = Anzahl der Protonen im Kern. Sie stimmt mit der Ordnungszahl im PSE und der Elektronenanzahl im neutralen Atom überein.
Was passiert bei: +/−, +/+, −/−?
+ und − → Anziehung (ungleiche Ladungen)
+ und + → Abstoßung (gleiche Ladungen)
− und − → Abstoßung (gleiche Ladungen)
Was bedeuten die Zahlen in der Schreibweise ²⁷₁₃Al?
27 = Massenzahl (Nukleonenzahl) = Protonen + Neutronen
13 = Kernladungszahl = Ordnungszahl = Protonenzahl
Neutronen = 27 − 13 = 14
Rechenaufgabe: ¹⁹₉F – wie viele Protonen, Neutronen und Elektronen?
Protonen = Kernladungszahl = 9
Neutronen = 19 − 9 = 10
Elektronen (neutral) = Protonenzahl = 9
Weiter im Kapitel – Atombau bis ZMKs
← 2.2 Atommodelle: Demokrit und Dalton 2.4 Bohrsches Schalenmodell →
🔁 Grundlagen (Kl. 8): Atommodell nach Dalton – Kugelteilchenmodell
⏩ Weiterführend: 2.5 Das Kugelwolkenmodell (KWM) · PSE Teil I
- Details
- Geschrieben von: Wolfram Hölzel
Was du auf dieser Seite lernst
Niels Bohr erweiterte das Rutherford-Modell: Elektronen bewegen sich nicht beliebig, sondern nur auf bestimmten Bahnen (Energiestufen, Schalen) um den Kern. Du lernst Bohrs zwei Postulate kennen, verstehst die 2n²-Formel für die maximale Elektronenzahl pro Schale und erfährst, wie das Modell Lichtabsorption und -emission erklärt.
Grundlagen aus der 9. Klasse
Voraussetzung ist das Kern-Hülle-Modell von Rutherford: → 2.3 Rutherford: Kern-Hülle-Modell und Elementarteilchen
Niels Bohrs Schalenmodell
Niels Bohrs Modell beschreibt das Atom aus einem positiv geladenen Kern und negativ geladenen Elektronen, die auf ganz bestimmten konzentrischen Bahnen den Kern umkreisen (ähnlich wie die Planeten die Sonne umkreisen).
↑ Zum Vergrößern klicken – Zoom-Overlay aktiv
▶ 1. Postulat – Niels Bohr, 1913
Die Elektronen bewegen sich nur auf ganz bestimmten, genau definierten Bahnen (= Energiestufen, Energieschalen, Schalen) um den Atomkern.
Diese Bahnen heißen Schalen und werden von innen nach außen mit K, L, M, N, … bezeichnet. Je weiter die Schale vom Kern entfernt ist, desto höher ist die Energie der Elektronen auf ihr.
Energieniveaus und Elektronenschalen
Die Begriffe Schale und Energiestufe beschreiben dasselbe: den Bereich, in dem sich Elektronen mit einer bestimmten Energie bewegen. Elektronen auf der M-Schale besitzen eine höhere Energie als solche auf der L-Schale, da sie weiter vom Kern entfernt sind.
👆 Tipp: Die interaktive Übersicht direkt darunter zeigt die Schalenbesetzung für alle Elemente der 1.–3. Periode – hover einfach über ein Element im PSE!
2. Postulat – Maximale Elektronenzahl pro Schale
▶ 2. Postulat – Niels Bohr, 1913
Jede Schale kann maximal 2 · n² Elektronen aufnehmen.
n = Schalennummer (n = 1, 2, 3, 4, …)
| Schale | n | 2 · n² | Max. Elektronen |
|---|---|---|---|
| K | 1 | 2 · 1² = 2 | 2 |
| L | 2 | 2 · 2² = 8 | 8 |
| M | 3 | 2 · 3² = 18 | 18 |
| N | 4 | 2 · 4² = 32 | 32 |
Beispiel 1
Wie viele Elektronen kann die 1. Schale maximal aufnehmen?
Lösung 1
1. Schale → n = 1 | 2·n² = 2·1·1 = 2
Beispiel 2
Wie viele Elektronen kann die N-Schale maximal aufnehmen?
Lösung 2
N-Schale ist die 4. Schale → n = 4 | 2·n² = 2·4² = 32
⚠️ Wichtig: Das bedeutet nur, dass so viele Elektronen maximal in diese Schale passen. Natürlich können jederzeit weniger Elektronen vorhanden sein!
🧠 Verständnisüberprüfung
Elektronen welcher Schale besitzen eine höhere Energie – die der L-Schale oder die der M-Schale?
▶ Lösung anzeigen
Die Elektronen der M-Schale, da diese weiter vom Kern entfernt sind und damit eine höhere potenzielle Energie besitzen.
Quantentheorie: Absorption und Emission von Licht
Quantentheorie (Planck, Einstein):
Die kleinsten nicht mehr teilbaren Energiebeträge heißen Quanten.
Durch Energiezufuhr kann ein Elektron vom Grundzustand (= energieärmster Zustand) in einen angeregten Zustand gebracht werden.
Da das Elektron zwischen den Schalen nicht existieren kann, nimmt es nur solche Energiequanten auf, die der Energiedifferenz zwischen zwei Schalen entsprechen – zum Beispiel durch Absorption von Licht.
Der angeregte Zustand ist sehr instabil: Das Elektron springt nach ca. 10⁻⁸ s wieder in den Grundzustand zurück und gibt dabei die Anregungsenergie als Licht (Emission) wieder ab.
Absorption: Elektron springt in höhere Schale · Emission: Rücksprung mit Lichtabgabe (≈ 10⁻⁸ s)
Übungsaufgaben
Aufgabe 1: Aus welchen Elementarteilchen besteht der Atomkern und wie ist er geladen?
Der Atomkern besteht aus Protonen und Neutronen. Er ist positiv geladen, da Protonen die Ladung +1 tragen und Neutronen neutral sind. → Wiederholung: Elementarteilchen
Aufgabe 2: Wie verteilen sich die Elektronen laut Niels Bohr?
Die Elektronen bewegen sich auf ganz bestimmten Bahnen (Schalen / Energiestufen) um den Kern. Die innerste Schale (K) wird zuerst besetzt. Erst wenn sie voll ist, werden äußere Schalen gefüllt.
Aufgabe 3: Wie lautet die Formel für die maximale Elektronenzahl pro Schale?
Maximale Elektronenzahl pro Schale = 2 · n², wobei n die Schalennummer ist. Beispiele: K (n=1) → 2, L (n=2) → 8, M (n=3) → 18.
Aufgabe 4: Auf welche Schale verteilt sich ein Elektron als erstes?
Auf die K-Schale (innerste, energieärmste Schale). Elektronen besetzen immer zuerst die energieärmste verfügbare Schale.
Aufgabe 5: Wie viele Elektronen kann die L-Schale maximal besitzen?
L-Schale → n = 2 → 2 · n² = 2 · 4 = 8 Elektronen.
Aufgabe 6: Woraus besteht der Hauptteil (fast der ganze Raum) eines Atoms?
Fast der gesamte Raum eines Atoms besteht aus leerem Raum. Der winzige Kern enthält fast die gesamte Masse, nimmt aber nur einen verschwindend kleinen Teil des Atomvolumens ein. → Größenverhältnis Kern/Hülle
Auf einen Blick – die wichtigsten Aussagen
1. Postulat
Elektronen bewegen sich nur auf genau definierten Bahnen (Energiestufen / Schalen: K, L, M, N …) um den Kern.
2. Postulat
Maximale Elektronenzahl pro Schale: 2 · n² (K = 2, L = 8, M = 18, N = 32).
Energiestufen
Je weiter die Schale vom Kern, desto höher die Energie der Elektronen. M-Elektronen haben mehr Energie als L-Elektronen.
Absorption / Emission
Absorption: Elektron springt in höhere Schale. Emission: Rücksprung → Licht wird abgegeben (≈ 10⁻⁸ s).
Häufige Fragen – Bohrsches Schalenmodell
Was sind die Postulate von Niels Bohr?
1. Postulat: Elektronen bewegen sich nur auf bestimmten Bahnen (Schalen/Energiestufen) um den Kern – keine anderen Positionen möglich. 2. Postulat: Jede Schale fasst maximal 2·n² Elektronen (n = Schalennummer). Innerste Schale wird zuerst besetzt.
Was ist der Unterschied zwischen Schale und Energiestufe?
Beides bezeichnet dasselbe: den Bereich, in dem sich Elektronen mit einer bestimmten Energie aufhalten. „Schale" betont den räumlichen Aspekt (kreisförmige Bahn), „Energiestufe" betont den energetischen Aspekt. In der Chemie werden beide Begriffe synonym verwendet. Die Schalen sind von innen nach außen K, L, M, N … benannt.
Wie viele Elektronen passen maximal in die K-, L- und M-Schale?
K-Schale (n=1): 2·1² = 2 Elektronen. L-Schale (n=2): 2·2² = 8 Elektronen. M-Schale (n=3): 2·3² = 18 Elektronen. Wichtig: Das sind Maximalwerte – es können immer weniger Elektronen vorhanden sein.
Wie erklärt das Bohr-Modell die Entstehung von Licht?
Elektronen können Lichtenergie (Photonen) absorbieren und dadurch in eine höhere Schale springen (angeregter Zustand). Da dieser Zustand instabil ist, springen sie nach ca. 10⁻⁸ s zurück in den Grundzustand und geben dabei ein Lichtquant (Photon) ab – das ist die Emission von Licht. Die Farbe des emittierten Lichts hängt von der Energiedifferenz zwischen den Schalen ab.
Wo liegen die Grenzen des Bohrschen Schalenmodells?
Das Bohr-Modell funktioniert nur exakt für Wasserstoff (1 Elektron). Bei mehreren Elektronen liefert es nur Näherungen. Außerdem widerspricht die Vorstellung einer genau definierten Kreisbahn der Quantenmechanik (Heisenbergsche Unschärferelation). Das modernere Kugelwolkenmodell (KWM) löst diese Probleme durch Aufenthaltswahrscheinlichkeiten statt fester Bahnen.
Lernkarten – Bohrsches Schalenmodell
Klicke auf eine Karte, um die Antwort zu sehen.
Nenne Bohrs 1. Postulat in einem Satz.
Elektronen bewegen sich nur auf ganz bestimmten, genau definierten Bahnen (= Energiestufen / Schalen) um den Atomkern.
Wie lautet die Formel für die max. Elektronen pro Schale? Was bedeutet n?
Max. Elektronen = 2 · n²
n = Schalennummer (K=1, L=2, M=3, N=4)
Was passiert bei der Absorption von Licht?
Das Elektron nimmt ein Lichtquant (Photon) auf und springt von einer niedrigeren in eine höhere Schale (Grundzustand → angeregter Zustand).
Warum senden Atome Licht aus? Was ist Emission?
Der angeregte Zustand ist instabil: Das Elektron springt zurück in den Grundzustand und gibt die Energiedifferenz als Licht (Photon) ab – das ist Emission.
Rechenaufgabe: Wie viele Elektronen passen maximal in die M-Schale?
M-Schale → n = 3
2 · n² = 2 · 3² = 2 · 9 = 18 Elektronen
Weiter im Kapitel – Atombau bis ZMKs
← 2.3 Rutherford: Kern-Hülle-Modell 2.5 Kugelwolkenmodell →
⏩ Weiterführend: 2.6 PSE und die Atommodelle · 2.5 Kugelwolkenmodell (KWM)
- Details
- Geschrieben von: Wolfram Hölzel