Was du auf dieser Seite lernst
Ammoniak ist ein Gas, das sich außergewöhnlich gut in Wasser löst – das zeigt der Springbrunnenversuch eindrucksvoll. Du lernst, wie Ammoniak mit Wasser nach der Brønsted-Theorie reagiert (Protolyse), warum dabei eine basische Lösung entsteht, und verstehst im Exkurs, warum Sprudelwasser sauer ist und wie man daraus den pH-Wert berechnet.
Grundlagen aus der 9. Klasse
Die Grundlagen zur Brønsted-Theorie (Protonendonator / Protonenakzeptor) hast du bereits in der 9. Klasse kennengelernt: → Brønsted-Theorie (Kl. 9) · → Säure-Base-Reaktionen (Kl. 9)
3.2 Ammoniak-Gas + Wasser (Springbrunnen 2)
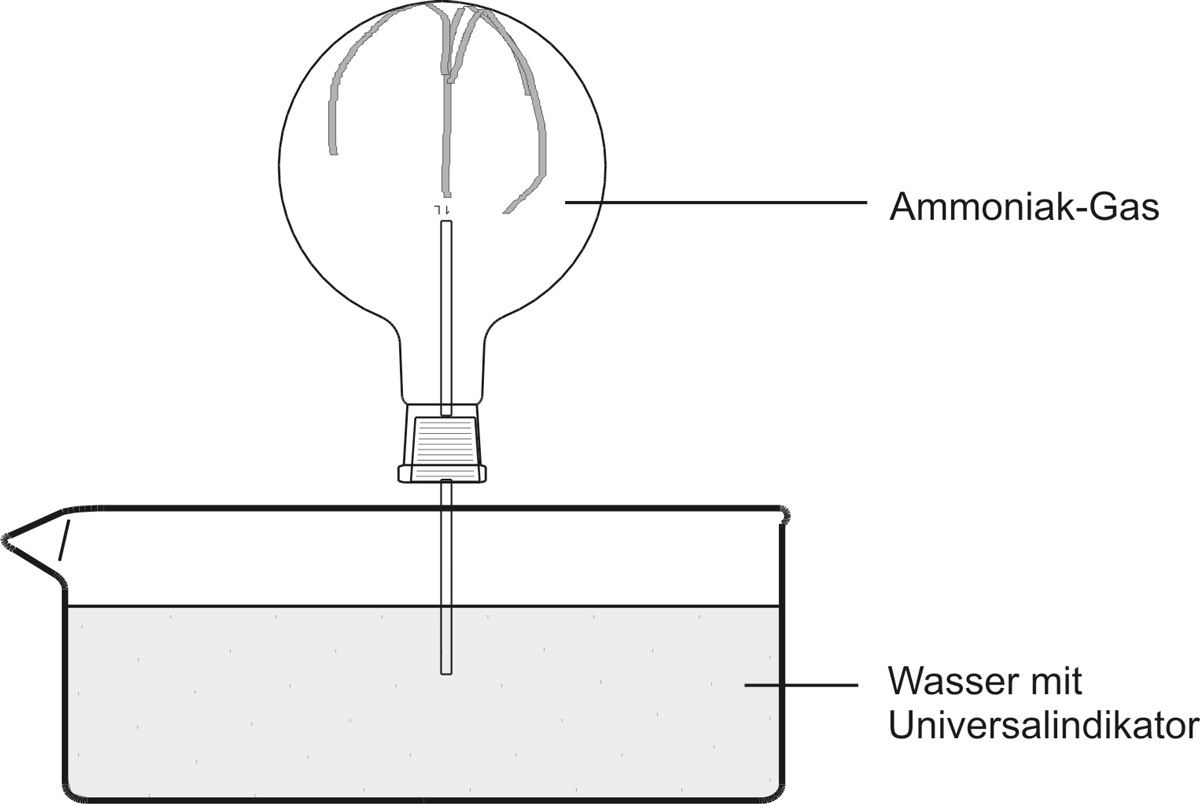
a) Versuch
↑ Zum Vergrößern klicken
✕
b) Beobachtung
Das Wasser „schießt" bergauf in den Rundkolben. Die Indikatorfarbe schlägt nach blau um. Die blaue wässrige Lösung riecht nach Ammoniak.
c) Erklärung
Ammoniak-Gas löst sich sehr gut in Wasser und reagiert teilweise mit Wasser. Im Kolben entsteht durch das Lösen des Gases ein starker Unterdruck. Die entstehenden Hydroxid-Ionen (OH⁻) färben den Universalindikator blau.
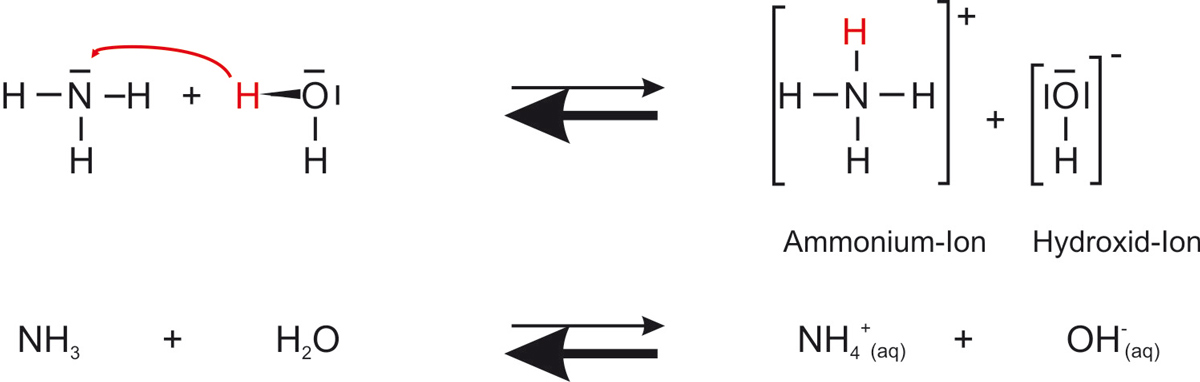
d) Reaktionsgleichung (mit Strukturformeln und Summenformeln)
Versuche die Gleichung erst selbst zu formulieren!
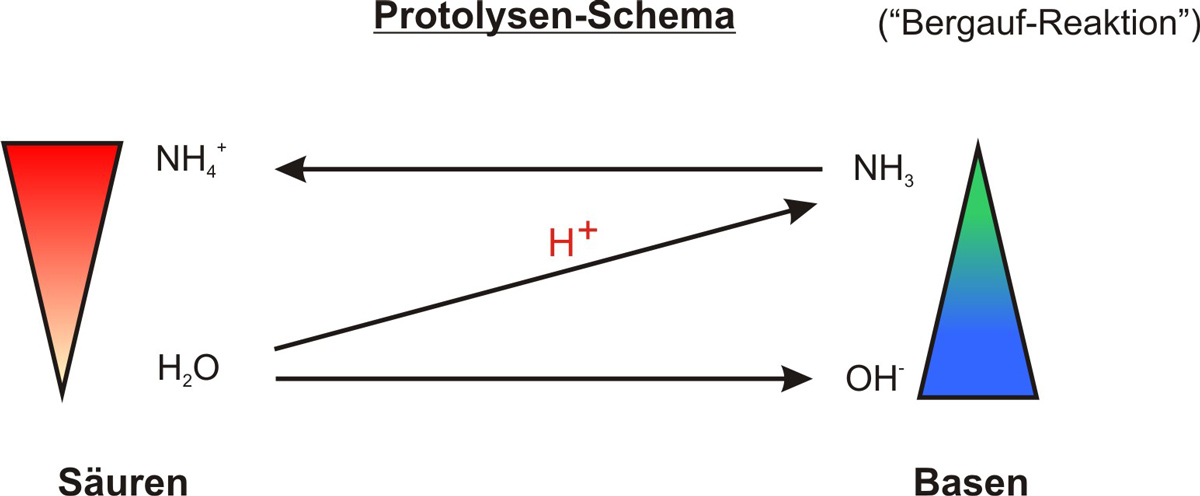
Formuliere nun das Protolyseschema:
Exkurs: Was macht den Sprudel sauer?
Kohlenstoffdioxid reagiert beim Lösen in Wasser im Gleichgewicht zu Kohlensäure:
CO₂ (g) + H₂O (l) ⇌ „H₂CO₃" (aq) – instabil (→ Erlenmeyer-Regel: zwei OH-Gruppen am selben C-Atom sind nicht beständig)
1. Protolysestufe: H₂CO₃ (aq) + H₂O (l) ⇌ HCO₃⁻ (aq) + H₃O⁺ (aq)
2. Protolysestufe: HCO₃⁻ (aq) + H₂O (l) ⇌ CO₃²⁻ (aq) + H₃O⁺ (aq)
Nachweis der H₃O⁺-Ionen durch:
- Geschmack (sauer)
- pH-Papier
- pH-Meter
Messwert: pH(Sprudel) = 5,1
Berechnung der Oxoniumionen-Konzentration:
pH = −lg c(H₃O⁺)
c(H₃O⁺) = 10−pH = 10−5,1 ≈ 7,9 · 10−6 mol/L
Auf einen Blick – die wichtigsten Aussagen
Springbrunneneffekt
NH₃ löst sich so gut in Wasser, dass im Kolben ein starker Unterdruck entsteht – das Wasser „schießt" nach oben in den Rundkolben.
Protolyse (Brønsted)
NH₃ + H₂O ⇌ NH₄⁺ + OH⁻. NH₃ ist Protonenakzeptor (Base), H₂O ist Protonendonator (Säure). Lösung basisch (pH > 7).
Erlenmeyer-Regel
H₂CO₃ ist instabil – zwei OH-Gruppen am selben C-Atom sind nicht beständig. H₂CO₃ zerfällt sofort in CO₂ und H₂O.
pH-Rechnung
pH = −lg c(H₃O⁺) · c(H₃O⁺) = 10−pH
Sprudel: pH 5,1 → c(H₃O⁺) ≈ 7,9 · 10−6 mol/L
Häufige Fragen – Ammoniak und Wasser
Warum steigt beim Springbrunnenversuch das Wasser von selbst auf?
Ammoniak löst sich außergewöhnlich gut in Wasser (ca. 700 Liter NH₃ in 1 Liter Wasser bei Raumtemperatur). Sobald Wasser mit dem Ammoniak-Gas in Berührung kommt, löst sich das Gas nahezu vollständig. Der Gasdruck im Kolben fällt schlagartig ab – es entsteht ein starker Unterdruck. Der Atmosphärendruck drückt daraufhin das Wasser durch die Glasspitze nach oben in den Kolben.
Ist NH₃ in Wasser eine Säure oder eine Base?
Nach Brønsted ist NH₃ eine Base: Es nimmt ein Proton (H⁺) vom Wasser auf und bildet das Ammoniumion NH₄⁺. Gleichzeitig gibt Wasser ein Proton ab und wird zur konjugierten Base OH⁻. Die Reaktion verläuft als Gleichgewicht:
NH₃ (aq) + H₂O (l) ⇌ NH₄⁺ (aq) + OH⁻ (aq)
Da OH⁻-Ionen entstehen, ist die Lösung basisch (pH > 7), was der Universalindikator durch Blaufärbung anzeigt.
Was bedeutet „konjugiertes Säure-Base-Paar"?
Ein konjugiertes Säure-Base-Paar unterscheidet sich nur um ein Proton H⁺. Bei der Ammoniak-Protolyse gibt es zwei solche Paare:
- NH₄⁺ / NH₃ – NH₄⁺ ist die Säure, NH₃ die konjugierte Base
- H₂O / OH⁻ – H₂O ist die Säure, OH⁻ die konjugierte Base
Das Protolyseschema stellt diese Paare mit Pfeilen dar und zeigt, in welche Richtung das Proton wandert. Mehr dazu auf der Seite → Brønsted-Theorie.
Was ist die Erlenmeyer-Regel und wozu braucht man sie?
Die Erlenmeyer-Regel besagt: Verbindungen, bei denen zwei Hydroxyl-Gruppen (OH) an demselben Kohlenstoffatom gebunden sind, sind instabil und wandeln sich spontan um. Kohlensäure H₂CO₃ hätte formal zwei OH-Gruppen am gleichen C-Atom – sie ist daher so instabil, dass sie sofort in CO₂ und H₂O zerfällt. Diese Regel erklärt, warum im Sprudelwasser kein stabiles H₂CO₃ vorliegt, sondern CO₂ im Gleichgewicht mit Wasser steht und dabei H₃O⁺-Ionen entstehen.
Wie berechnet man aus dem pH-Wert die Oxoniumionen-Konzentration?
Formel: pH = −lg c(H₃O⁺), umgestellt: c(H₃O⁺) = 10−pH
Beispiel Sprudel mit pH = 5,1:
c(H₃O⁺) = 10−5,1 ≈ 7,9 · 10−6 mol/L
Zum Vergleich: Reines Wasser hat c(H₃O⁺) = 10−7 mol/L (pH = 7). Weitere Berechnungen findest du auf der Seite → pH-Wert berechnen.
Lernkarten – Ammoniak und Wasser
Klicke auf eine Karte, um die Antwort zu sehen.
Warum entsteht beim Springbrunnenversuch ein Unterdruck im Kolben?
NH₃ löst sich extrem gut in Wasser → Gas verschwindet aus der Gasphase → Druck sinkt → Unterdruck → Atmosphärendruck drückt Wasser nach oben.
Formuliere die vollständige Protolysegleichung von NH₃ mit Wasser.
NH₃ (aq) + H₂O (l) ⇌ NH₄⁺ (aq) + OH⁻ (aq)
NH₃ = Base (Protonenakzeptor)
H₂O = Säure (Protonendonator)
Nenne die beiden konjugierten Säure-Base-Paare bei der Ammoniak-Protolyse.
Paar 1: NH₄⁺ (Säure) / NH₃ (Base)
Paar 2: H₂O (Säure) / OH⁻ (Base)
Warum ist Sprudelwasser sauer, obwohl H₂CO₃ instabil ist?
CO₂ reagiert im Gleichgewicht mit H₂O. Auch ohne stabiles H₂CO₃ entstehen durch Protolyse H₃O⁺-Ionen (Erlenmeyer-Regel) → saure Lösung (pH ≈ 5,1).
Berechne: Ein Sprudel hat pH = 4,5. Wie groß ist c(H₃O⁺)?
c(H₃O⁺) = 10−pH = 10−4,5 ≈ 3,2 · 10−5 mol/L
Weiter im Kapitel Säure-Base-Reaktionen
← 3 Protolyse-Reaktionen (Übersicht) → 3.3 Neutralisation
🔁 Grundlagen (Kl. 9): Säure-Base-Reaktionen (Kl. 9) · Brønsted-Theorie (Kl. 9) · Neutralisation (Kl. 9)
📈 Vertiefung: pH-Wert berechnen · pKB-Wert (Basestärke) · Pufferlösung