Was du auf dieser Seite lernst
Auf dieser Seite erweiterst du dein Verständnis des Satzes von Hess anhand weiterer Beispiele nach Atkins: Standardbildungsenthalpie von Methan (vollständig), Reduktion von CuO mit Zn sowie die indirekte Berechnung der CO-Bildungsenthalpie über einen Kreisprozess.
8.6 Satz von Hess – Teil II
Zunächst noch ein weiteres Beispiel nach dem Weg von „Atkins". Im Anschluss werden auch Überlegungen aufgezeigt, wie man den Satz von Hess noch anwenden kann.
Beispiel 1: Standardbildungsenthalpie von Methan
Gesucht: C(s) + 2 H₂(g) → CH₄(g) ΔH = ?
Leicht zu bestimmen: Verbrennungsenthalpien:
a) CH₄(g) + 2 O₂(g) → CO₂(g) + 2 H₂O ΔH° = −888 kJ
b) C(s) + O₂(g) → CO₂(g) ΔH° = −393 kJ
c) 2 H₂(g) + O₂(g) → 2 H₂O(l) ΔH° = −570 kJ
Anwendung: Satz von Hess
Eine Reaktionssequenz wird gesucht, deren Teilreaktionen aufsummiert werden können.
|
1. Schritt: a) Wählt einen Ausgangsstoff in der Gesamtreaktion aus b) schreibe eine Reaktionsgleichung, in der diese Substanz auch als Ausgangsstoff auftritt. |
1. Schritt: C als Ausgangsstoff → Gleichung b) C(s) + O₂(g) → CO₂(g) ΔH° = −393 kJ |
|
2. Schritt: a) Wähle eines der Produkte der Gesamtreaktion aus b) schreibe eine Reaktionsgleichung, in der diese Substanz auch als Produkt auftritt c) Summiere Gleichung 1 + 2. |
2. Schritt: Drehe Gleichung a) um (Vorzeichen ändern) CO₂(g) + 2 H₂O → CH₄(g) + 2 O₂(g) ΔH° = +888 kJ Addiere die zwei vorhergehenden Gleichungen (b) + (a) CO₂(g) + 2 H₂O + C(s) + O₂(g) → CO₂(g) + CH₄(g) + 2 O₂(g) ΔH° = −393 kJ + 888 kJ = +495 kJ Vereinfache so weit wie möglich 2 H₂O + C(s) → CH₄(g) + O₂(g) ΔH° = +495 kJ |
|
3. Schritt: a) Formuliere eine weitere Reaktionsgleichung, in der die unerwünschten Verbindungen jeweils auf der anderen Seite des Reaktionspfeils stehen. b) Lösche alle unerwünschten Verbindungen in der Summengleichung 2 aus. |
3. Schritt: unerwünschter Stoff (H₂O, O₂) → Gleichung c) 2 H₂(g) + O₂(g) → 2 H₂O(l) ΔH° = −570 kJ |
|
4. Schritt: a) Sobald Reaktionssequenz vollständig ist, summiert die Standard-Reaktionsenthalpien der Teilreaktionen. |
4. Schritt: Summiere die Gleichungen der Schritte 2 und 3 und vereinfache. 2 H₂O + C(s) + 2 H₂(g) + O₂(g) → CH₄(g) + O₂(g) + 2 H₂O(l) ΔH° = +495 kJ + (−570 kJ) = −75 kJ C(s) + 2 H₂(g) → CH₄(g) ΔH° = −75 kJ |
|
1.–4. Schritt: Es kann erforderlich sein, die Gleichung umzudrehen (Vorzeichenwechsel der Reaktionsenthalpie) oder mit einem Faktor zu multiplizieren. · Wolfram Hölzel, verändert nach P. Atkins, „Was ist Chemie"
|
|
🖼 Standardbildungsenthalpie von Methan als Bild anzeigen
Satz von Hess (Hess'scher Wärmesatz):
Die Enthalpieänderung ΔH eines Gesamtprozesses ist die Summe der Enthalpieänderungen der einzelnen Prozessschritte. Daraus folgt, dass die Reaktionsenthalpie unabhängig vom Reaktionsweg ist. Sie hängt nur vom Anfangs- und vom Endzustand des Systems ab.
1. Berechnung: Reduktion von Kupferoxid mit Zink
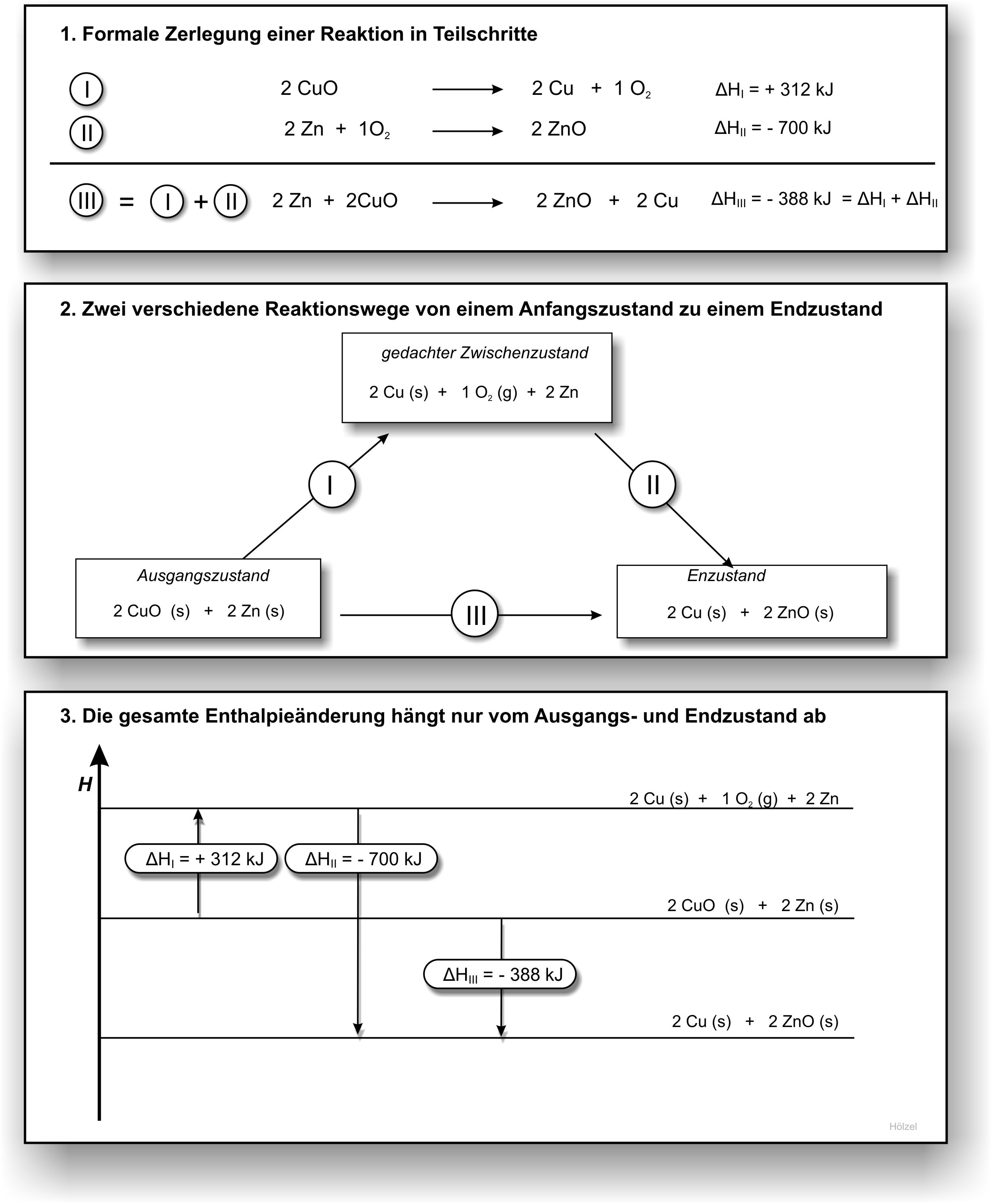
↑ Zum Vergrößern klicken
2. Berechnung der Verbrennungsenthalpie (Kohlenstoff zu Kohlenmonoxid)
Die molare Standard-Bildungsenthalpie ΔHf0(CO) = ΔHR10 kann experimentell nicht unmittelbar bestimmt werden, da ein Teil von CO zu CO₂ weiter reagiert. Man kann aber experimentell die folgenden molaren Reaktionsenthalpien messen.
Überlegt selbst, wie die Lösung lautet. Die Lösung bekommt ihr, wenn ihr über die Abbildung fahrt.
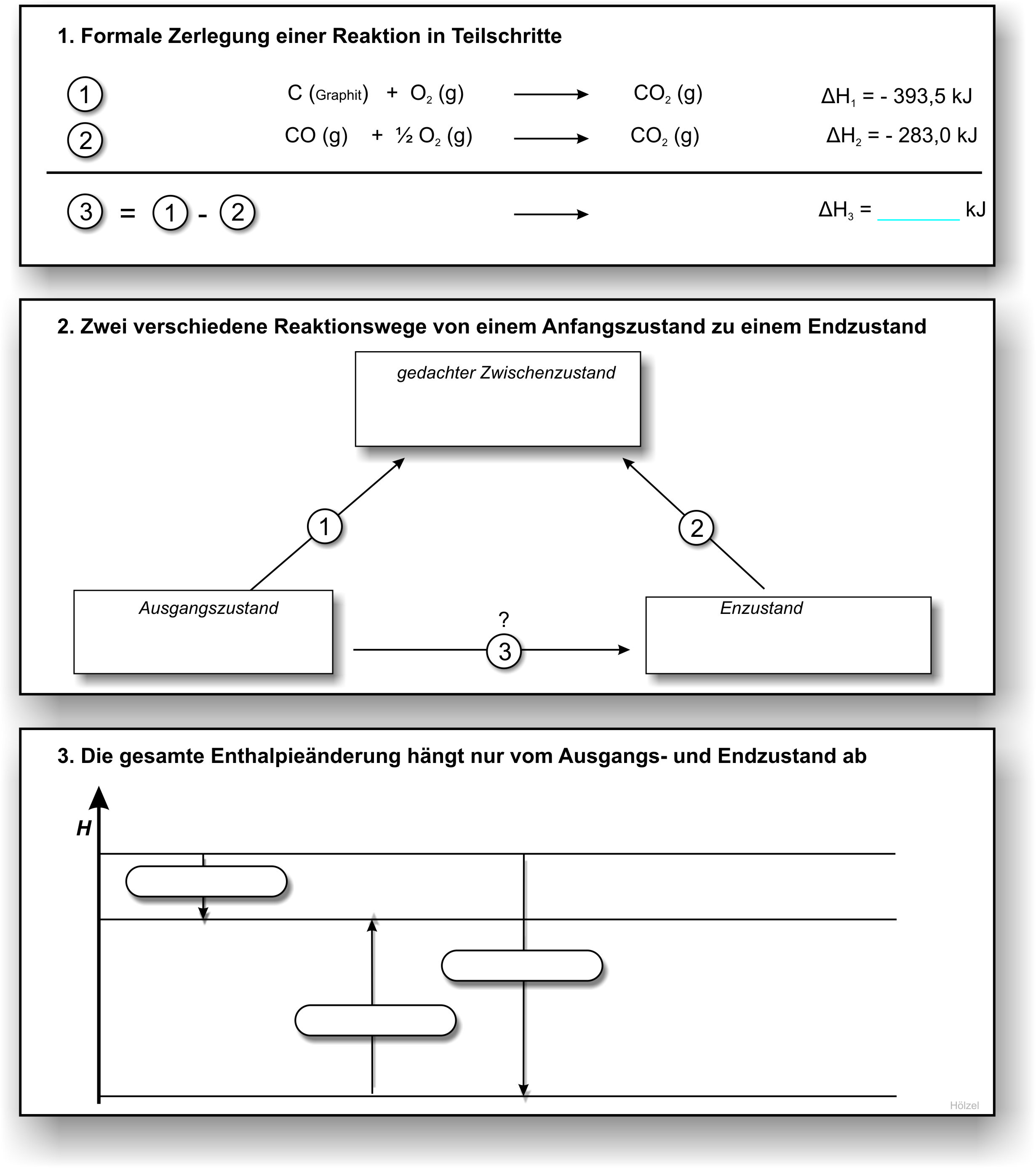
↑ Zum Vergrößern klicken · Maus drüberhalten für Lösung
Nach dem Energieerhaltungssatz ist es egal, ob Graphit zuerst nur bis zum Kohlenmonoxid und dieses dann bis zum Kohlenstoffdioxid weiter reagiert oder ob Graphit zum Kohlenstoffdioxid direkt verbrannt wird.
Auf einen Blick – die wichtigsten Aussagen
Methan-Bildungsenthalpie
C(s) + 2 H₂(g) → CH₄(g): ΔH° = −75 kJ/mol. Berechnet aus Verbrennungsenthalpien von CH₄, C und H₂.
Hess'scher Wärmesatz
ΔHGesamt = Σ ΔHTeilschritte. Voraussetzung: Enthalpie ist eine Zustandsfunktion.
Kreisprozess
Graphit → CO → CO₂ liefert dasselbe ΔH wie Graphit → CO₂ direkt. Basis für experimentell nicht messbare Enthalpien.
CO nicht direkt messbar
2C + O₂ → 2CO experimentell nicht rein realisierbar → ΔHf0(CO) muss indirekt berechnet werden.
Häufige Fragen
Wie berechnet man die Standardbildungsenthalpie von Methan?
Man nutzt die Verbrennungsenthalpien von CH₄, C und H₂. Schritt 1: C(s) → CO₂ (Gleichung b). Schritt 2: CO₂ + 2 H₂O → CH₄ + 2 O₂ (Gleichung a umgedreht, ΔH = +888 kJ). Schritt 3: 2 H₂ + O₂ → 2 H₂O (Gleichung c, für die unerwünschten Stoffe). Schritt 4: Alles summieren → ΔHf0(CH₄) = −75 kJ/mol.
Warum muss man manchmal eine Gleichung umdrehen und manchmal nicht?
Es hängt davon ab, auf welcher Seite die gewünschte Substanz steht. Im Schritt 1 braucht man den Ausgangsstoff als Edukt – kommt er als Produkt vor, dreht man um. Im Schritt 2 braucht man das Produkt als Produkt – kommt es als Edukt vor, dreht man um. Das Umdrehen kostet nur ein Vorzeichen bei ΔH.
Was versteht man unter einem Kreisprozess beim Satz von Hess?
Ein Kreisprozess beschreibt einen Reaktionsweg, bei dem man vom Ausgangszustand über einen oder mehrere Zwischenschritte zum Endzustand gelangt – und dabei dieselbe Enthalpieänderung erhält wie auf dem direkten Weg. Das Beispiel C → CO → CO₂ (indirekter Weg) liefert dasselbe ΔH wie C → CO₂ (direkt).
Welche Verbindungen lassen sich nur mit dem Satz von Hess berechnen?
Alle, deren Bildungsreaktion experimentell nicht realisierbar ist: CO (immer CO₂-Beimengung), viele organische Verbindungen mit langsamen Bildungsreaktionen, instabile Zwischenprodukte. Der Satz von Hess ist daher ein unverzichtbares Werkzeug der physikalischen Chemie.
Wie hängen Satz von Hess und Standardbildungsenthalpie zusammen?
Die Formel ΔHR0 = Σ ΔHf0(Produkte) − Σ ΔHf0(Edukte) aus Abschnitt 8.3 ist nichts anderes als der Satz von Hess, angewendet über den Umweg durch die reinen Elemente im Standardzustand.
Lernkarten – Satz von Hess Teil II
Klicke auf eine Karte, um die Antwort zu sehen.
Berechne ΔHf0(CH₄) aus:
a) CH₄+2O₂→CO₂+2H₂O: −888 kJ
b) C+O₂→CO₂: −393 kJ
c) 2H₂+O₂→2H₂O: −570 kJ
b) direkt: −393 kJ
rev.a): +888 kJ → +495 kJ
c) −570 kJ
ΔH° = −75 kJ/mol ✓
Was ist der Hess'sche Wärmesatz in einer Formel?
ΔHGesamt = Σ ΔHTeilschritte
Oder: ΔHR0 = Σ ΔHf0(Produkte) − Σ ΔHf0(Edukte)
Warum lässt sich ΔHf0(CO) nicht direkt messen?
Bei Verbrennung von C entsteht immer auch CO₂. Reines CO als einziges Produkt ist experimentell nicht realisierbar → indirekte Berechnung über Hess.
Was bedeutet „Kreisprozess" beim Satz von Hess?
Man geht vom Ausgangszustand über Umwege zum Endzustand. Da ΔH wegunabhängig ist, ergibt die Summe aller Teilschritte dasselbe ΔH wie der direkte Weg.
🔢 Graphit → CO₂ direkt: −394 kJ. Graphit → CO: −111 kJ. CO → CO₂: ?
Satz von Hess: ΔH(direkt) = ΔH(CO-Bildung) + ΔH(CO→CO₂)
−394 = −111 + x
x = −283 kJ/mol
Weiter im Kapitel Energetik
← 8.6 Satz von Hess → 9. Bindungsenthalpien 8.3 Standardbildungsenthalpie 11. Entropie S 12. Gibbs-Energie G
