Was du auf dieser Seite lernst
Du lernst den Aufbau eines Chloroplasten und wie Licht Elektronen im Chlorophyll anregt. Im Mittelpunkt steht die nichtzyklische Lichtreaktion (Z-Schema): Wie Wasser gespalten wird (Fotolyse), wie Elektronen von P680 über die Elektronentransportkette zu P700 und weiter zu NADPH fließen, und wie dabei ATP durch Chemiosmose gewonnen wird.
Exkurs: Fotosynthese
Chloroplast, Lichtanregung und Primärreaktion (Z-Schema) · Biologie Kursstufe BW
Im Folgenden findest du einen Schnellabriss der Primärreaktion sowie eine Übersicht der Fotosynthese. Die Abschnitte bauen aufeinander auf – lies sie der Reihe nach durch und überprüfe dein Verständnis anschließend mit den Lernkarten.
1. Aufbau eines Chloroplasten
Der Chloroplast ist der Ort der Fotosynthese in Pflanzenzellen. Er besitzt eine Doppelmembran sowie ein inneres Membransystem aus flachen Thylakoidscheiben, die zu Grana aufgestapelt sind und in das flüssige Stroma eingebettet liegen.
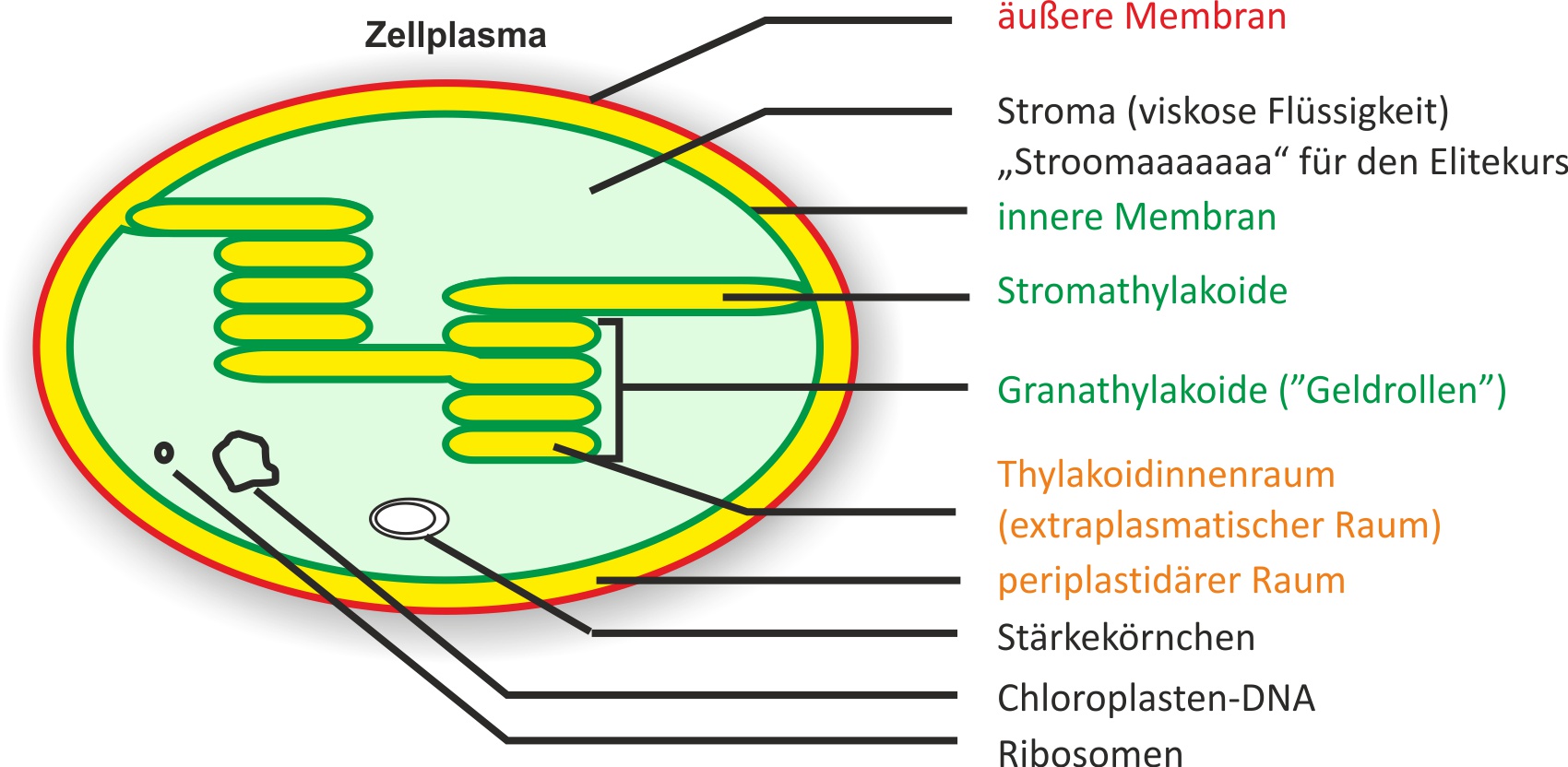
↑ Zum Vergrößern klicken · Abb. 1 – Querschnittsskizze eines Chloroplasten. Gut zu erkennen: die gestapelten Thylakoide (Grana) in der Stroma-Matrix sowie die Doppelmembran.
2. Lichtanregung des Chlorophylls
Bei der Absorption von Licht nehmen Elektronen der Farbstoffmoleküle die Energie auf. Ein Elektron kann nur die Energiemenge aufnehmen, die ziemlich genau dem Unterschied zwischen Grundzustand und Anregungszustand entspricht – daher absorbiert Chlorophyll bevorzugt rotes (~680 nm) und blaues (~430 nm) Licht. Grünes Licht wird überwiegend reflektiert, weshalb Blätter grün erscheinen.
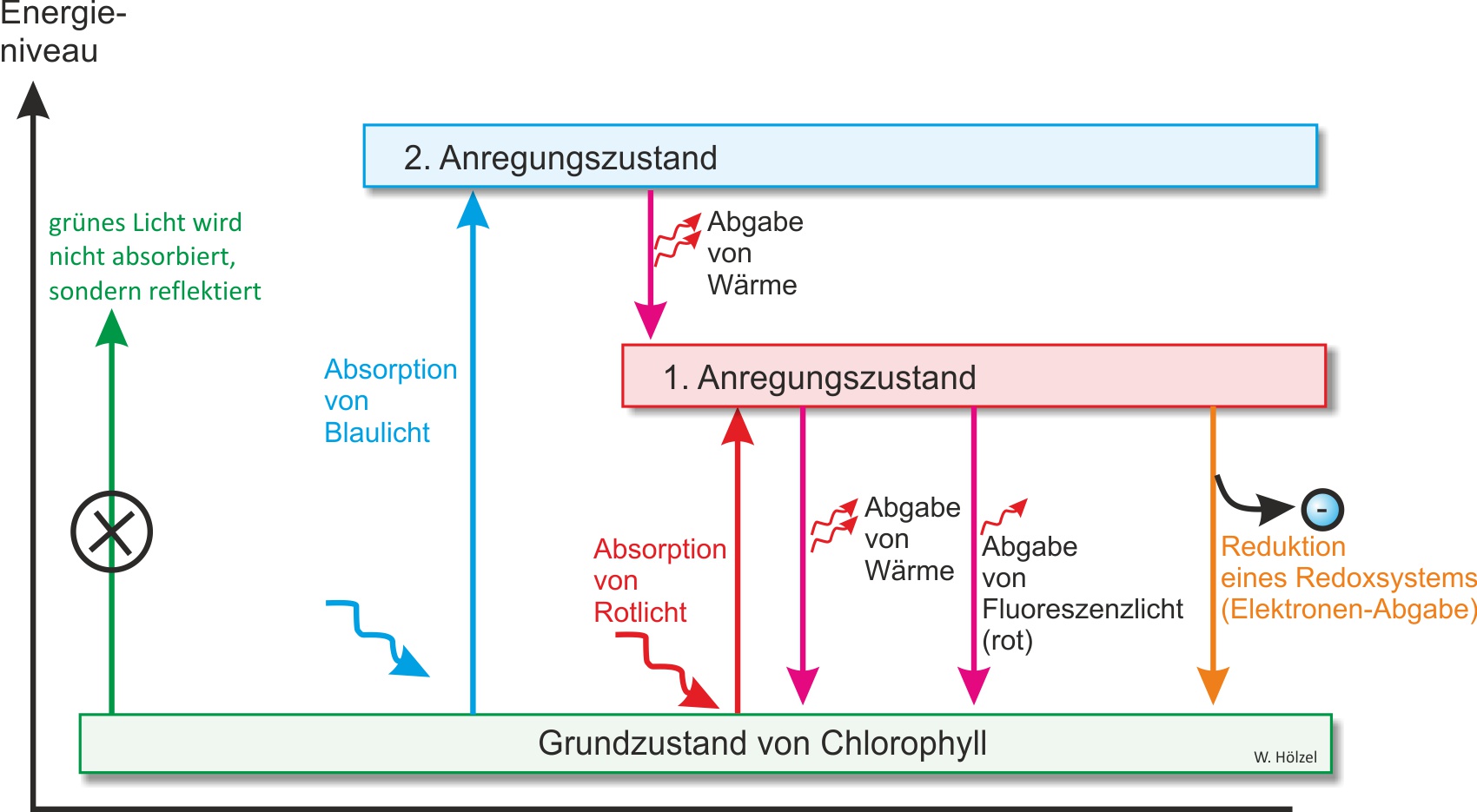
↑ Zum Vergrößern klicken · Abb. 2 – Lichtanregung des Chlorophylls. Nur bestimmte Wellenlängen haben genau die richtige Energie, um Elektronen anzuheben.
3. Lichtabhängige Reaktionen – Primärreaktion
a) Z-Schema der nichtzyklischen Lichtreaktion
Das Z-Schema zeigt schematisch, wie Elektronen bei der nichtzyklischen Lichtreaktion von Wasser über zwei Photosysteme zum NADP+ fließen. Der Name leitet sich von der Z-förmigen Kurve im Energiediagramm ab.
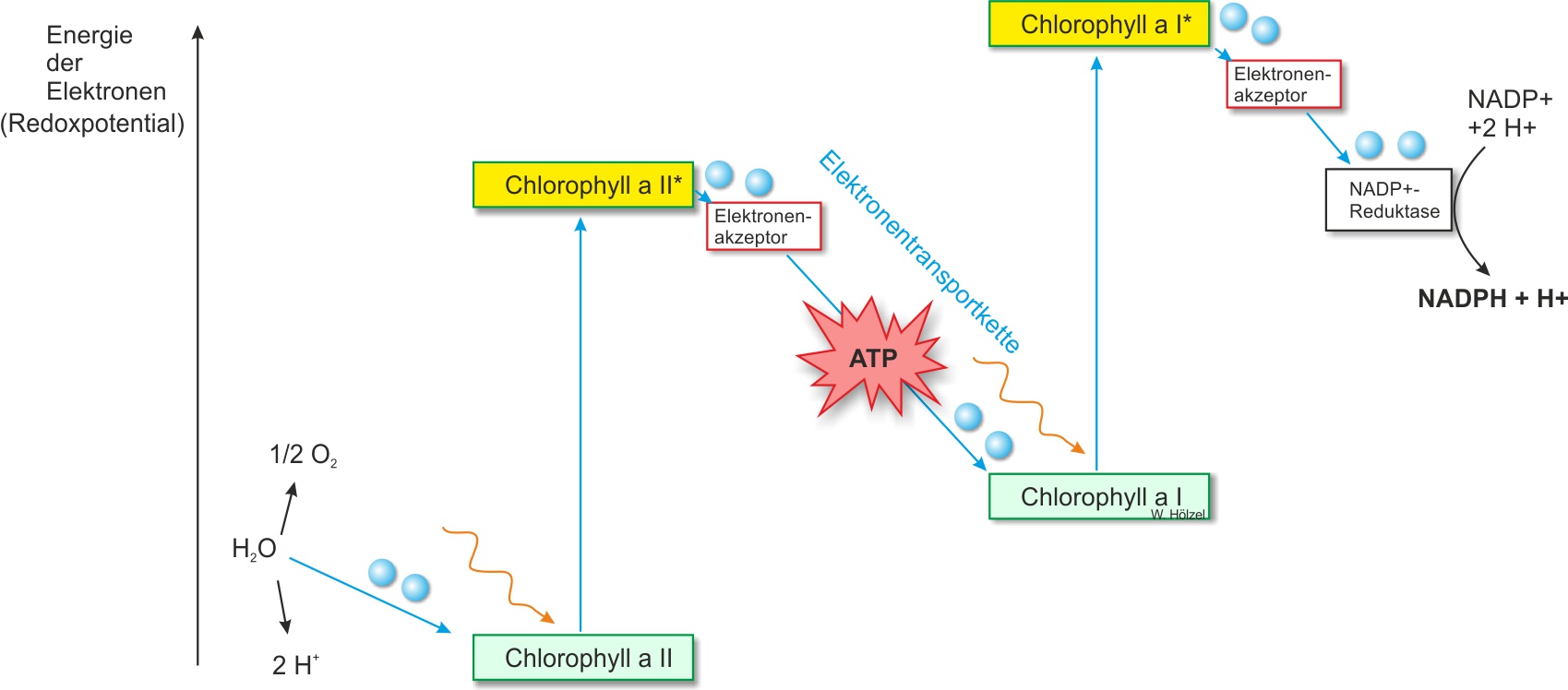
↑ Zum Vergrößern klicken · Abb. 3 – Z-Schema der Lichtreaktion. Die y-Achse repräsentiert den Energiegehalt der Elektronen. Von P680 (links, niedriges Niveau nach Fotolyse) bis NADPH (rechts, hohes Niveau) ergibt sich der namensgebende Z-förmige Verlauf.
Ablauf der nichtzyklischen Lichtreaktion:
Absorption von Lichtenergie am Chlorophyll-Paar a II (P680) → Anregung → 2 Elektronen werden abgespalten und auf den danebenliegenden Elektronenakzeptor übertragen (Reduktion des Akzeptors).
Elektronenweitergabe entlang der Elektronentransportkette: P680 → Elektronenakzeptor → Plastochinon → Cytochrom-b6f-Komplex → Plastocyanin → Chlorophyll a I (P700). Dieser Transport pumpt H+-Ionen in den Thylakoidinnenraum und erzeugt so den Protonengradienten für die ATP-Synthase.
Weitere Lichtanregung von P700 → 2 Elektronen abgespalten → Elektronenakzeptor → Ferredoxin → NADP+-Reduktase → Übertragung auf NADP+ (wird reduziert zu NADPH + H+).
Problem: Woher kommen die Elektronen für P680?
Fotolyse: Ein manganhaltiges Enzym (OEC – Oxygen Evolving Complex) entzieht Wassermolekülen ihre Elektronen und liefert sie an P680. Als Nebenprodukt entsteht der Sauerstoff, den wir atmen:
2 H2O → O2 + 4 H+ + 4 e−
Bei der nichtzyklischen Lichtreaktion fließen so permanent Elektronen von Wassermolekülen zum NADPH + H+.
b) ATP-Gewinnung durch Protonengradienten (Chemiosmose)
Parallel zur Elektronenweitergabe werden H+-Ionen in den Thylakoidinnenraum gepumpt. Das entstehende Konzentrationsgefälle (Protonengradient) treibt die ATP-Synthase an – dieser Vorgang heißt Chemiosmose.
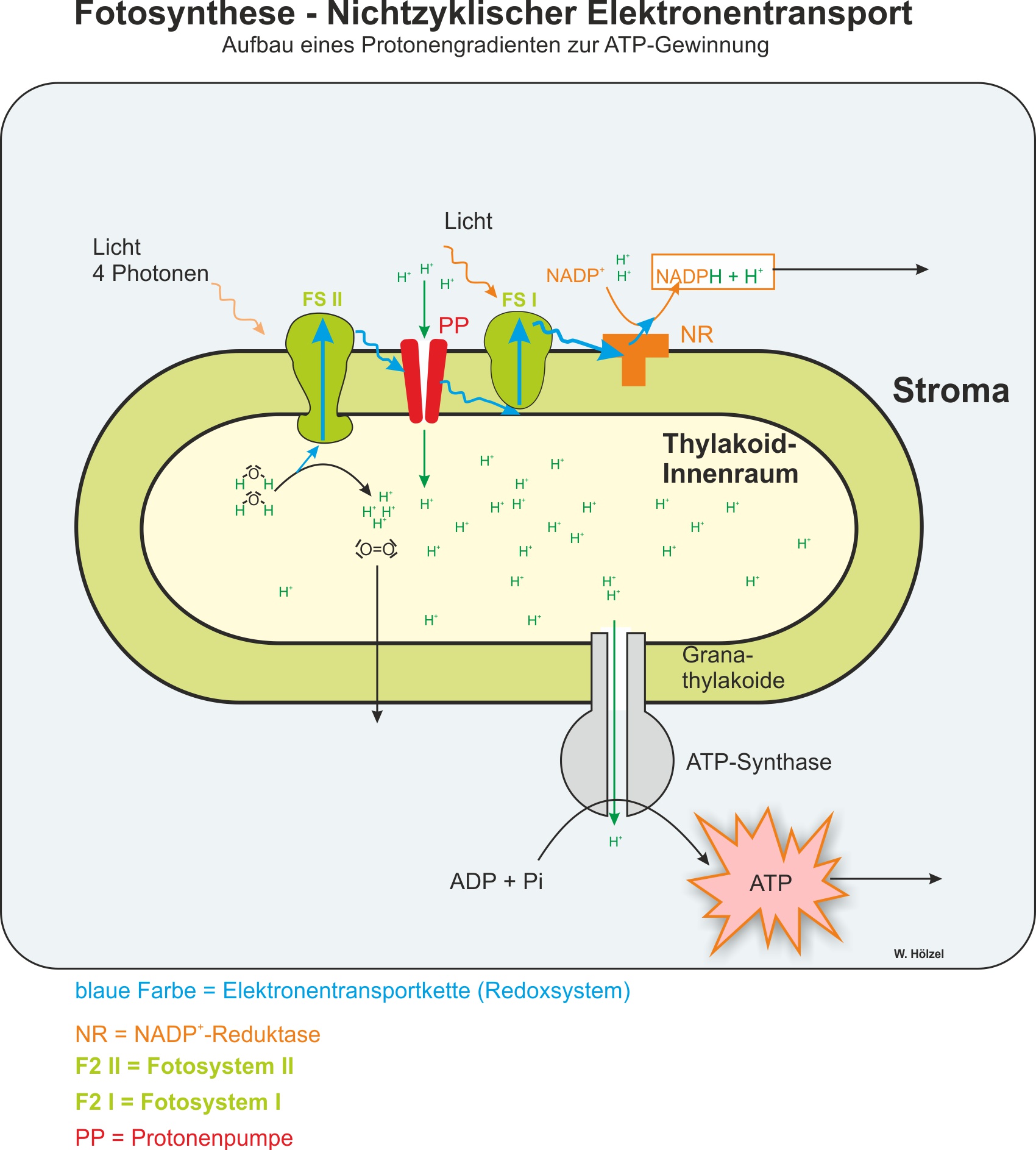
↑ Zum Vergrößern klicken · Abb. 4 – Modell der lichtabhängigen Reaktion in der Thylakoidmembran. Der Elektronentransport von PS II zu PS I baut einen H+-Gradienten auf (Chemiosmose → ATP). Am Ende entsteht NADPH als Reduktionsmittel für den Calvin-Zyklus.
Auf einen Blick – die wichtigsten Aussagen
Chloroplast
Ort der Fotosynthese. Doppelmembran + Thylakoide (gestapelt zu Grana) in flüssigem Stroma. Lichtreaktion: Thylakoid; Calvin-Zyklus: Stroma.
Z-Schema
Elektronen fließen: H₂O → P680 → Elektronentransportkette → P700 → NADPH. Zwei Lichtanregungen nötig (PS II + PS I). Freisetzung von O₂ als Nebenprodukt.
Fotolyse
2 H₂O → O₂ + 4 H⁺ + 4 e⁻. Manganhaltiges Enzym (OEC) liefert Elektronen an P680. Quelle des gesamten atmosph. Sauerstoffs.
Produkte der Lichtreaktion
ATP (Energieträger) und NADPH (Reduktionsmittel) – beide werden im Calvin-Zyklus zur CO₂-Fixierung verwendet.
Häufige Fragen zur Fotosynthese-Primärreaktion
Was ist der Unterschied zwischen Lichtreaktion und Calvin-Zyklus?
Die Lichtreaktion (Primärreaktion) läuft in der Thylakoidmembran ab und wandelt Lichtenergie in chemische Energie um: Es entstehen ATP und NADPH, außerdem wird O₂ freigesetzt. Der Calvin-Zyklus (Dunkelreaktion) läuft im Stroma ab und verwendet ATP und NADPH, um CO₂ zu Zucker (Glucose) zu fixieren – er benötigt kein direktes Licht, aber er hört ohne Nachschub aus der Lichtreaktion schnell auf.
Warum heißt das Schema „Z-Schema"?
Im Energiediagramm, in dem die y-Achse den Energiegehalt der Elektronen darstellt, ergibt der Weg der Elektronen einen Z-förmigen Verlauf: Erst sinkt das Energieniveau (Elektronenabgabe durch P680 nach Fotolyse), dann steigt es durch die zweite Lichtanregung (P700) wieder stark an, bis die Elektronen schließlich auf NADP⁺ übertragen werden und NADPH entsteht.
Welche Rolle spielt der Protonengradient bei der ATP-Synthese?
Während der Elektronen entlang der Transportkette wandern, werden H⁺-Ionen aktiv in den Thylakoidinnenraum gepumpt. Dadurch entsteht ein starkes Konzentrationsgefälle (hohe H⁺-Konzentration innen, niedrig außen). Die H⁺-Ionen strömen durch die ATP-Synthase zurück ins Stroma – dieser Fluss treibt das Enzym wie eine Turbine an und erzeugt ATP aus ADP + Pi. Dieses Prinzip heißt Chemiosmose (Mitchell-Hypothese).
Warum erscheinen Blätter grün, obwohl sie Licht für Fotosynthese brauchen?
Chlorophyll absorbiert bevorzugt rotes (~680 nm) und blaues (~430 nm) Licht – diese Wellenlängen werden für die Fotosynthese genutzt. Grünes Licht (~520–560 nm) wird von Chlorophyll nur schlecht absorbiert und stattdessen reflektiert. Dieses reflektierte grüne Licht nehmen unsere Augen wahr – daher erscheinen Blätter grün. Die Pflanze „verschwendet" also keine nutzbare Energie.
Was passiert, wenn kein Wasser für die Fotolyse vorhanden ist?
Ohne Wasser fehlen P680 die Ersatz-Elektronen nach der Lichtanregung. PS II kann keine weiteren Elektronen in die Transportkette einspeisen. Die gesamte nichtzyklische Lichtreaktion kommt zum Stillstand: kein ATP aus Chemiosmose, kein NADPH. Außerdem akkumulieren reaktive Sauerstoffspezies (ROS), die die Fotosysteme schädigen können. Bei Trockenstress schließen Pflanzen daher die Stomata – was wiederum die CO₂-Aufnahme für den Calvin-Zyklus drosselt.
Lernkarten – Fotosynthese Primärreaktion
Klicke auf eine Karte, um die Antwort zu sehen.
Nenne die drei Kompartimente des Chloroplasten und ordne Lichtreaktion und Calvin-Zyklus zu.
Stroma (flüssig): Calvin-Zyklus
Thylakoidmembran: Lichtreaktion (Elektronentransport, ATP-Synthase)
Thylakoidlumen: H⁺-Reservoir (Protonengradient)
Warum absorbiert Chlorophyll rotes und blaues Licht – und nicht grünes?
Ein Elektron kann nur genau die Energie aufnehmen, die dem Unterschied zwischen Grundzustand und Anregungszustand entspricht. Rotes und blaues Licht haben passende Wellenlängen (~680 nm / ~430 nm). Grünes Licht (~540 nm) passt nicht → wird reflektiert → Blätter erscheinen grün.
Beschreibe den Elektronenweg im Z-Schema von Wasser bis NADPH.
H₂O → (Fotolyse) → P680 → Elektronenakzeptor → Plastochinon → Cyt-b6f → Plastocyanin → P700 → Ferredoxin → NADP⁺-Reduktase → NADPH
Was ist Fotolyse? Nenne Reaktionsgleichung und das wichtigste Nebenprodukt.
Lichtabhängige Spaltung von Wasser durch ein manganhaltiges Enzym (OEC):
2 H₂O → O₂ + 4 H⁺ + 4 e⁻
Nebenprodukt: O₂ – Quelle des gesamten atmosphärischen Sauerstoffs!
🔢 Wie viele O₂-Moleküle entstehen, wenn 6 H₂O-Moleküle durch Fotolyse gespalten werden? Wie viele Elektronen werden dabei freigesetzt?
Reaktion: 2 H₂O → O₂ + 4 H⁺ + 4 e⁻
6 H₂O = 3 × (2 H₂O) →
3 O₂-Moleküle
12 Elektronen (3 × 4 e⁻)
12 H⁺
Weiter in der Biologie
← Jahrgangsstufen-Übersicht Biologie-Übersicht Calvin-Zyklus (noch nicht online)
- Details
- Geschrieben von: Wolfram Hölzel
