Siedetemperatur
-
01.7 Struktur und Eigenschaften der Alkane
Was du auf dieser Seite lernst
Die Struktur der Alkane bestimmt ihre Eigenschaften. Du lernst, warum Alkane reaktionsträge sind, welche zwischenmolekularen Kräfte (ZMK) zwischen ihren Molekülen wirken und was das für Siedepunkt, Schmelzpunkt und Löslichkeit bedeutet.
Grundlagen aus der 9. Klasse
Polare und unpolare Bindungen sowie zwischenmolekulare Kräfte (ZMK) hast du bereits in der 9. Klasse kennengelernt:
→ Polare und unpolare Atombindung (Kl. 9) · → Elektrische Dipole (Kl. 9)1.7 Struktur und Eigenschaften der Alkane
1.7.1 Bindungsverhältnisse
a) Bindungsverhältnisse im Molekül lassen bestimmte chemische Verhaltensweisen voraussagen:
- sehr starke Einfachbindung
→ reaktionsträge - fast unpolare Atombindung
→ normalerweise keine Reaktion als Säure (auch keine Eigenprotolyse), da kein Proton abgespalten wird.
→ bei starkem Erhitzen bzw. starkem Angriff kommt es zur symmetrischen (radikalischen, homolytischen) Spaltung der Bindung.
- keine freien Elektronenpaare
→ kann nicht als Base reagieren (kann kein Proton aufnehmen) - keine Elektronenpaarlücke
→ kann nicht als elektrophiles Teilchen reagieren b) Bindungen bzw. Kräfte zwischen den Molekülen (ZMKs) sind verantwortlich für die physikalischen Eigenschaften (Siedetemperatur, Schmelztemperatur, Löslichkeit etc.):
- nur van-der-Waals-Kräfte
- keine Wasserstoffbrücken
- keine Dipol-Dipol-Wechselwirkungen
- Siedepunkt ist niedrig (steigt mit der Molekülgröße)
- Schmelzpunkt ist niedrig (steigt mit der Molekülgröße)
- Löslichkeit: schlecht in Stoffen, in denen starke Wasserstoffbrücken vorliegen
- Löslichkeit: schlecht in polaren Stoffen
- Alkane lösen keine Salze, da sie keine Solvationshüllen ausbilden
Alkane sind typisch unpolare Stoffe (hydrophob, wassermeidend).
Auf einen Blick – die wichtigsten Aussagen
REAKTIONSTRÄGHEIT
Starke, fast unpolare C–C- und C–H-Bindungen machen Alkane reaktionsträge – weder Säure noch Base noch Nucleophil noch Elektrophil.
ZMK
Zwischen Alkanmolekülen wirken nur van-der-Waals-Kräfte – keine Wasserstoffbrücken, keine Dipol-Wechselwirkungen.
SIEDEPUNKT
Mehr C-Atome → größere Moleküloberfläche → stärkere vdW-Kräfte → höherer Siedepunkt. Stärkere Verzweigung senkt den Siedepunkt.
HYDROPHOB
Alkane sind unpolar und wassermeidend (hydrophob). Sie lösen sich nicht in Wasser und lösen keine Salze.
Häufige Fragen – Eigenschaften der Alkane
Warum sind Alkane so reaktionsträge?
Die C–C- und C–H-Bindungen in Alkanen sind sehr stark und fast unpolar (Elektronegativitätsunterschied sehr gering). Dadurch bieten Alkane weder freie Elektronenpaare (kein Angriffspunkt für Elektrophile) noch eine Elektronenpaarlücke (kein Angriffspunkt für Nucleophile). Auch eine Protonenabgabe findet praktisch nicht statt. Nur unter extremen Bedingungen – sehr hohe Temperaturen oder UV-Licht – kommt es zur homolytischen Bindungsspaltung und damit zu einer radikalischen Reaktion.
Warum steigt der Siedepunkt der Alkane mit der Kettenlänge?
Mit jedem zusätzlichen C-Atom wächst die Moleküloberfläche. Größere Oberfläche bedeutet mehr Kontaktfläche zwischen den Molekülen und damit stärkere van-der-Waals-Kräfte. Um ein Molekül aus dem flüssigen Zustand zu befreien, muss mehr Energie aufgewendet werden → der Siedepunkt steigt. Methan (C1) siedet bei –162 °C, Hexan (C6) bereits bei +69 °C.
Warum lösen sich Alkane nicht in Wasser?
Wasser ist ein stark polares Lösungsmittel, das ausgeprägte Wasserstoffbrücken zwischen seinen Molekülen ausbildet. Alkane sind unpolar und können keine entsprechenden Wechselwirkungen mit Wasser eingehen. Nach dem Prinzip „Gleiches löst Gleiches" (lat. similia similibus solvantur) bleiben Alkane in Wasser ungelöst und bilden eine separate Phase (z. B. Öl auf Wasser). Salze lösen Alkane ebenfalls nicht auf, da Alkane keine Solvationshüllen um Ionen ausbilden können.
Warum haben verzweigte Alkane niedrigere Siedepunkte als unverzweigte?
Je stärker ein Alkan verzweigt ist, desto kompakter (kugelförmiger) ist das Molekül. Die Oberfläche, über die van-der-Waals-Kräfte wirken können, wird kleiner → die Anziehungskräfte zwischen den Molekülen sind schwächer → der Siedepunkt sinkt. Beispiel: n-Pentan (unverzweigt) siedet bei 36 °C, 2,2-Dimethylpropan (stark verzweigt) bereits bei 9 °C – obwohl beide die gleiche Summenformel C5H12 haben. Mehr dazu unter: → Isomere von C₇H₁₆.
Was ist die homolytische (radikalische) Spaltung einer Bindung?
Bei der homolytischen Spaltung teilen sich beide Bindungspartner die gemeinsamen Elektronen gleichmäßig auf – jedes Atom erhält ein Elektron. Es entstehen Radikale (Teilchen mit einem ungepaarten Elektron), die sehr reaktiv sind. Dies geschieht bei Alkanen nur unter extremen Bedingungen wie hohen Temperaturen oder UV-Strahlung. Es ist die Grundlage der radikalischen Substitution. Im Gegensatz dazu werden bei der heterolytischen Spaltung beide Elektronen von einem Partner behalten.
Lernkarten – Eigenschaften der Alkane
Klicke auf eine Karte, um die Antwort zu sehen.
1Warum sind Alkane reaktionsträge? Nenne zwei Gründe.
1. C–C- und C–H-Bindungen sind sehr stark.
2. Die Bindungen sind fast unpolar → kein Angriffspunkt für Nucleophile oder Elektrophile.2Welche ZMK wirken zwischen Alkanmolekülen?
Ausschließlich van-der-Waals-Kräfte. Keine Wasserstoffbrücken, keine Dipol-Dipol-Wechselwirkungen (Alkane sind unpolar).
3Warum steigt der Siedepunkt der Alkane mit der Kettenlänge?
Mehr C-Atome → größere Oberfläche → stärkere van-der-Waals-Kräfte → mehr Energie nötig zum Verdampfen → höherer Siedepunkt.
4Was bedeutet „hydrophob"? Warum sind Alkane hydrophob?
Hydrophob = wassermeidend. Alkane sind unpolar → können keine Wechselwirkungen mit polarem Wasser eingehen → lösen sich nicht in Wasser.
5n-Pentan oder 2,2-Dimethylpropan – welches hat den höheren Siedepunkt? Begründe.
n-Pentan (Sdp. 36 °C) > 2,2-Dimethylpropan (Sdp. 9 °C). n-Pentan ist gestreckter → größere Oberfläche → stärkere vdW-Kräfte – obwohl beide C5H12 sind.
Weiter im Kapitel Alkane
← 1.6 Übungen zur Nomenklatur → 1.8 Angriffsfreudige Teilchen
🔁 Grundlagen: Polare und unpolare Atombindung (Kl. 9) · Elektrische Dipole (Kl. 9)
-
01.9 Reaktion von Alkanen mit Halogenen
Was du auf dieser Seite lernst
Alkane reagieren unter Lichtzufuhr mit Halogenen in einer radikalischen Substitution (SR): Ein Wasserstoff-Atom wird durch ein Halogen-Atom ersetzt. Du lernst den dreistufigen Reaktionsmechanismus kennen und erfährst, welche Eigenschaften die entstehenden Halogenalkane haben.
Grundlagen – Angriffsfreudige Teilchen
Radikale und die homolytische Bindungsspaltung hast du auf der vorherigen Seite kennengelernt:
→ 1.8 Angriffsfreudige Teilchen · → 1.7 Eigenschaften der Alkane1.9 Reaktion von Alkanen mit Halogenen
1.9.1 Versuch
Experiment:
Gemisch aus 4 ml Isooctan (2,2,4-Trimethylpentan) und 1,3 ml Brom werden belichtet.
An das entstehende Gas wird …- … Flasche mit konz. Ammoniak
- … feuchtes pH-Papier
… gehalten.
Es entstehen:
a) ein farbloses Gas:
- Nebelbildung an feuchter Luft (HBr);
- mit Ammoniak bildet sich ein weißer Rauch (Ammoniak und der Stoff reagiert zu einem porösen Salz (NH4Br));
- angefeuchtetes Indikatorpapier färbt sich rot (Säure muss entstanden sein → HBr).
→ Die Beobachtungen sprechen dafür, dass das farblose Gas Bromwasserstoff (HBr) ist.
b) eine Flüssigkeit:
- größere Dichte als Wasser;
- Beilsteinprobe positiv (Beilsteinprobe: halogenhaltige Verbindungen ergeben mit Kupfer in der Flamme eine Grünfärbung).
→ Die Flüssigkeit ist ein Bromalkan (hauptsächlich).
1.9.2 Reaktionsschema
Alkan + Brom —(Belichtung)→ Bromalkan + Bromwasserstoff
Allgemein:
Alkan + Halogen —(Belichtung)→ Halogenalkan + Halogenwasserstoff1.9.3 Reaktionsmechanismus
(vereinfacht: statt Isooctan wird Methan verwendet)
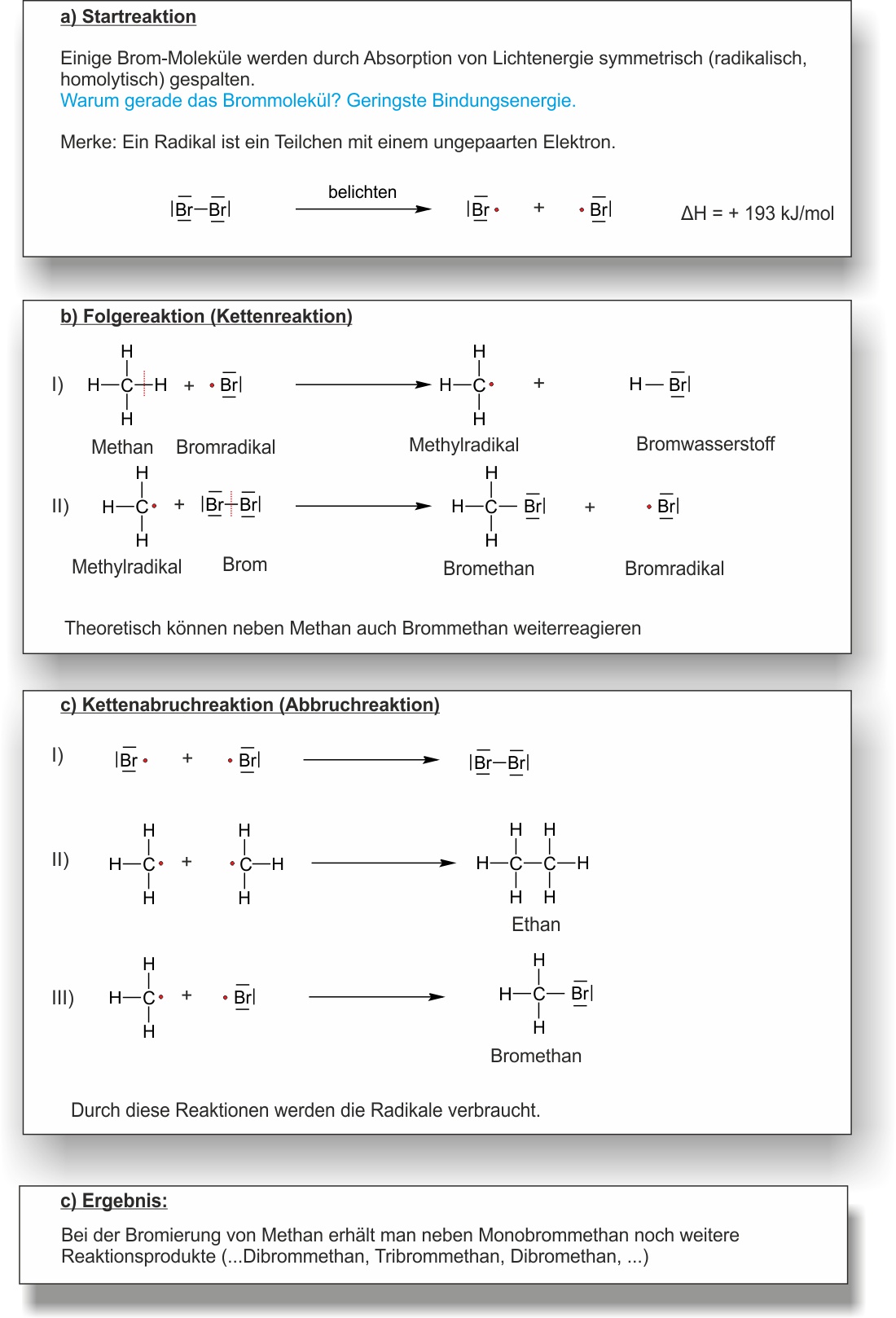
Folgende Abbildung zeigt den Reaktionsmechanismus der radikalischen Substitutionsreaktion zu einem Halogenalkan unter Bildung eines Halogenwasserstoffs.
↑ Zum Vergrößern klicken
✕
Merke
Reaktionen, bei denen Atome oder Atomgruppen einer Verbindung durch andere Atome ersetzt werden, bezeichnet man als Substitution.
Die Bromierung von Methan ist eine radikalische Substitution (SR-Reaktion).1.9.4 Halogenalkane
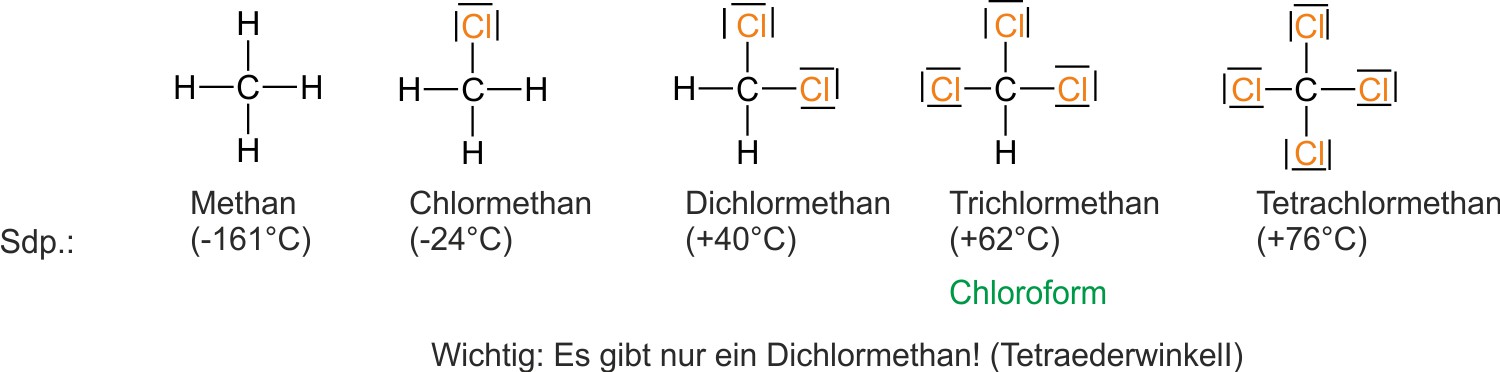
a) Halogenalkane sind Derivate (Abkömmlinge) der Alkane.
↑ Zum Vergrößern klicken
✕
b) Eigenschaften der Halogenalkane:
Löslichkeit Halogenalkane sind in Wasser unlöslich.
Sie sind sehr gute Lösungsmittel für Alkane und Fette (hydrophobe Stoffe).Dichte Halogenalkane haben meistens eine größere Dichte als 1 g/cm³. Siedetemperatur Sie liegt bei Halogenalkanen höher als bei vergleichbaren Alkanen (Grund: größere van-der-Waals-Kräfte). Brennbarkeit Je mehr H-Atome durch Halogen-Atome ersetzt sind, umso schlechter ist die Brennbarkeit der Halogenalkane. c) Verwendung:
- hervorragende Lösungsmittel (Extraktion pflanzlicher Öle, Entfetten von Metallteilen, chemische Reinigung …)
- Treibgase in Sprays
- Kältemittel für Kühlanlagen
- Feuerlöschmittel (Halon, Bromtrifluormethan)
- Desinfektionsmittel (Jodoform, Trijodmethan)
- Insektizide (Lindan, Hexachlorcyclohexan)
Auf einen Blick – die wichtigsten Aussagen
STARTREAKTION
Licht spaltet Br₂ homolytisch → zwei Br-Radikale (Br•). Energiezufuhr notwendig, läuft nur einmal ab.
KETTENREAKTION
Br• + CH₄ → HBr + CH₃• · CH₃• + Br₂ → CH₃Br + Br• · Das Radikal regeneriert sich ständig → Kettenreaktion.
ABBRUCH
Zwei Radikale rekombinieren → stabile Verbindung. Kette bricht ab, wenn Radikale aufeinandertreffen.
HALOGENALKANE
Dichte > 1 g/cm³ · in Wasser unlöslich · höherer Sdp. als Alkane · weniger brennbar je mehr Halogenatome.
Häufige Fragen – Radikalische Substitution und Halogenalkane
Was ist eine radikalische Substitution (SR)?
Bei einer Substitution wird ein Atom oder eine Atomgruppe in einem Molekül durch ein anderes Atom ersetzt. Bei der radikalischen Substitution (SR) übernehmen Radikale die Angreiferrolle. Bei der Bromierung von Methan wird ein H-Atom durch ein Br-Atom ersetzt: CH₄ + Br₂ → CH₃Br + HBr. Die Reaktion läuft als Kettenreaktion in drei Stufen ab: Startreaktion, Kettenreaktion, Abbruchreaktion.
Warum wird für die Bromierung von Alkanen Licht benötigt?
Die Reaktion beginnt mit der Startreaktion: Licht (hν) liefert die nötige Energie, um die Br–Br-Bindung homolytisch zu spalten – jedes Br-Atom erhält ein Elektron und wird zum Radikal (Br•). Diese Br-Radikale lösen die Kettenreaktion aus. Ohne Lichtzufuhr findet keine Startreaktion statt, und die Gesamtreaktion kommt nicht in Gang.
Welche drei Schritte hat der Reaktionsmechanismus der SR?
1. Startreaktion: Br₂ →(hν)→ 2 Br• (einmalig, braucht Energie).
2. Kettenreaktion (läuft sehr oft ab):
Br• + CH₄ → HBr + CH₃• (Br-Radikal zieht H ab)
CH₃• + Br₂ → CH₃Br + Br• (Methyl-Radikal greift Br₂ an, neues Br• entsteht)
3. Abbruchreaktion: Zwei Radikale rekombinieren, z. B. CH₃• + Br• → CH₃Br. Die Kette bricht ab.Warum haben Halogenalkane einen höheren Siedepunkt als vergleichbare Alkane?
Halogenatome sind größer und polarisierbarer als Wasserstoff-Atome. Dadurch sind die van-der-Waals-Kräfte zwischen Halogenalkanmolekülen stärker als zwischen reinen Alkanmolekülen gleicher Kettenlänge. Stärkere ZMK bedeuten mehr Energie zum Verdampfen → höherer Siedepunkt. Zusätzlich besitzen C–X-Bindungen (X = Halogen) einen Dipolcharakter, der weitere Anziehungskräfte beiträgt.
Was ist die Beilsteinprobe und was zeigt sie an?
Die Beilsteinprobe ist ein einfacher Nachweis für halogenhaltige organische Verbindungen. Dazu wird ein Kupferdraht in der Flamme erhitzt und dann kurz in die Probe getaucht. Enthält die Substanz Halogene (Cl, Br, I), färbt sich die Flamme charakteristisch grün (durch Kupferhalogenid-Verbindungen). Beim Versuch in 1.9.1 wurde so bestätigt, dass die entstandene Flüssigkeit ein Bromalkan ist.
Lernkarten – Radikalische Substitution
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist eine Substitution? Was bedeutet „radikalisch"?
Substitution: Ein Atom/Gruppe wird durch ein anderes ersetzt. Radikalisch: Der Angreifer ist ein Radikal (Einzelelektron).
2Nenne die drei Stufen der SR-Reaktion.
1. Startreaktion (Br₂ + hν → 2 Br•)
2. Kettenreaktion (Radikale reagieren, neues Radikal entsteht)
3. Abbruchreaktion (zwei Radikale rekombinieren)3Welche Produkte entstehen bei der Bromierung von Methan?
CH₄ + Br₂ →(hν)→ CH₃Br (Brommethan) + HBr (Bromwasserstoff).
4Nenne zwei Unterschiede zwischen Halogenalkanen und Alkanen.
1. Dichte > 1 g/cm³ (Alkane < 1).
2. Höherer Siedepunkt (stärkere vdW-Kräfte).
3. In Wasser unlöslich, aber gutes Lösungsmittel für Fette.5Methan wird zweifach bromiert. Nenne Produkt und systematischen Namen.
CH₄ + 2 Br₂ →(hν)→ CH₂Br₂ + 2 HBr
Name: Dibrommethan (Di- für zwei Br-Atome, Stamm Methan).Weiter in der Organischen Chemie
← 1.8 Angriffsfreudige Teilchen → 2.1 Ethen – Alkene
🔁 Grundlagen: Eigenschaften der Alkane (Kl. 10) · Radikale & Elektrophile (Kl. 10)
-
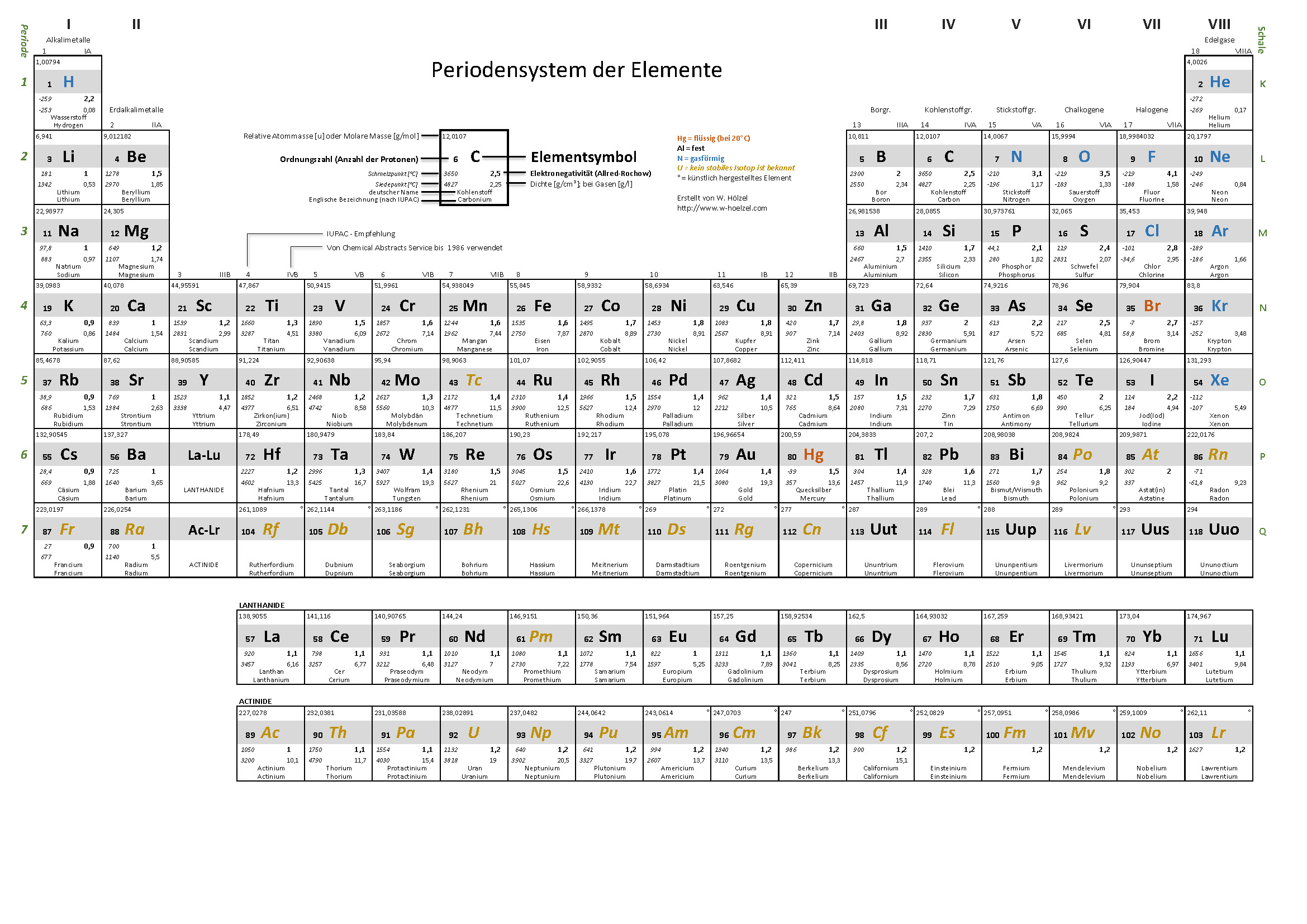
Periodensystem der Elemente - PSE
Ich habe für meine Schüler Periodensysteme erstellt, die jederzeit ausgedruckt werden können. Das Ziel: je nach Aufgabenstellung nur die wesentlichen Informationen. Die Werte stammen aus verschiedenen Quellen (www.wikipedia.de, www.internetchemie.info, Mortimer „Chemie", Holleman-Wiberg „Lehrbuch der anorganischen Chemie").
Falls gravierende Fehler vorhanden sind, würde ich mich über eine Nachricht freuen. Diese Periodensysteme können heruntergeladen und ausgedruckt werden.
Kurze Einführung in das Periodensystem der Elemente
Eine kurze Einführung in das PSE mit einfachen Übungen findest du auf meiner Basischemie-Seite. Allerdings ist das empfohlene PSE nicht mehr online (weshalb ich selber welche erstellte; vgl. unten).
Periodensysteme
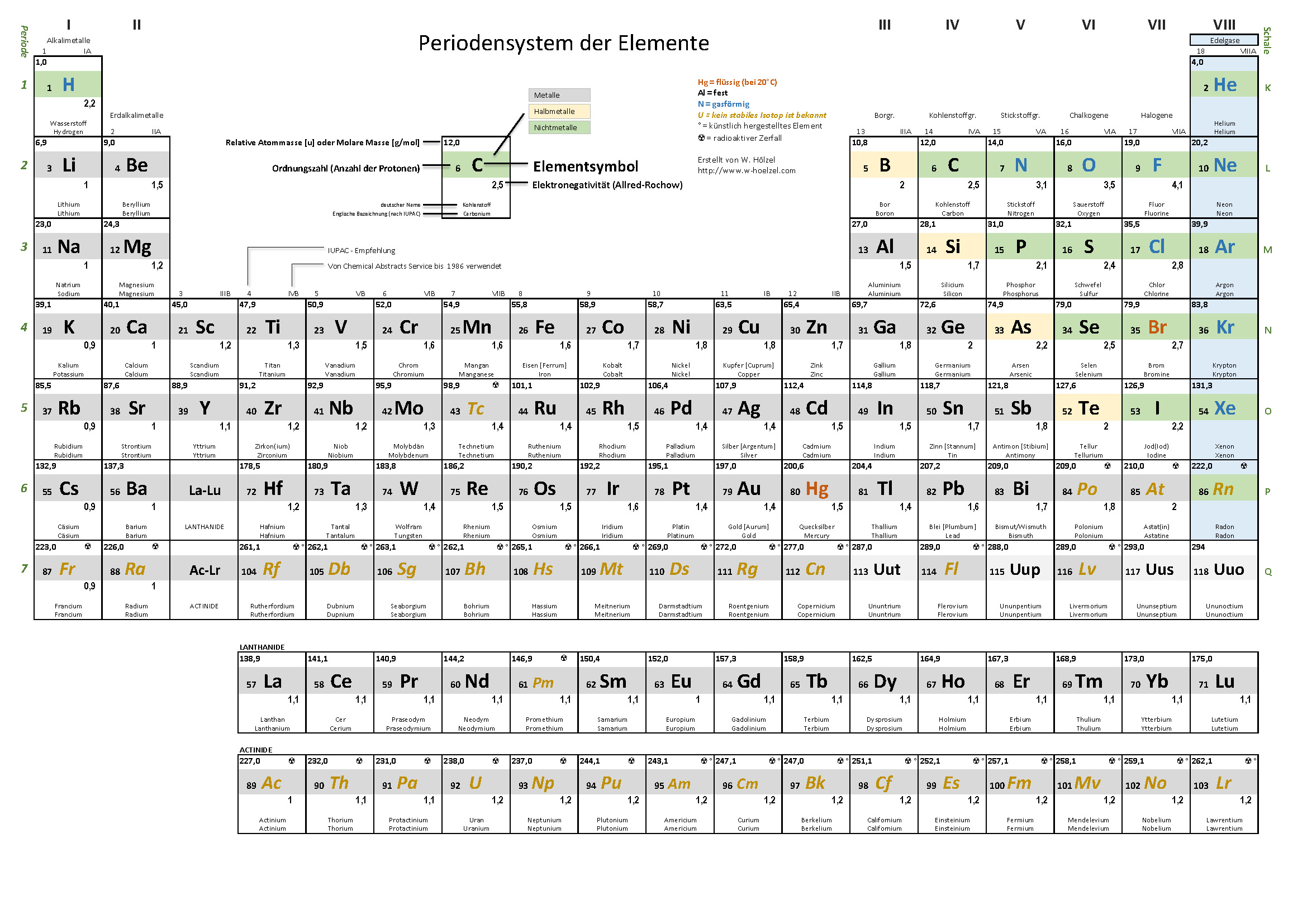
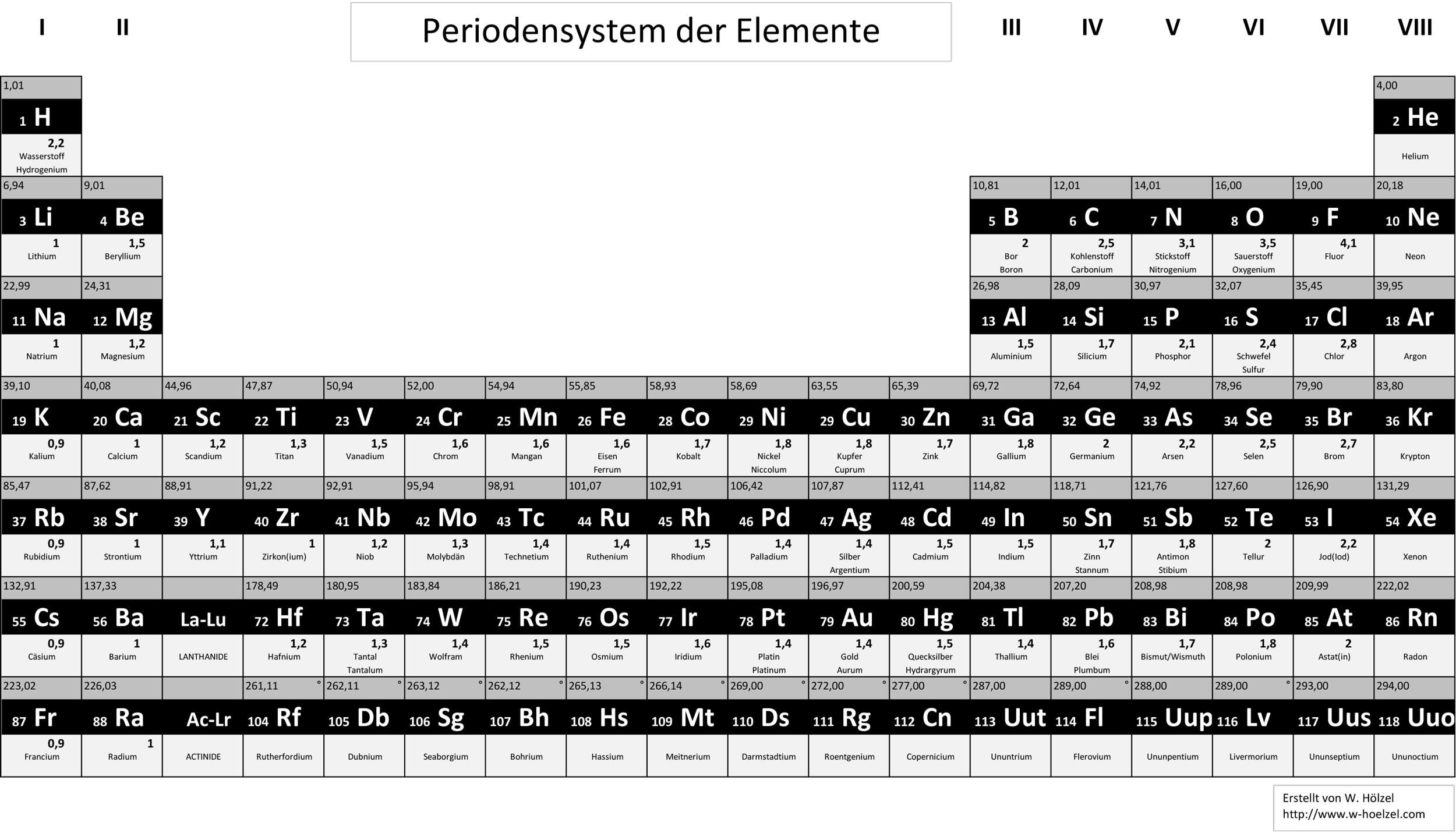
1. Einfaches PSE für die Schule
Beschränkt sich auf die wesentlichen Informationen. Auch die Halbmetalle sind sehr einfach wiedergegeben.
- Elektronegativität
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Halbmetalle (vereinfacht; vgl. Wikipedia)
- Metalle · Nichtmetalle · Edelgase
- Aggregatzustand bei 20 °C
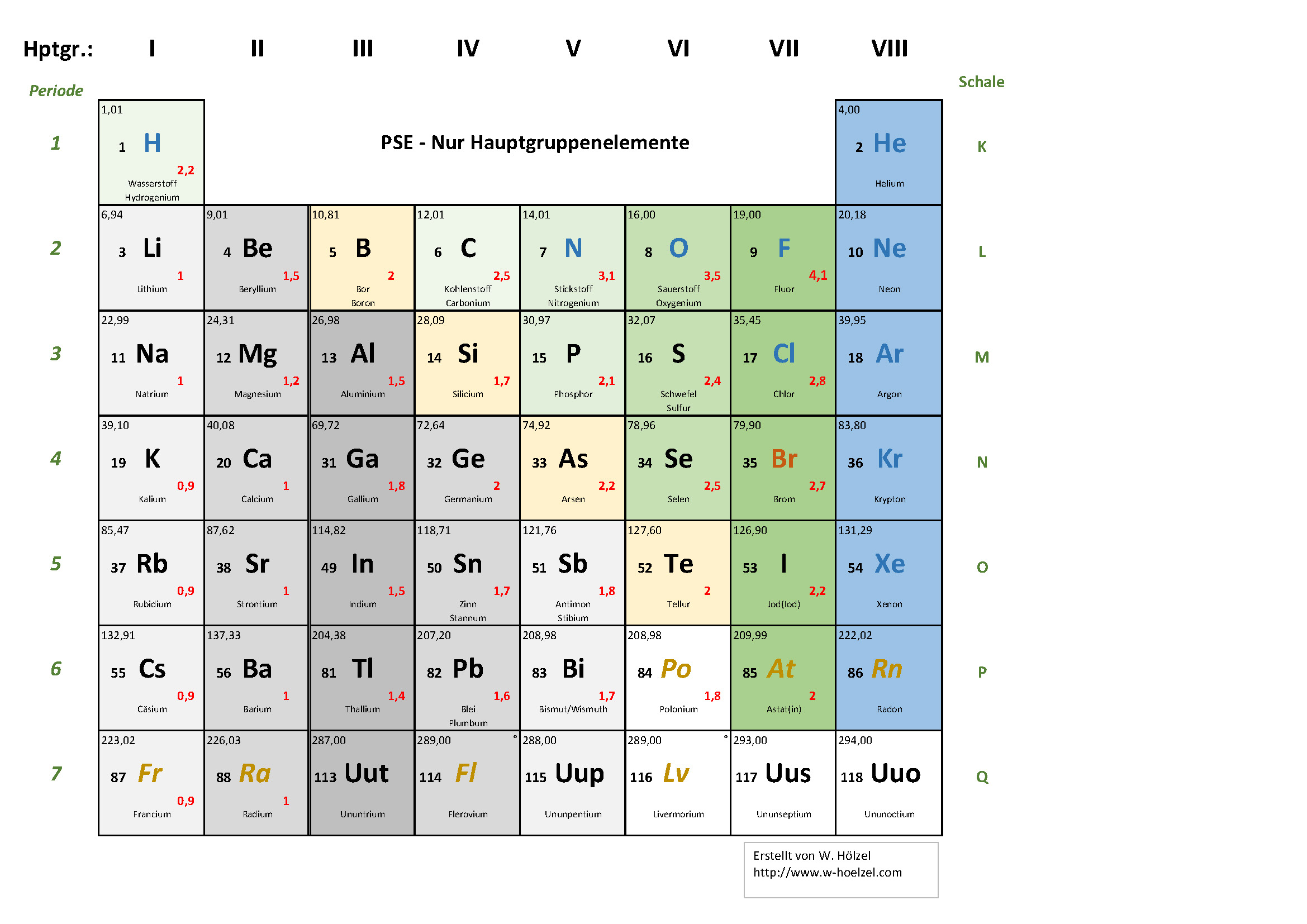
3. PSE – Nur Hauptgruppenelemente
Für Edelgasregel, Atombindungen und erste Salze — ohne Nebengruppen.
- Elektronegativität
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Halbmetalle (vgl. Wikipedia)
- Metalle · Nichtmetalle · Edelgase
- KEINE Nebengruppen, Lanthanide, Actinide

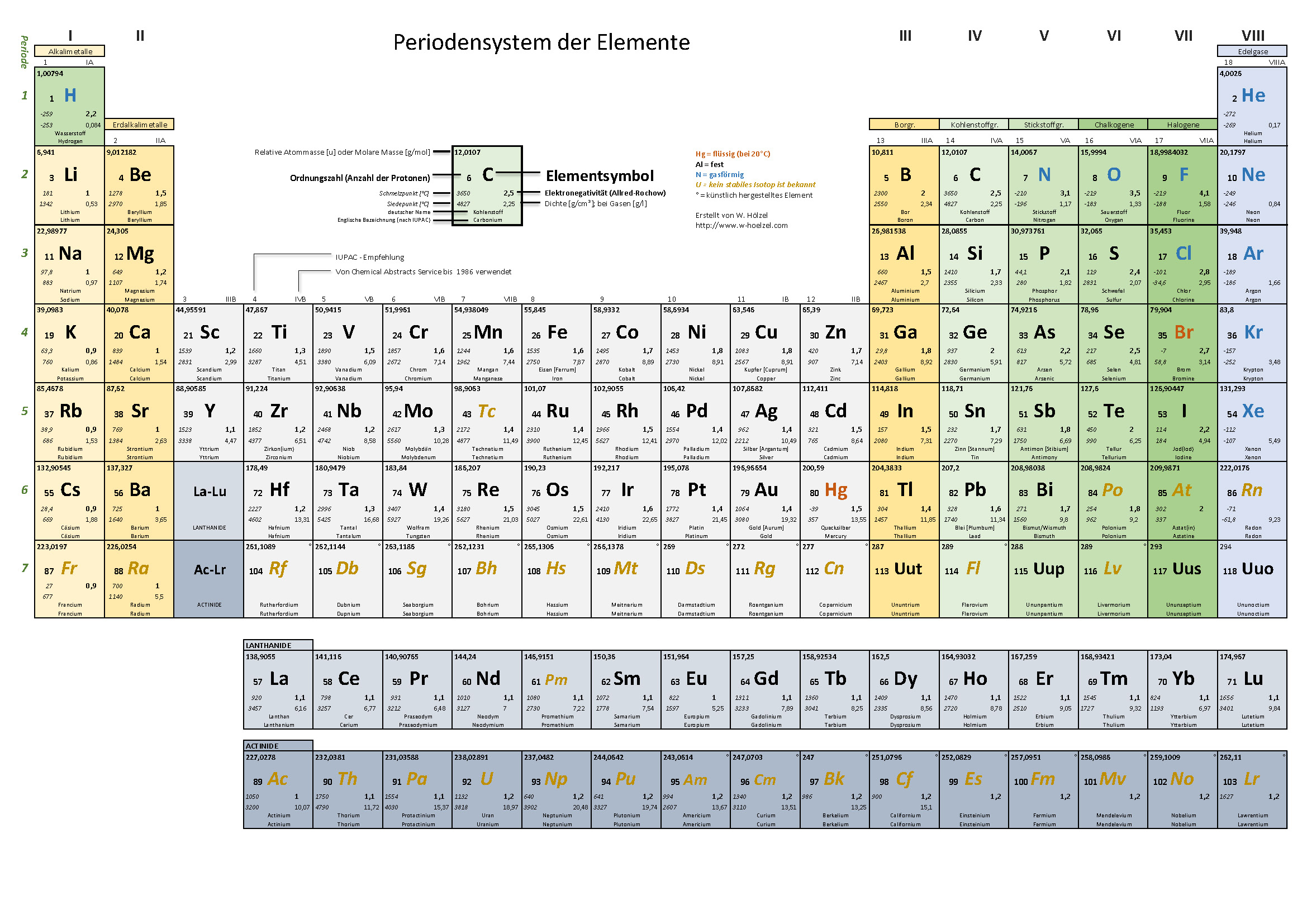
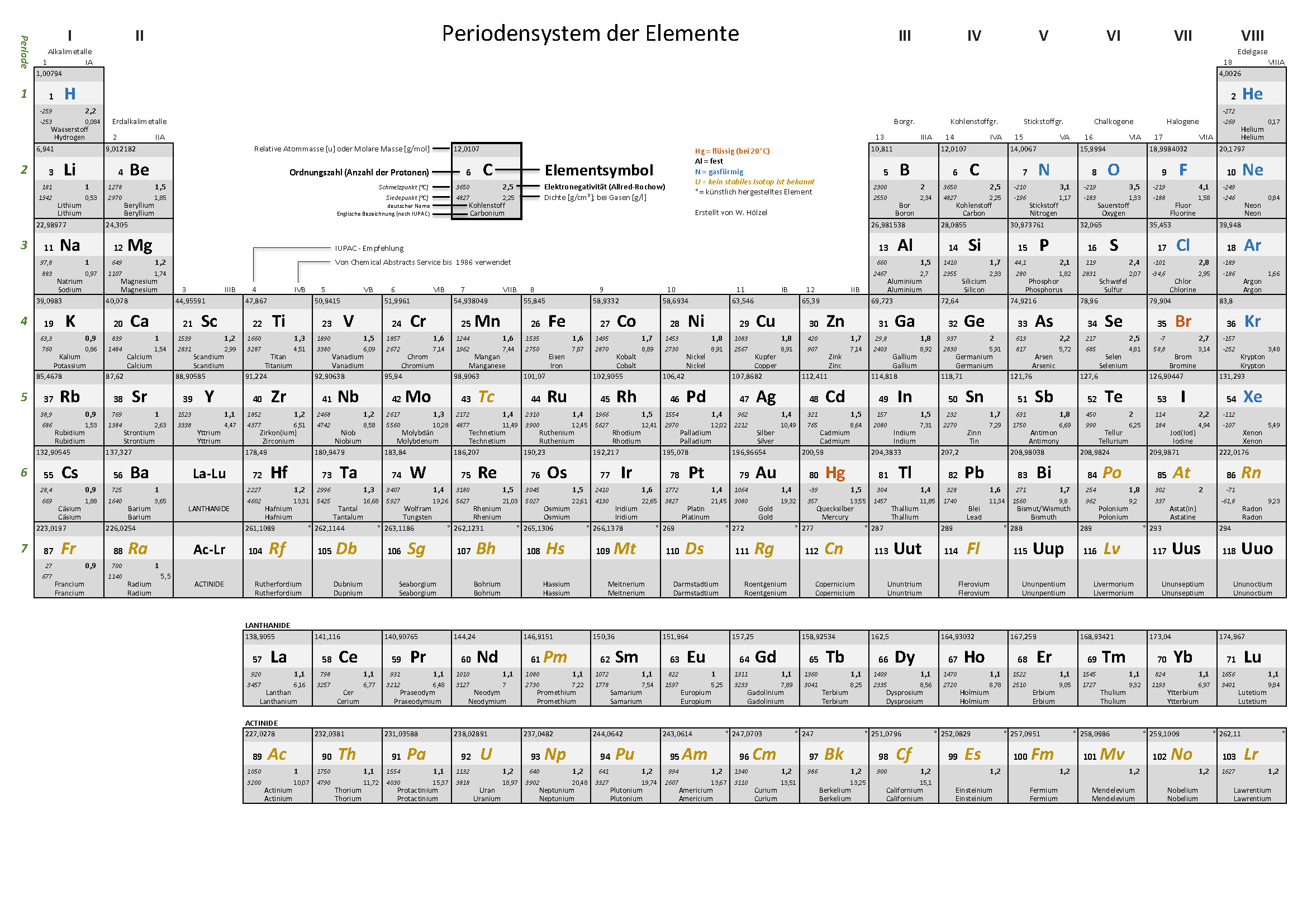
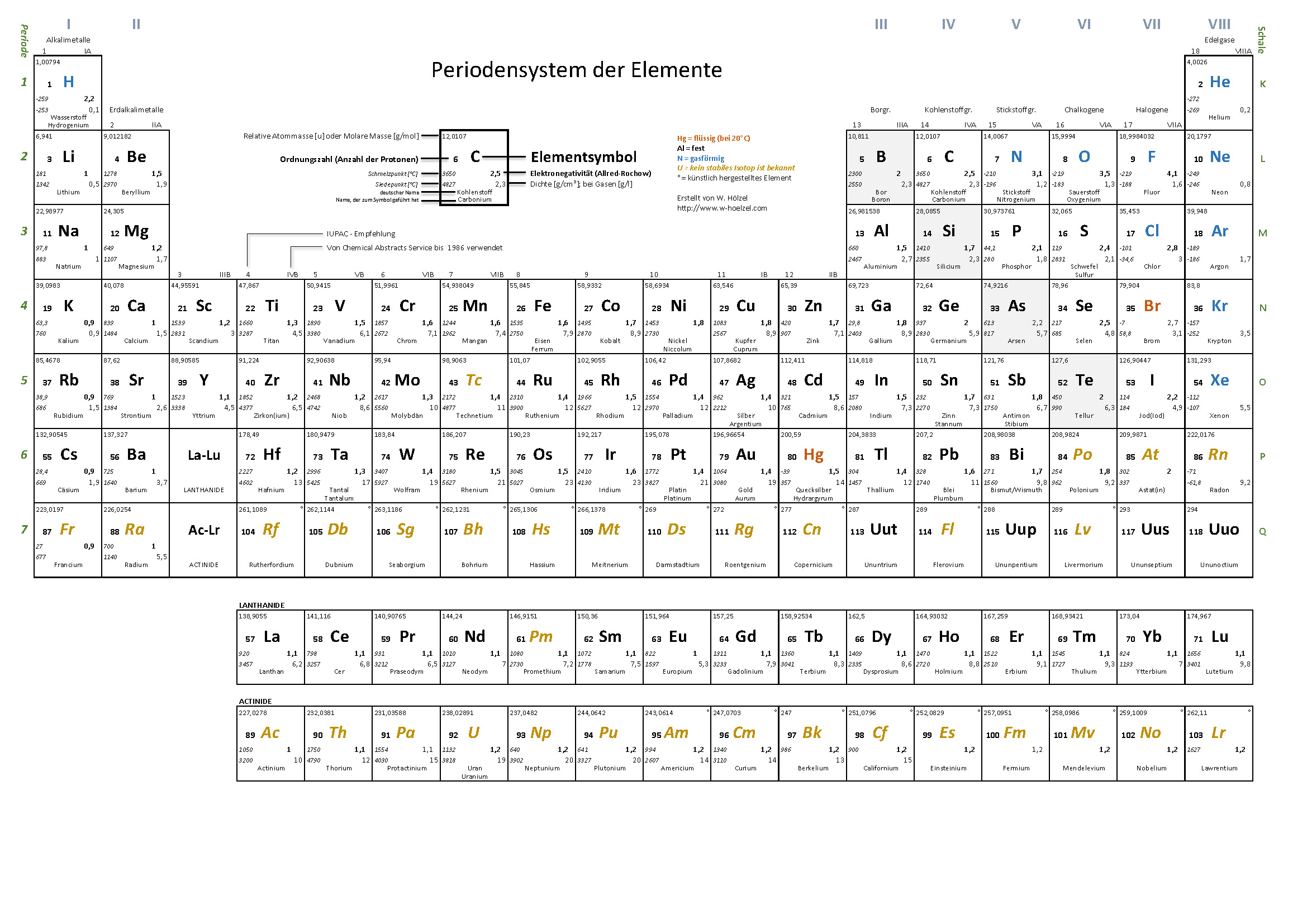
6. PSE – Einteilung Metalle / Nichtmetalle
Farbige Einteilung der Metalle, Halbmetalle, Nichtmetalle und Edelgase.
- Elektronegativität
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Halbmetalle (vgl. Wikipedia)
- Metalle · Nichtmetalle · Edelgase
- Aggregatzustand · Dichte · Schmelz- und Siedetemperatur
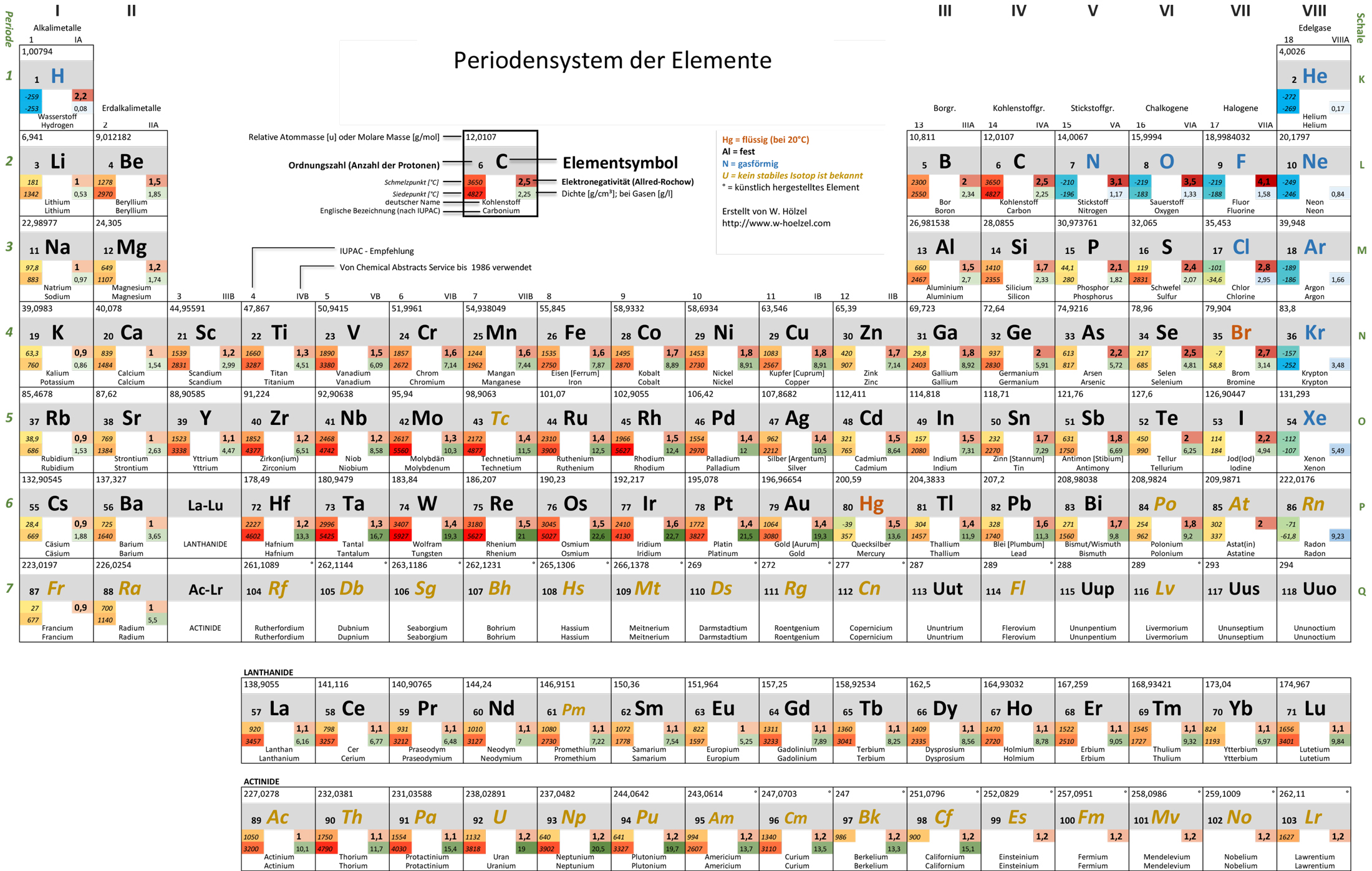
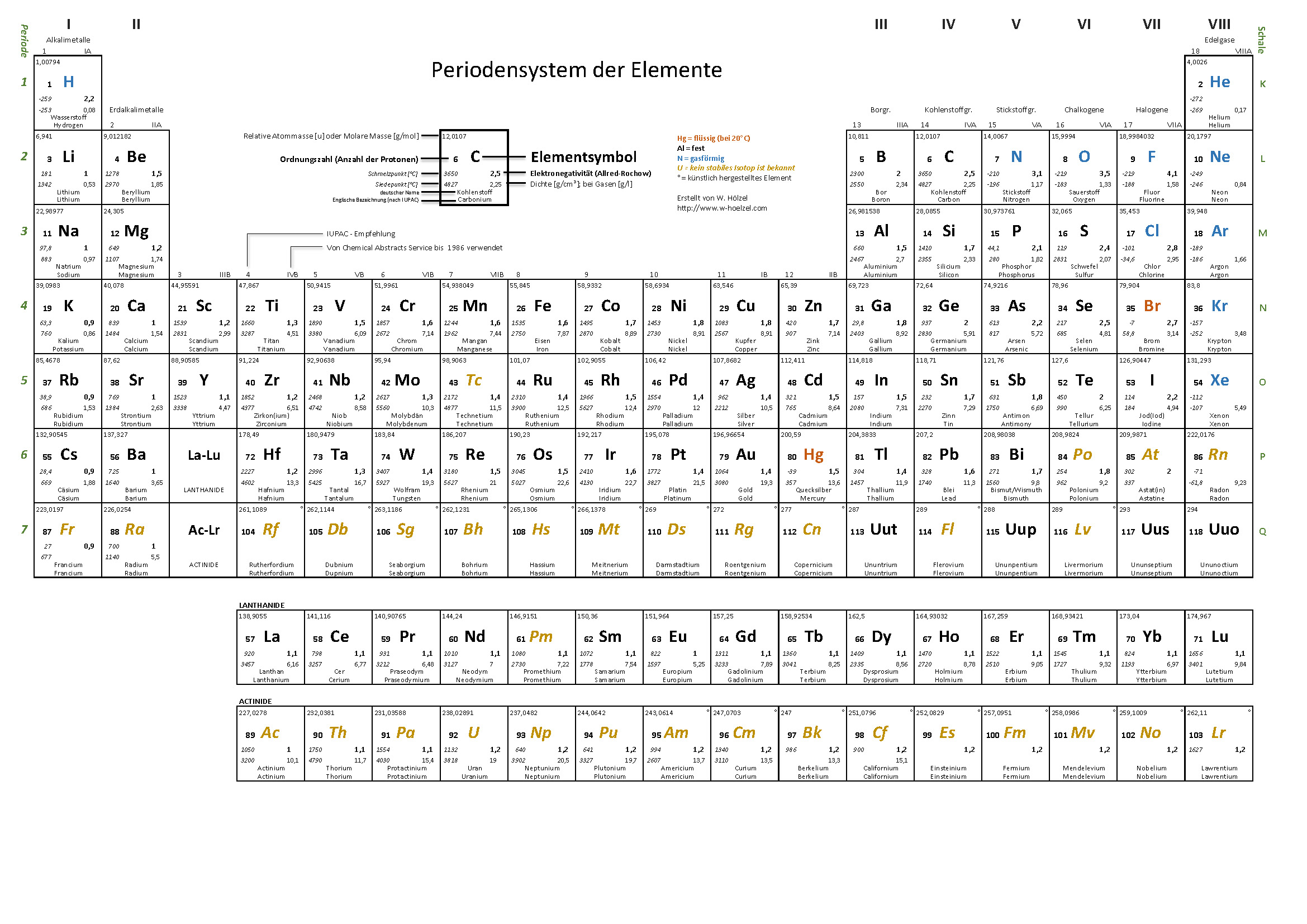
10. PSE – Farbkodierung für Eigenschaften
Visualisiert Schmelztemperatur, Siedetemperatur, Dichte und Elektronegativität mittels Farbkodierung.
- Elektronegativität [farbig]
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Aggregatzustand · Dichte [farbig]
- Schmelztemperatur [farbig] · Siedetemperatur [farbig]
Einige Beispiele weiterer Periodensysteme im Internet
- Zentrale Übersicht: https://de.wikipedia.org/wiki/Periodensystem
- Hervorragende Datensammlung: www.internetchemie.info
- Interaktives PSE mit Elektronenverteilung und Wikipedia-Links: www.ptable.com
- Interaktives PSE mit PSE-Ansichten: www.uniterra.de