Reaktionsmechanismus
-
01.8 Angriffsfreudige Teilchen
Was du auf dieser Seite lernst
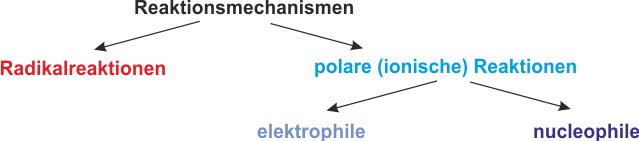
Chemische Reaktionen werden nach dem angreifenden Teilchen benannt. Du lernst drei Typen kennen: Radikale (Einzelelektronen), Elektrophile (Elektronenpaarlücke) und Nucleophile (freie Elektronenpaare). Diese Konzepte sind die Grundlage für alle Reaktionsmechanismen in der organischen Chemie.
Grundlagen aus der 9. Klasse
Freie Elektronenpaare und Strukturformeln von Molekülen hast du in der 9. Klasse behandelt:
→ Lewis-Formeln für Moleküle (Kl. 9) · → HNO-Regel (Kl. 9)1.8 Angriffsfreudige Teilchen
1.8.1 Teilchen mit Einzelelektronen: Radikale
Bsp.:
↑ Zum Vergrößern klicken
✕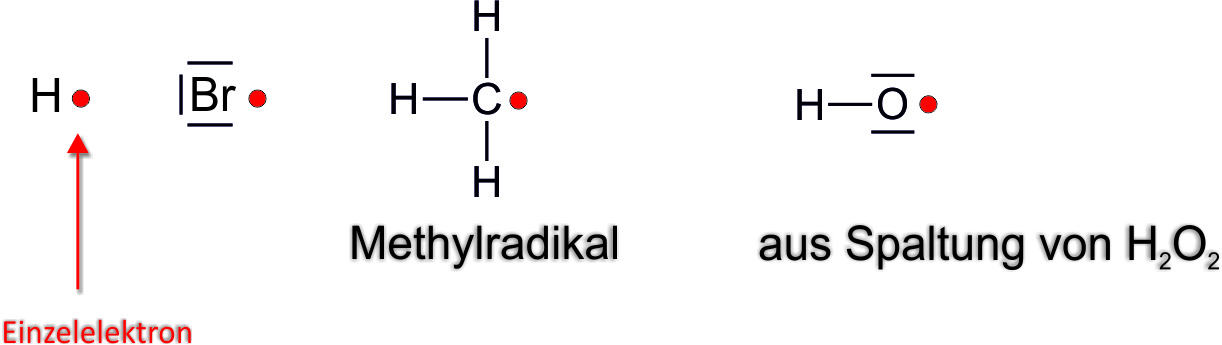
Radikale sind meist unbeständige Teilchen. Sie entstehen durch homolytische Spaltung (meist) unpolarer Bindungen unter Energiezufuhr (z. B. Wärme, Licht). Radikale sind sehr reaktionsfreudig und reagieren mit ihresgleichen oder mit Molekülen unter Neubildung von Radikalen.
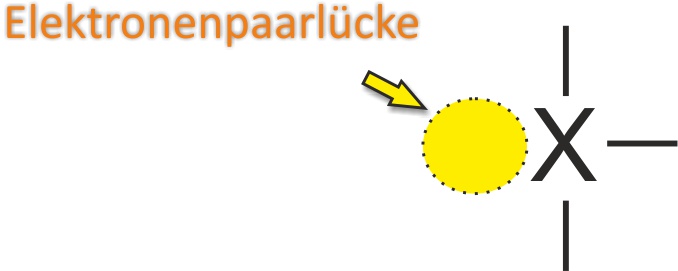
1.8.2 Teilchen mit Elektronenpaarlücke: Elektrophile Teilchen
Bsp.:
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕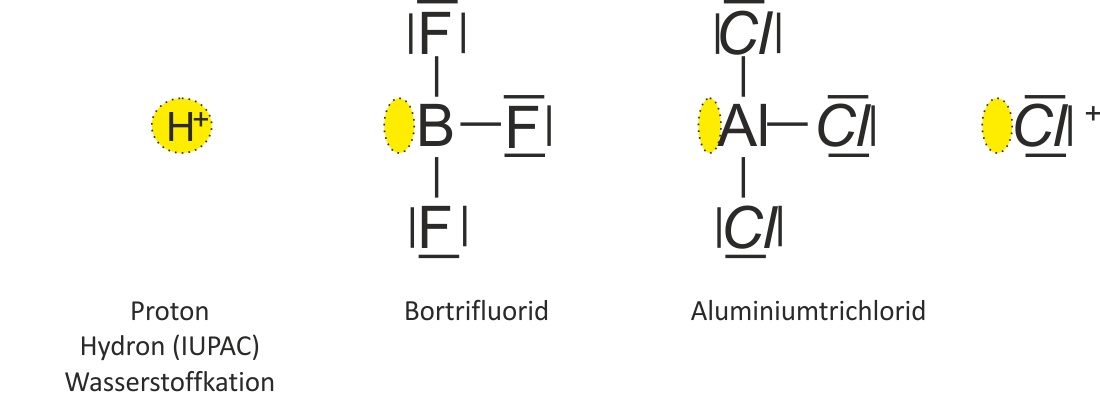
Elektrophile Teilchen sind sehr reaktionsfreudige Teilchen; sie wollen sich an ein freies Elektronenpaar anlagern (= Lewis-Säuren – für die Universität).
1.8.3 Teilchen mit freien Elektronenpaaren: Nucleophile Teilchen oder Basen
Bsp.:
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕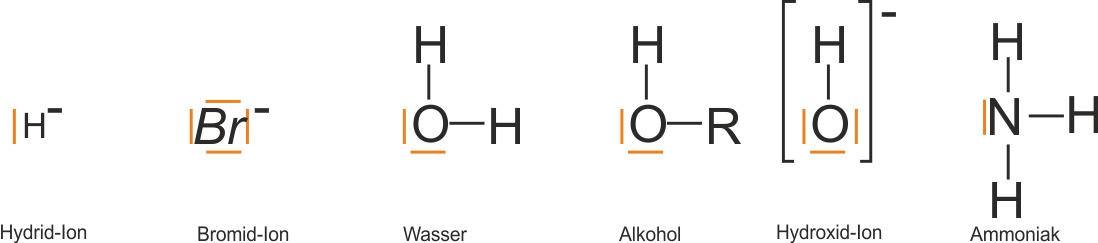
a) Nucleophile wollen positiv geladene oder positivierte Teilchen anlagern:
- als Basen: Protonen
- als nucleophile Teilchen (Lewis-Basen): andere Teilchen mit Elektronenpaarlücke (elektrophile Teilchen)
b) Basizität und Nucleophilie verlaufen annähernd parallel
- so ist z. B. das Hydroxid-Ion stärker basisch und stärker nucleophil als Wasser
- Basizität und Nucleophilie sind von der Zahl der freien Elektronenpaare unabhängig!
Zusammenfassung:
- Reaktionen werden nach der Funktion der angreifenden Teilchen benannt.
- Als Angreifer wird i. a. das kleinere Teilchen bezeichnet.
↑ Zum Vergrößern klicken
✕
Auf einen Blick – die wichtigsten Aussagen
RADIKALE
Teilchen mit einem ungepaarten Elektron. Entstehen durch homolytische Spaltung unter Energiezufuhr. Sehr reaktiv.
ELEKTROPHILE
Teilchen mit Elektronenpaarlücke. Suchen freie Elektronenpaare (= Lewis-Säuren). Bsp.: H⁺, BF₃, AlCl₃.
NUCLEOPHILE
Teilchen mit freien Elektronenpaaren. Greifen elektrophile Zentren an (= Lewis-Basen). Bsp.: OH⁻, NH₃, H₂O.
REAKTIONSNAME
Der Name einer Reaktion folgt dem angreifenden Teilchen: radikalisch · elektrophil · nucleophil.
Häufige Fragen – Angriffsfreudige Teilchen
Was ist ein Radikal und wie entsteht es?
Ein Radikal ist ein Teilchen mit einem ungepaarten Elektron (Einzelelektron). Radikale entstehen durch homolytische (symmetrische) Spaltung einer kovalenten Bindung: Dabei erhält jeder Bindungspartner genau eines der beiden Bindungselektronen. Dies geschieht unter starker Energiezufuhr – etwa durch UV-Licht oder hohe Temperaturen. Radikale sind meist kurzlebig und sehr reaktionsfreudig, weil das Einzelelektron nach einem Bindungspartner „sucht".
Was ist der Unterschied zwischen einem Elektrophil und einem Nucleophil?
Ein Elektrophil hat eine Elektronenpaarlücke – es ist elektronenarm und sucht ein freies Elektronenpaar (= Lewis-Säure). Ein Nucleophil hat freie Elektronenpaare – es ist elektronenreich und greift elektronenärmere Zentren an (= Lewis-Base). Elektrophile und Nucleophile sind komplementäre Partner: Der Nucleophil spendet sein Elektronenpaar an die Lücke des Elektrophils.
Warum sind Radikale so reaktionsfreudig?
Radikale besitzen ein ungepaart vorliegendes Elektron, das energetisch ungünstig ist. Das Radikal strebt danach, eine stabile Elektronenpaarung zu erreichen. Es reagiert deshalb sofort mit verfügbaren Molekülen oder anderen Radikalen. Bei der Reaktion mit einem Molekül entsteht häufig ein neues Radikal – dies führt zu einer Kettenreaktion, wie sie bei der radikalischen Substitution der Alkane auftritt. Mehr dazu: → Radikalische Substitution.
Was haben Nucleophile und Brønsted-Basen gemeinsam?
Beide besitzen freie Elektronenpaare. Eine Brønsted-Base nimmt ein Proton (H⁺) auf – dazu braucht sie ein freies Elektronenpaar. Ein Nucleophil greift allgemein elektronenärmere Teilchen an. Basizität und Nucleophilie verlaufen daher annähernd parallel: Das Hydroxid-Ion (OH⁻) ist sowohl stärker basisch als auch stärker nucleophil als Wasser (H₂O). Entscheidend ist aber nicht die Anzahl der freien Elektronenpaare, sondern deren Verfügbarkeit (Polarisierbarkeit).
Was versteht man unter Lewis-Säure und Lewis-Base?
Das Lewis-Konzept ist eine Erweiterung des Brønsted-Konzepts und gilt für die Universität: Eine Lewis-Säure ist ein Elektronenpaarakzeptor (= Elektrophil) – sie nimmt ein Elektronenpaar auf. Eine Lewis-Base ist ein Elektronenpaardonor (= Nucleophil) – sie stellt ein Elektronenpaar zur Verfügung. Das Lewis-Konzept ist weiter gefasst als das Brønsted-Konzept, da es keine Protonen benötigt: BF₃ ist eine Lewis-Säure, obwohl es kein Proton abgeben kann. Mehr zur Säure-Base-Theorie: → Brønsted-Definition (Kl. 9).
Lernkarten – Angriffsfreudige Teilchen
Klicke auf eine Karte, um die Antwort zu sehen.
1Was kennzeichnet ein Radikal? Wie entsteht es?
Ein Radikal hat ein ungepaart vorliegendes Elektron. Es entsteht durch homolytische Spaltung einer Bindung unter Energiezufuhr (Wärme, UV-Licht).
2Was ist ein Elektrophil? Nenne zwei Beispiele.
Elektrophil = Teilchen mit Elektronenpaarlücke; sucht freie Elektronenpaare (Lewis-Säure). Bsp.: H⁺, BF₃, AlCl₃.
3Was ist ein Nucleophil? Nenne zwei Beispiele.
Nucleophil = Teilchen mit freiem Elektronenpaar; greift elektronenärmere Zentren an (Lewis-Base). Bsp.: OH⁻, NH₃, H₂O.
4Wie heißt eine Reaktion, bei der ein Nucleophil angreift?
Nucleophile Reaktion (z. B. nucleophile Substitution SN). Reaktionen werden nach dem angreifenden Teilchen benannt – das ist i. d. R. das kleinere.
5Ordne zu: H⁺ · OH⁻ · Cl• – Radikal, Elektrophil oder Nucleophil?
H⁺ → Elektrophil (Elektronenpaarlücke)
OH⁻ → Nucleophil (freies Elektronenpaar)
Cl• → Radikal (Einzelelektron)Weiter im Kapitel Alkane
← 1.7 Eigenschaften der Alkane → 1.9 Radikalische Substitution
🔁 Grundlagen: Lewis-Formeln (Kl. 9) · Brønsted-Definition (Kl. 9)
-
01.9 Reaktion von Alkanen mit Halogenen
Was du auf dieser Seite lernst
Alkane reagieren unter Lichtzufuhr mit Halogenen in einer radikalischen Substitution (SR): Ein Wasserstoff-Atom wird durch ein Halogen-Atom ersetzt. Du lernst den dreistufigen Reaktionsmechanismus kennen und erfährst, welche Eigenschaften die entstehenden Halogenalkane haben.
Grundlagen – Angriffsfreudige Teilchen
Radikale und die homolytische Bindungsspaltung hast du auf der vorherigen Seite kennengelernt:
→ 1.8 Angriffsfreudige Teilchen · → 1.7 Eigenschaften der Alkane1.9 Reaktion von Alkanen mit Halogenen
1.9.1 Versuch
Experiment:
Gemisch aus 4 ml Isooctan (2,2,4-Trimethylpentan) und 1,3 ml Brom werden belichtet.
An das entstehende Gas wird …- … Flasche mit konz. Ammoniak
- … feuchtes pH-Papier
… gehalten.
Es entstehen:
a) ein farbloses Gas:
- Nebelbildung an feuchter Luft (HBr);
- mit Ammoniak bildet sich ein weißer Rauch (Ammoniak und der Stoff reagiert zu einem porösen Salz (NH4Br));
- angefeuchtetes Indikatorpapier färbt sich rot (Säure muss entstanden sein → HBr).
→ Die Beobachtungen sprechen dafür, dass das farblose Gas Bromwasserstoff (HBr) ist.
b) eine Flüssigkeit:
- größere Dichte als Wasser;
- Beilsteinprobe positiv (Beilsteinprobe: halogenhaltige Verbindungen ergeben mit Kupfer in der Flamme eine Grünfärbung).
→ Die Flüssigkeit ist ein Bromalkan (hauptsächlich).
1.9.2 Reaktionsschema
Alkan + Brom —(Belichtung)→ Bromalkan + Bromwasserstoff
Allgemein:
Alkan + Halogen —(Belichtung)→ Halogenalkan + Halogenwasserstoff1.9.3 Reaktionsmechanismus
(vereinfacht: statt Isooctan wird Methan verwendet)
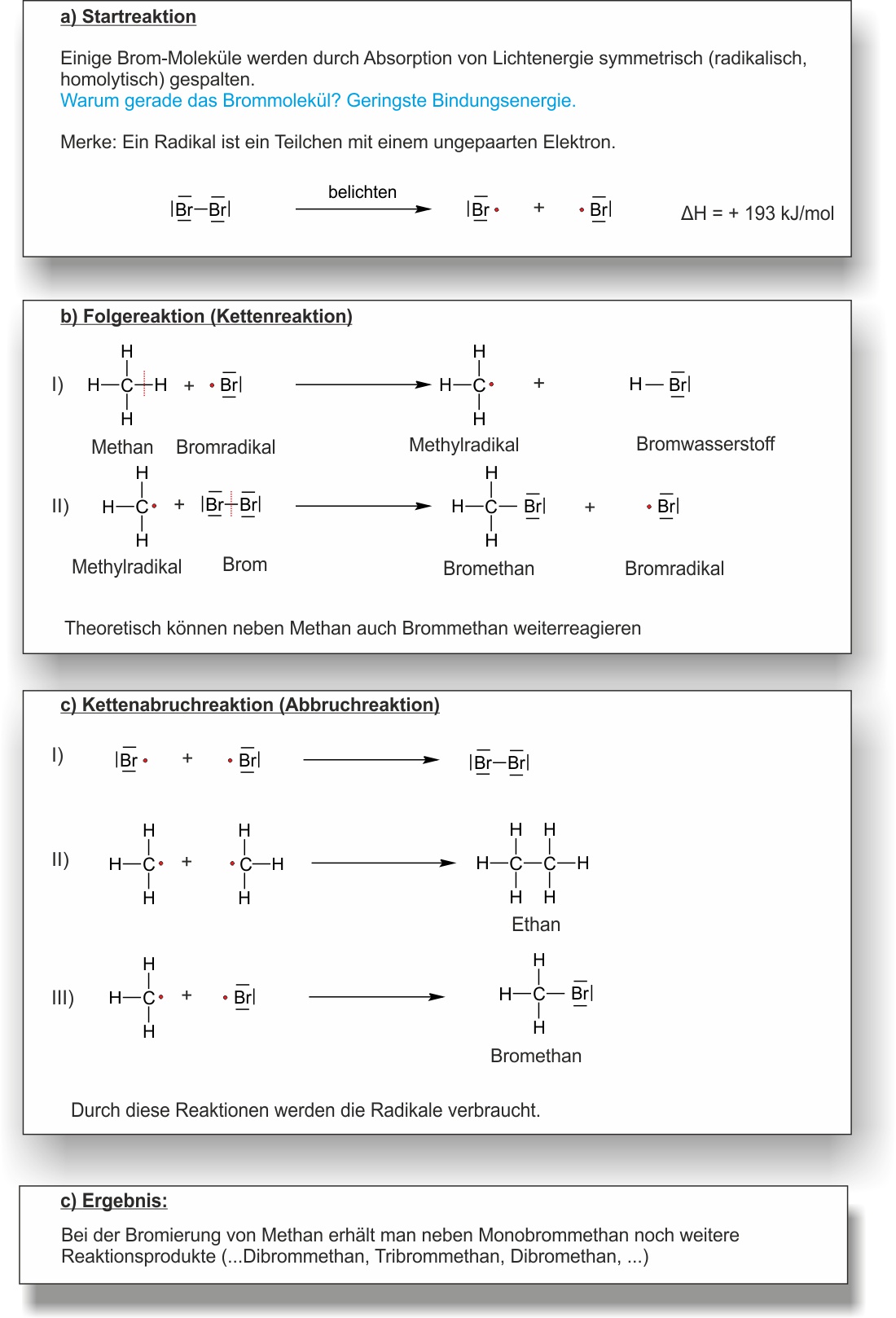
Folgende Abbildung zeigt den Reaktionsmechanismus der radikalischen Substitutionsreaktion zu einem Halogenalkan unter Bildung eines Halogenwasserstoffs.
↑ Zum Vergrößern klicken
✕
Merke
Reaktionen, bei denen Atome oder Atomgruppen einer Verbindung durch andere Atome ersetzt werden, bezeichnet man als Substitution.
Die Bromierung von Methan ist eine radikalische Substitution (SR-Reaktion).1.9.4 Halogenalkane
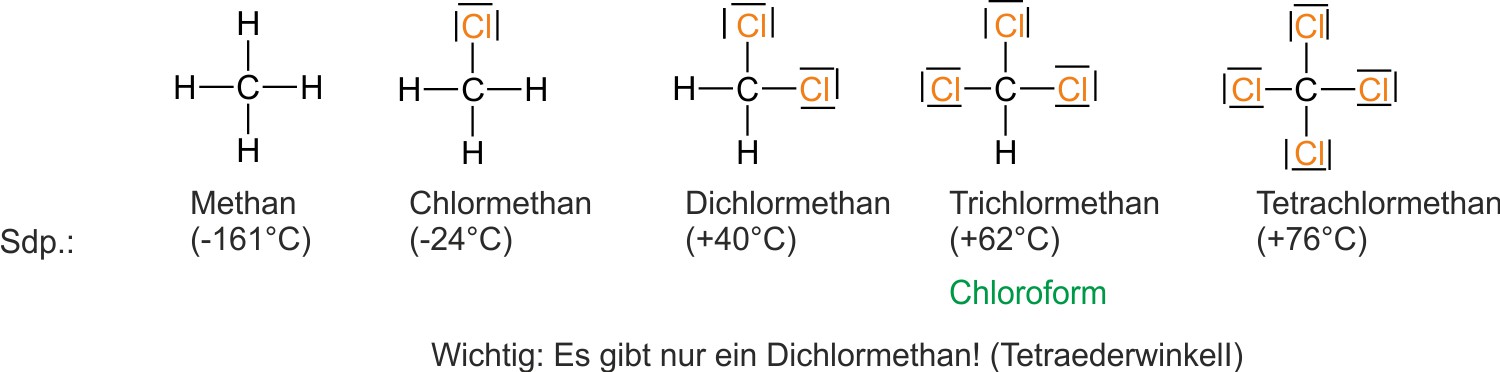
a) Halogenalkane sind Derivate (Abkömmlinge) der Alkane.
↑ Zum Vergrößern klicken
✕
b) Eigenschaften der Halogenalkane:
Löslichkeit Halogenalkane sind in Wasser unlöslich.
Sie sind sehr gute Lösungsmittel für Alkane und Fette (hydrophobe Stoffe).Dichte Halogenalkane haben meistens eine größere Dichte als 1 g/cm³. Siedetemperatur Sie liegt bei Halogenalkanen höher als bei vergleichbaren Alkanen (Grund: größere van-der-Waals-Kräfte). Brennbarkeit Je mehr H-Atome durch Halogen-Atome ersetzt sind, umso schlechter ist die Brennbarkeit der Halogenalkane. c) Verwendung:
- hervorragende Lösungsmittel (Extraktion pflanzlicher Öle, Entfetten von Metallteilen, chemische Reinigung …)
- Treibgase in Sprays
- Kältemittel für Kühlanlagen
- Feuerlöschmittel (Halon, Bromtrifluormethan)
- Desinfektionsmittel (Jodoform, Trijodmethan)
- Insektizide (Lindan, Hexachlorcyclohexan)
Auf einen Blick – die wichtigsten Aussagen
STARTREAKTION
Licht spaltet Br₂ homolytisch → zwei Br-Radikale (Br•). Energiezufuhr notwendig, läuft nur einmal ab.
KETTENREAKTION
Br• + CH₄ → HBr + CH₃• · CH₃• + Br₂ → CH₃Br + Br• · Das Radikal regeneriert sich ständig → Kettenreaktion.
ABBRUCH
Zwei Radikale rekombinieren → stabile Verbindung. Kette bricht ab, wenn Radikale aufeinandertreffen.
HALOGENALKANE
Dichte > 1 g/cm³ · in Wasser unlöslich · höherer Sdp. als Alkane · weniger brennbar je mehr Halogenatome.
Häufige Fragen – Radikalische Substitution und Halogenalkane
Was ist eine radikalische Substitution (SR)?
Bei einer Substitution wird ein Atom oder eine Atomgruppe in einem Molekül durch ein anderes Atom ersetzt. Bei der radikalischen Substitution (SR) übernehmen Radikale die Angreiferrolle. Bei der Bromierung von Methan wird ein H-Atom durch ein Br-Atom ersetzt: CH₄ + Br₂ → CH₃Br + HBr. Die Reaktion läuft als Kettenreaktion in drei Stufen ab: Startreaktion, Kettenreaktion, Abbruchreaktion.
Warum wird für die Bromierung von Alkanen Licht benötigt?
Die Reaktion beginnt mit der Startreaktion: Licht (hν) liefert die nötige Energie, um die Br–Br-Bindung homolytisch zu spalten – jedes Br-Atom erhält ein Elektron und wird zum Radikal (Br•). Diese Br-Radikale lösen die Kettenreaktion aus. Ohne Lichtzufuhr findet keine Startreaktion statt, und die Gesamtreaktion kommt nicht in Gang.
Welche drei Schritte hat der Reaktionsmechanismus der SR?
1. Startreaktion: Br₂ →(hν)→ 2 Br• (einmalig, braucht Energie).
2. Kettenreaktion (läuft sehr oft ab):
Br• + CH₄ → HBr + CH₃• (Br-Radikal zieht H ab)
CH₃• + Br₂ → CH₃Br + Br• (Methyl-Radikal greift Br₂ an, neues Br• entsteht)
3. Abbruchreaktion: Zwei Radikale rekombinieren, z. B. CH₃• + Br• → CH₃Br. Die Kette bricht ab.Warum haben Halogenalkane einen höheren Siedepunkt als vergleichbare Alkane?
Halogenatome sind größer und polarisierbarer als Wasserstoff-Atome. Dadurch sind die van-der-Waals-Kräfte zwischen Halogenalkanmolekülen stärker als zwischen reinen Alkanmolekülen gleicher Kettenlänge. Stärkere ZMK bedeuten mehr Energie zum Verdampfen → höherer Siedepunkt. Zusätzlich besitzen C–X-Bindungen (X = Halogen) einen Dipolcharakter, der weitere Anziehungskräfte beiträgt.
Was ist die Beilsteinprobe und was zeigt sie an?
Die Beilsteinprobe ist ein einfacher Nachweis für halogenhaltige organische Verbindungen. Dazu wird ein Kupferdraht in der Flamme erhitzt und dann kurz in die Probe getaucht. Enthält die Substanz Halogene (Cl, Br, I), färbt sich die Flamme charakteristisch grün (durch Kupferhalogenid-Verbindungen). Beim Versuch in 1.9.1 wurde so bestätigt, dass die entstandene Flüssigkeit ein Bromalkan ist.
Lernkarten – Radikalische Substitution
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist eine Substitution? Was bedeutet „radikalisch"?
Substitution: Ein Atom/Gruppe wird durch ein anderes ersetzt. Radikalisch: Der Angreifer ist ein Radikal (Einzelelektron).
2Nenne die drei Stufen der SR-Reaktion.
1. Startreaktion (Br₂ + hν → 2 Br•)
2. Kettenreaktion (Radikale reagieren, neues Radikal entsteht)
3. Abbruchreaktion (zwei Radikale rekombinieren)3Welche Produkte entstehen bei der Bromierung von Methan?
CH₄ + Br₂ →(hν)→ CH₃Br (Brommethan) + HBr (Bromwasserstoff).
4Nenne zwei Unterschiede zwischen Halogenalkanen und Alkanen.
1. Dichte > 1 g/cm³ (Alkane < 1).
2. Höherer Siedepunkt (stärkere vdW-Kräfte).
3. In Wasser unlöslich, aber gutes Lösungsmittel für Fette.5Methan wird zweifach bromiert. Nenne Produkt und systematischen Namen.
CH₄ + 2 Br₂ →(hν)→ CH₂Br₂ + 2 HBr
Name: Dibrommethan (Di- für zwei Br-Atome, Stamm Methan).Weiter in der Organischen Chemie
← 1.8 Angriffsfreudige Teilchen → 2.1 Ethen – Alkene
🔁 Grundlagen: Eigenschaften der Alkane (Kl. 10) · Radikale & Elektrophile (Kl. 10)
