Kondensationsreaktion
-
04.1.7 Glycosid- bzw. Vollacetalbildung
zu 4.1.7 Reaktionen der Monosaccharide
Glycosidbildung (~Halbacetal, Vollacetal)
a) Aldehyd + Alkohol ⇌ Halbacetal (nucleophile Addition)
b) Halbacetal + Alkohol ⇌ (Voll)Acetal + WasserTypische Kondensationsreaktion (unter Wasserabspaltung)
Beispiel:
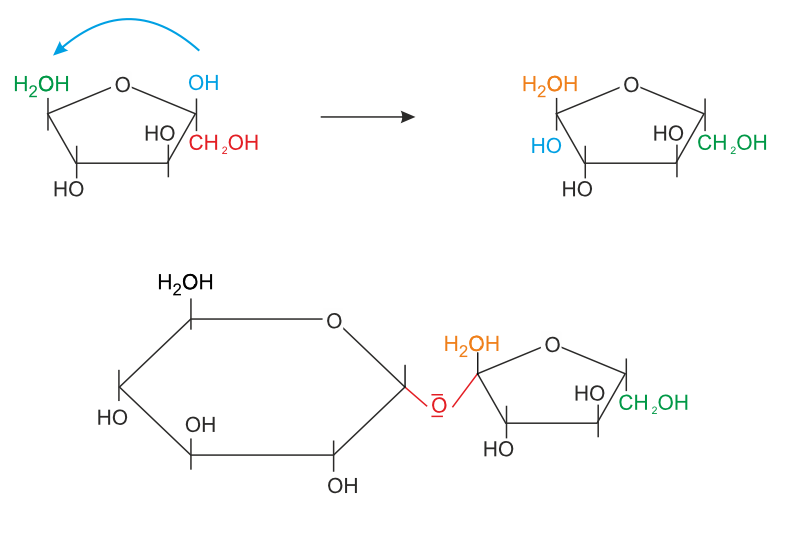
β-D-Glucose + Methanol ⇌ β-Methyl-Glucosid + Wasser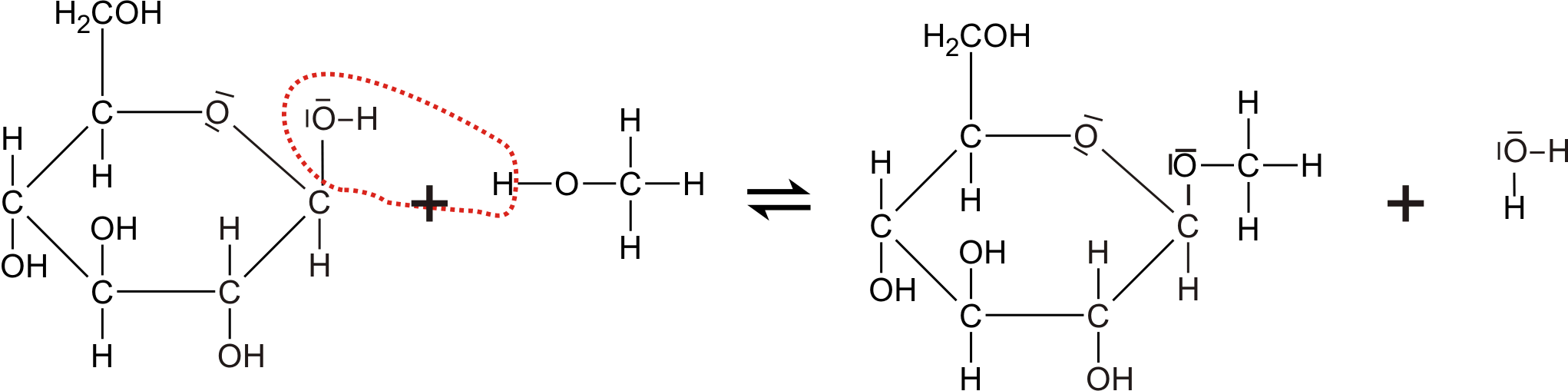
Zucker + Alkohol ⇌ Glycosid + Wasser
Fructose + Alkohol ⇌ Fructosid + Wasser
Glucose + Alkohol ⇌ Glucosid + Wasser
Reaktionen von Zuckern untereinander ergeben Di-, Oligo- und Polysaccharide. -
04.2 Disaccharide
4.2 Disaccharide
4.2.1 Maltose (Malzzucker)
Vorkommen: Entsteht durch unvollständige Hydrolyse von Stärke .
Stärke -----(Enzym: Amylase)-----> MaltoseVerwendung: Gerstenmalz (Bier brauen)
Eigenschaften:
- Fehling positiv
- zeigt Mutarotation
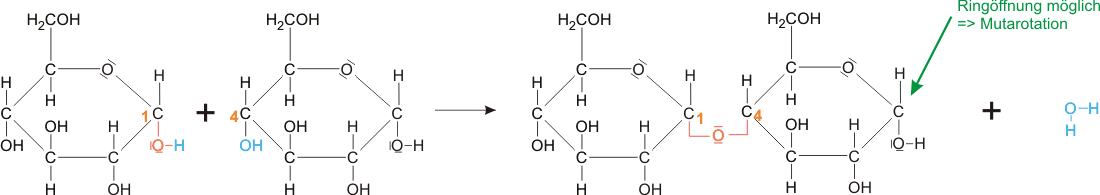
- besteht aus 2 α-D-Glucoseeinheiten, α-1→4 glycosidisch verknüpft.
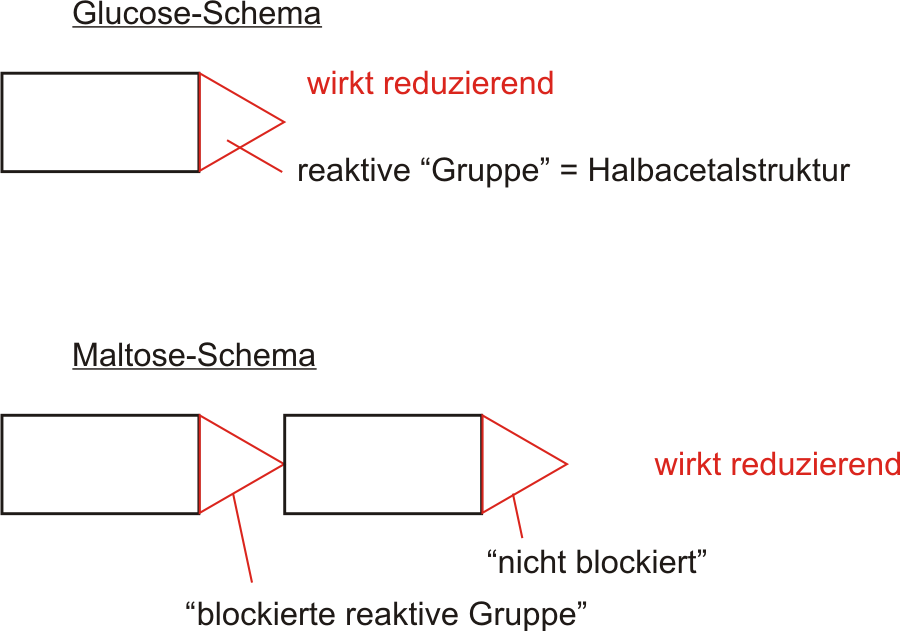
4.2.2 CellobioseVorkommen: Verdauungsprodukt von Pflanzenfressern aus Zellulose
Eigenschaften:
- Fehling positiv
- zeigt Mutarotation
- besteht aus 2 β-D-Glucoseeinheiten, β 1 → 4 glycosidisch verknüpft.
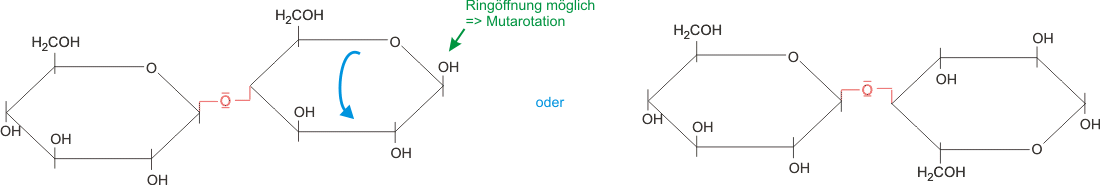
4.2.3 Lactose (Milchzucker)
Vorkommen: Muttermilch von Säugetiere (1,5 – 8 %)
Eigenschaften:- Fehling positiv
- zeigt Mutarotation
Hydrolyse ergibt β-D-Glucose und β-D-Galactose, β-1 → 4 glycosidisch verknüpft.
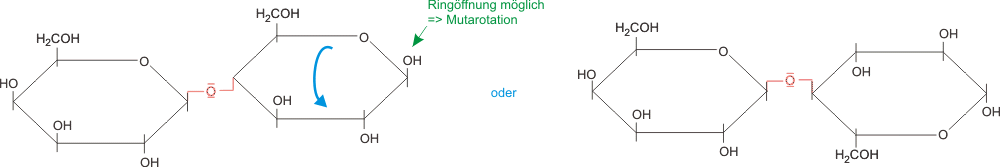
-
04.2.4 Saccharose
4.2.4 Saccharose (Rohr- oder Rübenzucker)
Vorkommen: Haushaltszucker, Kristallzucker, Zuckerrüben (18-20%), Zuckerrohr (16-22%)
Summenformel: C12H22O11 → Dissaccharide (2 Moleküle Monosaccharid minus 1 Molekül Wasser)
Physikalische Eigenschaften:
- hoher Schmelzpunkt (ca. 180°C)
- harte Kristalle
Folgerung:
- Molekülgitter mit vielen H-Brückenbindungen
- sehr leicht löslich in Wasser
- eine Rohrzuckerlösung ist zähflüssig → viele Wasserstoffbrücken
Chemische Eigenschaften:
- Fehling negativ
- zeigt keine Mutarotation
Schülerexperiment: Nach einer Hydrolyse mit verdünnter Salzsäure:
- Fehling positiv
- Saccharose besteht aus α-D-Glucose und β-D-Fructose
- Beide Monosaccharide sind α-1→2-glycosidisch verknüpft
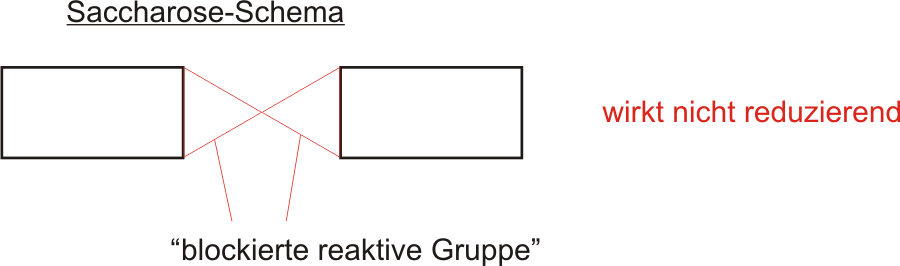
Spaltung der Saccharose mit verdünnter Salzsäure = saure Hydrolyse
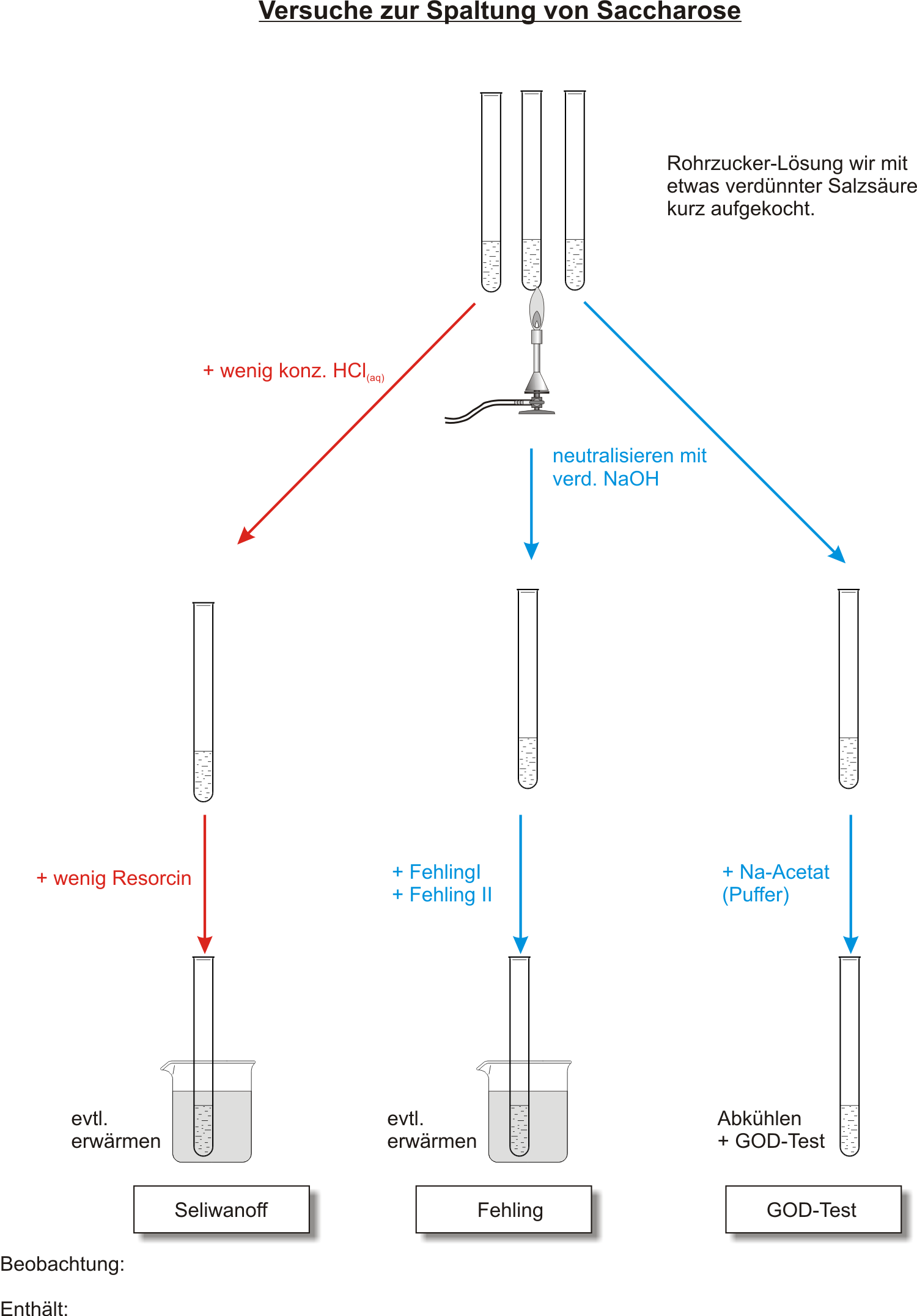
färbt sich rosa roter Niederschlag positiv
enthält Fructose Aldehydgruppe Glucose

Unter Hydrolyse versteht man einen Vorgang, bei dem Atombindungen unter Aufnahme von Wasser gespalten werden (Bsp. Esterspaltungen).
Wichtig: die leichte Hydrolisierbarkeit spricht für eine Verknüpfung über Sauerstoff.
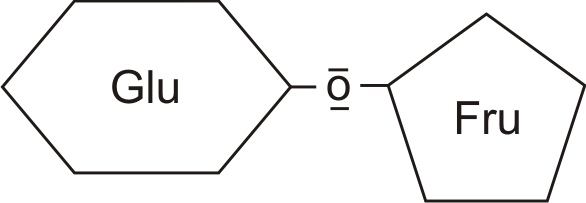
4.2.5 Invertzucker
Saccharose dreht die Ebene des polarisierten Lichts nach rechts. Während der Hydrolyse (durch verdünnte Salzsäure oder Ferment/Enzym Invertase) nimmt die Drehung fortwährend ab und geht in eine Linksdrehung über:
Saccharose + Wasser → D-Glucose + D-Fructose
+66° + 0° + 54,7 - 92,4
Zahlenwerte αsp in ml/(g • dm)
Man bezeichnet daher diese Spaltung als Inversion des Rohrzuckers und das entstehende Gemisch als Invertzucker.
Inversion: Vorzeichenwechsel der optischen Aktivität im Verlauf einer Reaktion optisch aktiver Verbindungen. -
04.3 Polysaccharide-amylose
5.4.3 Polysaccharide
- Wichtigsten Beispiele: Stärke, Glykogen (tier. Stärke), Cellulose
- Funktion: Speicher- und Gerüstsubstanz
- Monomere der genannten Beispiele: Glucose; unterschiedl. Verknüpfung
4.3.1 Stärke
a) Vorkommen:
- Pflanzen (Speicherstoff, osmotisch nicht wirksam)
- Nahrungsmittel (Brot, Teigwaren, Kartoffel, usw.),
b) Aufbau eines Stärkemoleküls:
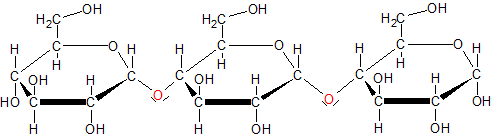
c) Bau: α-D-Glucose – StärkekornAmyolse Amylopektin Anteil: (10-30%) (70-90%) Bau: linearen Ketten (helikaler
(Schrauben-)Struktur)
stark verzweigten Strukturen Verknüpfung α-1,4-glykosidisch α-1,4-glykosidischen
α-1,6-glykosidischenLöslichkeit in heißem Wasser kolloidal löslich unlöslich Mit I2 bildet es __ Lösung blaue violette Im Stärkekorn Hülle Innen
d) Nachweis: Iodstärke-Reaktion
Versuch: Zu einer Stärkelösung gibt man ein paar Tropfen einer Lösung von Iod in Kaliumiodid (Iod-Kaliumiodid-Lösung, Lugolsche Lösung) Elementares Iod ist in Wasser kaum löslich. Liegen jedoch schon gelöste Iodid-Ionen vor, löst sich das Iod unter Bildung von Polyiodidionen:2 I2 + I- → I3- + I2 → I5-
Beobachtung: Lösung wird tiefblau
Beim Erhitzen wird die Lösung hell, beim Abkühlen wieder tiefblau
Erklärung: Die Stärkemoleküle sind spiralig angeordnet, in den entstehenden Hohlraum lagern sich Jodmoleküle ein die dort durch van-der-Waals-Kräfte gebunden werden. Eine blaue Iod-Stärke-Einlagerungsverbindung bildet sich. Das gelbe Licht wird absorbiert, die Lösung erscheint blau. Beim Erhitzen nimmt die Beweglichkeit der I2-Moleküle zu, so dass beim Erhitzen eine Entfärbung eintritt.Eigenschaften von Stärke (Amylose)
- in kaltem Wasser: unlöslich
- heißem Wasser: löslich
- schmeckt nicht süß
- kolloide Lösung (Kolloide: Moleküle oder Aggregate, die sich aus etw. 103 bis 109 Atomen zusammensetzt und in einem Dispersionsmittel verteilt sind).
Versuch:
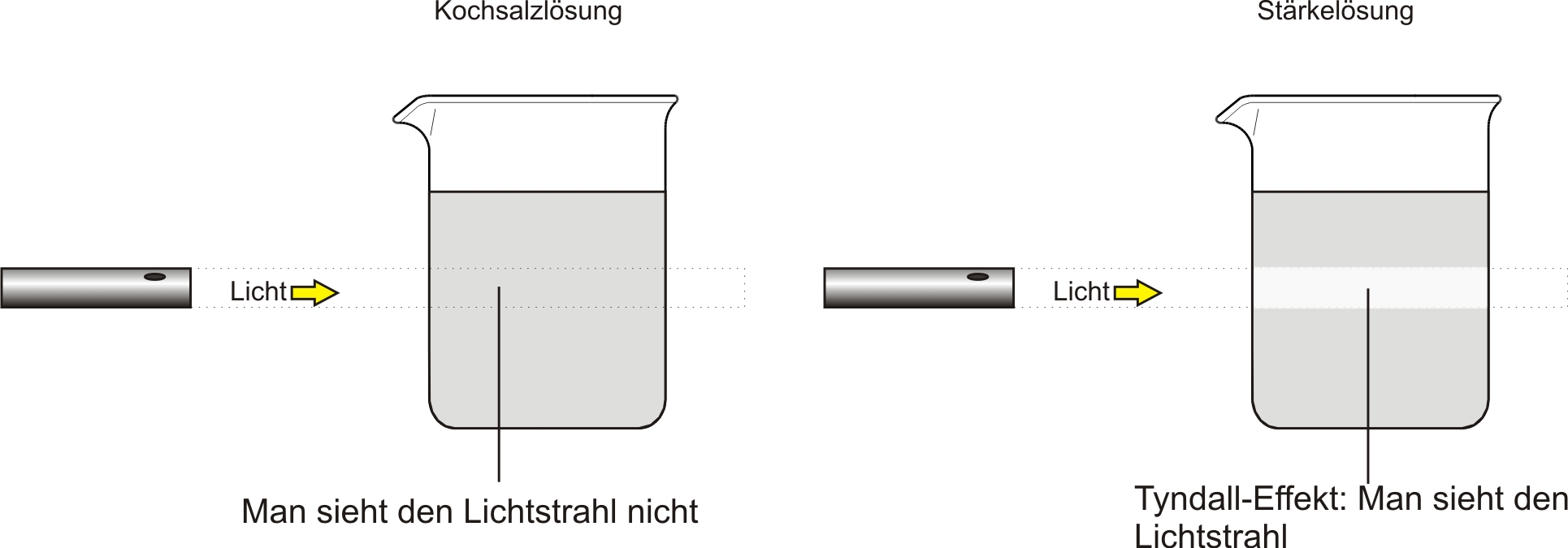
Beobachtung:
Im Gegensatz zu NaCl-Lösung ist der Verlauf des Lichtes in der Stärkelösung sichtbar (= Tyndall-Effekt).
Erklärung:
Gebündeltes Licht wird beim Durchgang durch kolloid- oder molekulardisperse Systeme gestreut (d.H. jedes Teilchen streut einen Teil des auftreffenden Lichtes in alle Richtungen des Raums. Dieser von Tyndall 1868 erstmals untersuchte Effekt tritt immer dann auf, wenn Teilchen vorliegen, deren Größe etwa der Wellenlänge des Lichtes entsprechen. Solche Teilchen haben einen Durchmesser von 1 bis 1000 nm.van-der-Waals-Kräfte/strong
-
2.5 Estergleichgewicht
Was du auf dieser Seite lernst
Du lernst, wie Carbonsäuren und Alkohole in einer Kondensationsreaktion zu Estern und Wasser reagieren. Am Beispiel des Estergleichgewichts (Essigsäure + Ethanol) wird deutlich, dass sowohl Hin- als auch Rückreaktion zum gleichen Endzustand führen – ein klassisches Beispiel für ein chemisches Gleichgewicht.
Grundlagen aus der 10. Klasse
Die Grundlagen zu Carbonsäuren und Alkoholen hast du bereits in der 10. Klasse kennengelernt:
→ Essigsäure / Ethansäure (Kl. 10) · → Alkohole / Alkanole (Kl. 10)2.5 Estergleichgewicht
Allgemeine Reaktion
Carbonsäure + Alkohol ⇌ Ester + Wasser
Wer sich an die 10. Klasse erinnern kann, kann ja mal versuchen, die Reaktionsgleichung für Ethansäure und Ethanol zu formulieren.
Tipp 1: Es handelt sich um eine Kondensationsreaktion – zwei Moleküle verbinden sich unter Abspaltung eines kleinen Moleküls (hier: Wasser).
Tipp 2: Es reagieren meist die funktionellen Gruppen miteinander und selten die Alkylgruppen.
Allgemeine Reaktionsgleichung (Summenformeln)
R–COOH + R'–OH ⇌ R–COO–R' + H2O
Carbonsäure + Alkohol ⇌ Ester + Wasser | Katalysator: H+ (z. B. konz. H2SO4)
✕Lösung: Reaktionsgleichung Ethansäure + Ethanol
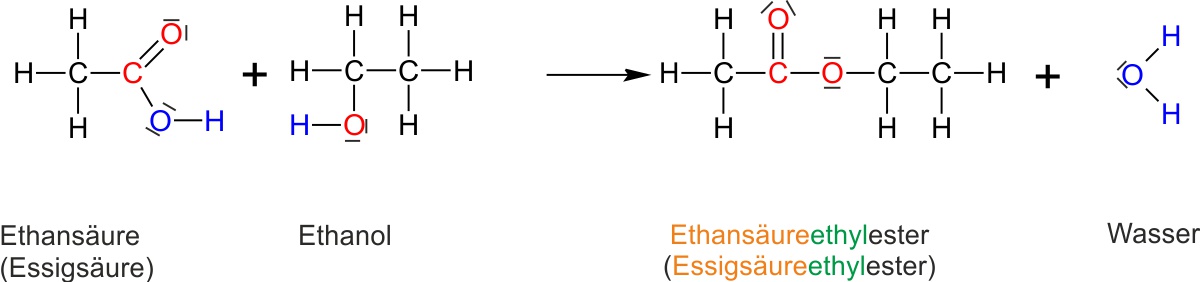
Mechanismus der Veresterung (säurekatalysiert)
Der Mechanismus der säurekatalysierten Veresterung verläuft in vier reversiblen Teilschritten. Der Katalysator (H+) wird am Ende wieder freigesetzt:
↑ Zum Vergrößern klicken
✕Die 4 Teilschritte in Kurzform
1. Protonierung der Carbonylfunktion der Carbonsäure → Carbokation
2. Nukleophiler Angriff des Alkohols (freies Elektronenpaar) → Oxoniumion
3. Protonenumlagerung → Wasserabspaltung → erneutes Carbokation
4. Protonenabspaltung (H+ wird regeneriert) → CarbonsäureesterAlle Teilschritte sind reversibel (⇌). Der H+-Katalysator beschleunigt die Reaktion, verschiebt aber das Gleichgewicht nicht.
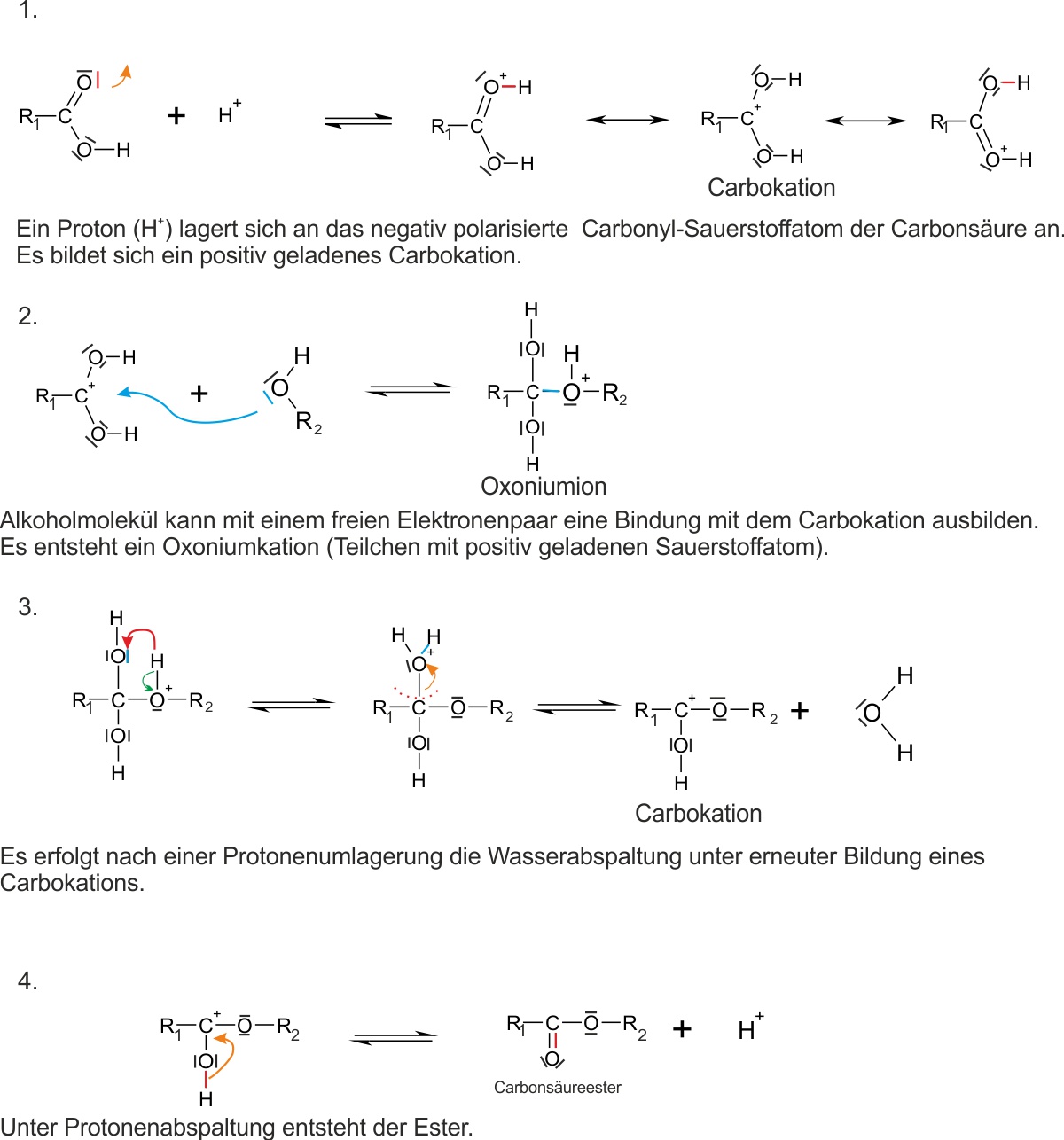
Das Estergleichgewicht – Nachweis durch zwei Versuchsansätze
Versuchsansatz 1 (Hinreaktion): Man gibt 1 mol Carbonsäure und 1 mol Alkohol zusammen.
Versuchsansatz 2 (Rückreaktion): Man gibt 1 mol Ester und 1 mol Wasser zusammen.Tipp: Was erwartest du?
Schau dir nochmals die Merkmale eines chemischen Gleichgewichts an. Ein echtes Gleichgewicht wird vom gleichen Endzustand aus erreicht – egal von welcher Seite man startet.
✕Lösung: Ergebnis des Experiments
Ergebnis: Man erhält in beiden Fällen denselben Endzustand.
↑ Zum Vergrößern klicken
Reaktionsgleichung und Mengenverhältnisse im Gleichgewicht
CH3COOH + C2H5OH ⇌ CH3COOC2H5 + H2O
Zeitpunkt n(CH3COOH) n(C2H5OH) n(Ester) n(H2O) Anfang 1 (Hinreaktion) 1 mol 1 mol 0 mol 0 mol Gleichgewicht ⅓ mol ⅓ mol ⅔ mol ⅔ mol Anfang 2 (Rückreaktion) 0 mol 0 mol 1 mol 1 mol 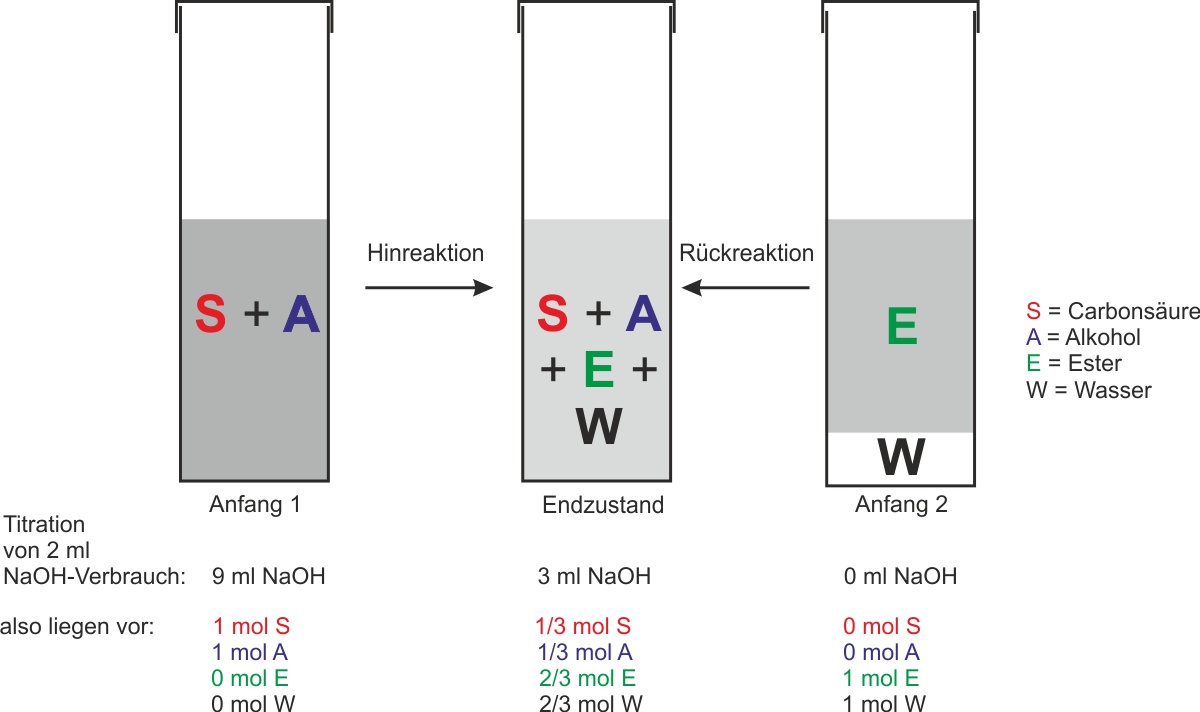
Quantitativer Nachweis: Titration der Carbonsäure
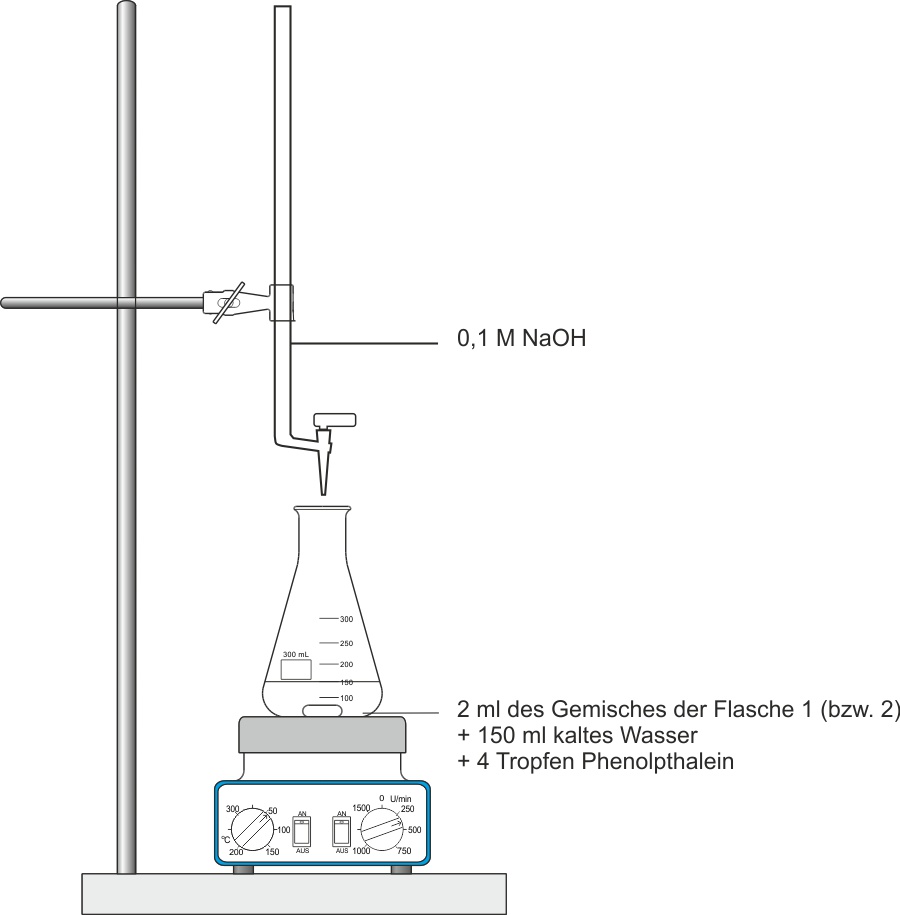
Man kann in beiden Versuchsansätzen die vorhandene Carbonsäuremenge durch quantitative Reaktion mit Natronlauge (Titration) messen.
Reaktionsgleichung der Titration (Summenformeln)
CH3COOH + NaOH → CH3COONa + H2O
Essigsäure reagiert vollständig und quantitativ mit NaOH. Mit 0,1 M NaOH und dem Verbrauch kann die Säuremenge berechnet werden: n(CH3COOH) = c(NaOH) · V(NaOH)
↑ Zum Vergrößern klicken
✕
Auf einen Blick – die wichtigsten Aussagen
KONDENSATIONSREAKTION
Bei der Veresterung verbinden sich Carbonsäure und Alkohol unter Abspaltung von Wasser – typische Kondensationsreaktion.
MECHANISMUS
4 reversible Schritte: Protonierung → Carbokation → Oxoniumion → Wasserabspaltung → Ester. H+ ist Katalysator.
GLEICHGEWICHT
Hin- und Rückreaktion erreichen denselben Endzustand: ⅔ mol Ester + ⅔ mol Wasser (aus je 1 mol Edukt).
TITRATION
Der Gleichgewichtszustand lässt sich quantitativ nachweisen: Die Carbonsäuremenge wird durch Titration mit NaOH bestimmt.
Häufige Fragen – Estergleichgewicht
Was ist eine Kondensationsreaktion und warum ist die Veresterung eine solche?
Bei einer Kondensationsreaktion verbinden sich zwei Moleküle unter Abspaltung eines kleinen Moleküls – hier Wasser. Bei der Veresterung reagiert die Carboxylgruppe (–COOH) der Carbonsäure mit der Hydroxylgruppe (–OH) des Alkohols: Beide funktionellen Gruppen treten miteinander in Wechselwirkung, und als Nebenprodukt entsteht ein Wassermolekül. Mehr zur Carboxylgruppe findest du auf der Seite Funktionelle Gruppe der Monocarbonsäuren (Kl. 10).
Wie läuft der Mechanismus der säurekatalysierten Veresterung ab?
Der Mechanismus verläuft in vier reversiblen Schritten: (1) Ein Proton (H+) lagert sich an das Carbonyl-Sauerstoffatom der Carbonsäure – es entsteht ein Carbokation. (2) Ein freies Elektronenpaar des Alkohols greift das Carbokation an – es bildet sich ein Oxoniumkation. (3) Nach einer Protonenumlagerung wird Wasser abgespalten und erneut ein Carbokation gebildet. (4) Durch Protonenabspaltung entsteht der fertige Ester, und H+ wird regeneriert.
Warum führen Hin- und Rückreaktion zum gleichen Endzustand?
Weil es sich um ein echtes chemisches Gleichgewicht handelt. Das Gleichgewicht wird dynamisch erreicht: Hin- und Rückreaktion laufen gleichzeitig ab, bis ihre Geschwindigkeiten gleich groß sind. Egal ob man mit 1 mol Carbonsäure + 1 mol Alkohol (Hinreaktion) oder mit 1 mol Ester + 1 mol Wasser (Rückreaktion) startet – der Endzustand ist identisch: ca. ⅔ mol Ester und ⅔ mol Wasser liegen neben ⅓ mol Carbonsäure und ⅓ mol Alkohol vor. Mehr zu den Merkmalen eines Gleichgewichts: Merkmale eines chemischen Gleichgewichts.
Wie kann man das Estergleichgewicht zugunsten des Esters verschieben?
Nach dem Prinzip von Le Chatelier kann das Gleichgewicht verschoben werden, indem man:
• einen der Reaktionspartner im Überschuss einsetzt (z. B. mehr Alkohol),
• ein Produkt laufend entzieht (z. B. Wasser durch Destillation oder mit einem Trockenmittel entfernt).
Hinweis: Ein Katalysator (konz. H2SO4) beschleunigt lediglich die Gleichgewichtseinstellung – er verschiebt das Gleichgewicht nicht.
Mehr dazu: Prinzip von Le Chatelier.Wie wird das Estergleichgewicht experimentell nachgewiesen?
Man misst quantitativ die verbliebene Carbonsäuremenge durch Titration mit Natronlauge (NaOH) und dem Indikator Phenolphthalein. Aus dem NaOH-Verbrauch lässt sich n(Carbonsäure) berechnen: n = c(NaOH) · V(NaOH). Beim Gleichgewichtsansatz verbraucht man nur noch ⅓ des ursprünglichen NaOH-Verbrauchs, was zeigt, dass ⅔ der Essigsäure abreagiert haben. Mehr zur Säure-Base-Titration: Säure-Base-Titration (Kursstufe).
Lernkarten – Estergleichgewicht
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist eine Kondensationsreaktion? Nenne ein Beispiel.
Zwei Moleküle verbinden sich unter Abspaltung eines kleinen Moleküls (z. B. H2O). Beispiel: Veresterung – Carbonsäure + Alkohol → Ester + Wasser.
2Welche Zwischenstufen entstehen im Mechanismus der säurekatalysierten Veresterung?
1. Carbokation (nach Protonierung der Carbonsäure)
2. Oxoniumkation (nach Angriff des Alkohols)
3. erneutes Carbokation (nach Wasserabspaltung)
→ Ester + H+ (regeneriert)3Was beweist das Estergleichgewicht-Experiment mit zwei Ansätzen?
Beide Ansätze (1 mol S + 1 mol A bzw. 1 mol E + 1 mol W) führen zum gleichen Endzustand – Beweis für ein echtes dynamisches Gleichgewicht.
4Nenne zwei Maßnahmen, um das Estergleichgewicht auf die Esterseite zu verschieben.
1. Überschuss eines Reaktionspartners (z. B. mehr Alkohol)
2. Entzug eines Produkts (z. B. Wasser abdestillieren oder binden)
→ Prinzip von Le Chatelier
Nicht geeignet: Katalysator – beschleunigt nur, verschiebt nicht.5Beim GG-Ansatz (1 mol CH3COOH + 1 mol C2H5OH) verbraucht die Titration von 2 ml Probe 3 ml NaOH (0,1 M). Wie viel mol Essigsäure sind noch vorhanden, wenn der Gesamtansatz 50 ml beträgt?
n(NaOH) pro 2 ml Probe = 0,003 l · 0,1 mol/l = 3·10−4 mol
→ Hochrechnung auf 50 ml: n(CH3COOH) = 3·10−4 · 25 = 7,5·10−3 mol ≈ ⅓ der Ausgangsmenge (erwartet: ⅓ mol)Weiter im Kapitel Gleichgewichtsreaktionen
← Merkmale eines chemischen Gleichgewichts → Schreibweise und Kollisionsmodell
🔁 Grundlagen aus Klasse 10: Essigsäure / Ethansäure (Kl. 10) · Alkohole / Alkanole (Kl. 10) · Funktionelle Gruppe der Monocarbonsäuren (Kl. 10)
⬇️ Weiter im Kapitel: Prinzip von Le Chatelier · Massenwirkungsgesetz · Ammoniaksynthese
-
2.6 Schreibweise und 2.7 Kollisionsmodell
Was du auf dieser Seite lernst
Du lernst, wie man die Lage eines Gleichgewichts mit verschieden langen Pfeilen sichtbar macht. Das Kollisionsmodell erklärt, warum die Reaktionsgeschwindigkeit vom Produkt der Konzentrationen abhängt – und warum ein Katalysator zwar schneller zum Gleichgewicht führt, es aber nicht verschiebt.
Grundlagen aus diesem Kapitel
Die Merkmale des dynamischen Gleichgewichts: → Merkmale eines chemischen Gleichgewichts · Konkret am Beispiel des Estergleichgewichts: → Estergleichgewicht
2.6 Schreibweise für Gleichgewichtsreaktionen
Die Lage des Gleichgewichts lässt sich durch unterschiedlich lange Gleichgewichtspfeile visualisieren. Am Beispiel des Estergleichgewichts (S = Säure, A = Alkohol, E = Ester, W = Wasser):
↑ Zum Vergrößern klicken
✕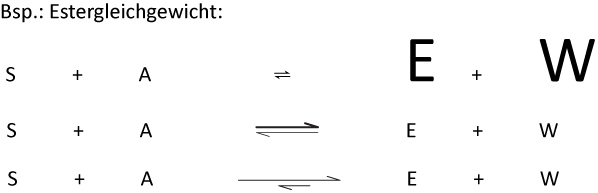
Merksatz – Pfeilnotation
- Gleich lange Pfeile (⇌): Gleichgewicht liegt in der Mitte – ähnlich viele Edukte wie Produkte.
- Längerer Pfeil nach rechts (⟹): Gleichgewicht liegt auf der Produktseite – Produkte überwiegen.
- Längerer Pfeil nach links (⟸): Gleichgewicht liegt auf der Eduktseite – Edukte überwiegen.
2.7 Kollisionsmodell und Reaktionsgeschwindigkeit
Das Kollisionsmodell erklärt, warum die Reaktionsgeschwindigkeit vom Produkt der Konzentrationen der Reaktionspartner abhängt. Entscheidend ist die Anzahl der möglichen Zusammenstöße (Treffermöglichkeiten) zwischen Edukt-Teilchen:
↑ Zum Vergrößern klicken
✕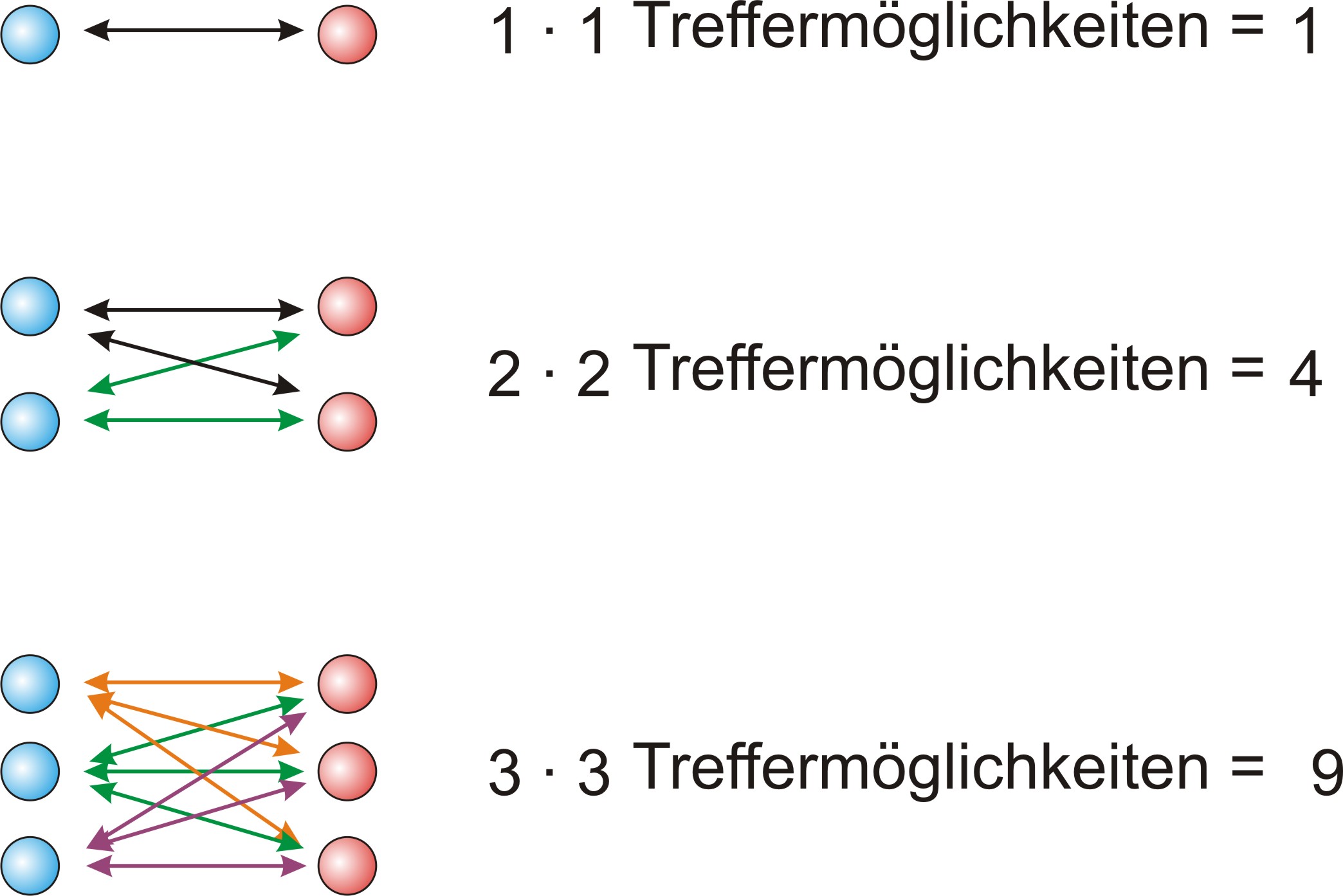
Das Kollisionsmodell liefert die Grundlage für das Massenwirkungsgesetz: Die Geschwindigkeit der Hinreaktion ist proportional zum Produkt der Edukt-Konzentrationen, die der Rückreaktion proportional zum Produkt der Produkt-Konzentrationen.
Aktivierungsenergie und Katalysator
Das Energiediagramm zeigt, wie ein Katalysator die Aktivierungsenergie senkt und damit die Reaktion beschleunigt:
↑ Zum Vergrößern klicken
✕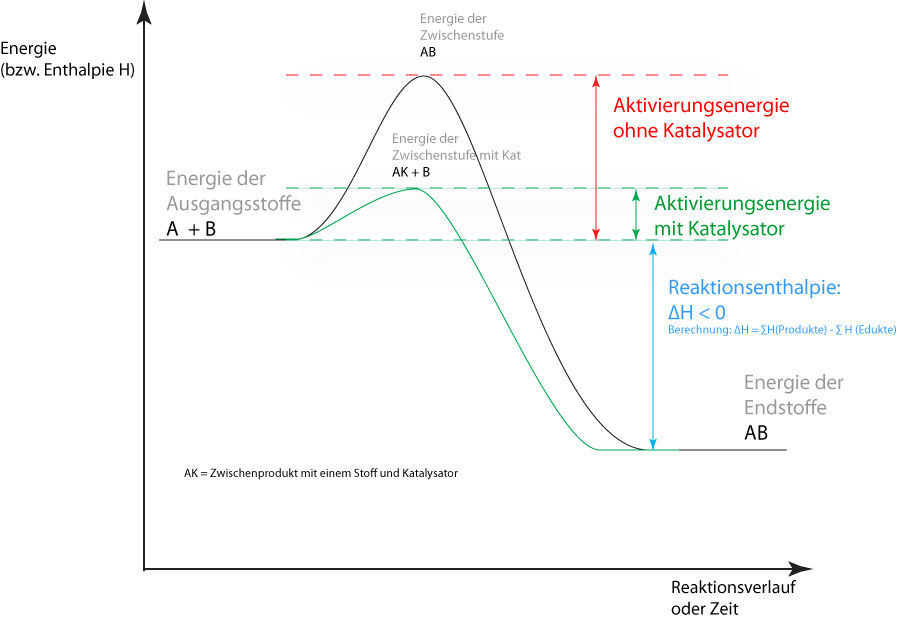
Wichtiger Hinweis zum Katalysator: Ein Katalysator senkt die Aktivierungsenergie für Hin- und Rückreaktion gleichermaßen. Er beschleunigt das Erreichen des Gleichgewichts – verschiebt es aber nicht. Die Lage des Gleichgewichts (Kc-Wert) bleibt durch einen Katalysator unverändert.
Auf einen Blick – die wichtigsten Aussagen
Pfeilnotation
Die Länge der Gleichgewichtspfeile zeigt die Lage des Gleichgewichts: Längerer Pfeil = bevorzugte Reaktionsrichtung.
Kollisionsmodell
Treffermöglichkeiten = n(A) · n(B). Verdoppelt man beide Konzentrationen, vervierfacht sich die Reaktionsrate (2·2 = 4).
Aktivierungsenergie
Ein Katalysator senkt die Aktivierungsenergie über ein energieärmeres Zwischenprodukt (AK). Die Reaktionsenthalpie ΔH bleibt unverändert.
Katalysator ≠ Verschiebung
Ein Katalysator beschleunigt Hin- und Rückreaktion gleichermaßen. Er bringt das System schneller ins Gleichgewicht – verschiebt es aber nicht.
Häufige Fragen – Schreibweise und Kollisionsmodell
Was bedeutet es, wenn ein Gleichgewichtspfeil länger ist als der andere?
Ein längerer Pfeil zeigt die bevorzugte Reaktionsrichtung an. Zeigt der längere Pfeil nach rechts (→⇌), liegt das Gleichgewicht auf der Produktseite – es bilden sich mehr Produkte als Edukte. Zeigt er nach links (⇌←), überwiegen die Edukte. Gleich lange Pfeile (⇌) bedeuten: ähnlich viele Edukte und Produkte im Gleichgewicht. Das genaue Verhältnis beschreibt der Kc-Wert.
Was besagt das Kollisionsmodell für Gleichgewichtsreaktionen?
Die Geschwindigkeit einer Reaktion hängt davon ab, wie oft sich Teilchen treffen und zusammenstoßen. Die Anzahl der Treffermöglichkeiten ist proportional zum Produkt der Teilchenzahlen (bzw. Konzentrationen) der Reaktionspartner: Wenn n(A) = 2 und n(B) = 2, gibt es 2 · 2 = 4 Treffermöglichkeiten. Bei n(A) = 3 und n(B) = 3 sind es 3 · 3 = 9. Dieses Prinzip bildet die Grundlage des Massenwirkungsgesetzes.
Was passiert mit der Reaktionsgeschwindigkeit, wenn man eine Konzentration verdoppelt?
Für die Reaktion A + B → Produkte gilt nach dem Kollisionsmodell: v ∝ [A] · [B]. Verdoppelt man nur [A] (von 1 auf 2), verdoppeln sich die Treffermöglichkeiten. Verdoppelt man beide Konzentrationen, vervierfachen sich die Treffermöglichkeiten (2 · 2 = 4). Die Reaktionsgeschwindigkeit steigt also quadratisch, wenn man beide Eduktkonzentrationen verdoppelt. Wichtig: Das gilt analog für die Rückreaktion mit den Produktkonzentrationen.
Wie wirkt ein Katalysator auf die Aktivierungsenergie – und warum verschiebt er das Gleichgewicht nicht?
Ein Katalysator bildet ein energieärmeres Zwischenprodukt (AK) mit einem der Reaktionspartner. Dadurch ist die Aktivierungsenergie für die Hinreaktion und für die Rückreaktion gleichermaßen kleiner. Beide Reaktionen werden schneller – aber im gleichen Verhältnis. Da sich beide Geschwindigkeiten proportional ändern, bleibt das Gleichgewicht (Kc) unverändert.
Merksatz: Ein Katalysator verändert nicht, wo das Gleichgewicht liegt, sondern nur, wie schnell es erreicht wird. Mehr zur Verschiebung des Gleichgewichts: Prinzip von Le Chatelier.Was ist der Unterschied zwischen Reaktionsenthalpie ΔH und Aktivierungsenergie EA?
Die Reaktionsenthalpie ΔH ist der Energieunterschied zwischen Edukten und Produkten – sie beschreibt, ob eine Reaktion exotherm (ΔH < 0) oder endotherm (ΔH > 0) ist. Die Aktivierungsenergie EA ist die Energiebarriere, die Teilchen überwinden müssen, damit die Reaktion überhaupt abläuft. Ein Katalysator senkt EA, ändert aber nicht ΔH. Die thermodynamischen Hintergründe zu ΔH findest du in der Energetik: Enthalpie H.
Lernkarten – Schreibweise und Kollisionsmodell
Klicke auf eine Karte, um die Antwort zu sehen.
1Was zeigt ein längerer Pfeil auf der rechten Seite des Gleichgewichtspfeils (A ⇌⟹ B) an?
Das Gleichgewicht liegt auf der Produktseite. Es überwiegen die Produkte. Kc > 1.
2Wie viele Treffermöglichkeiten gibt es bei 4 blauen und 4 roten Teilchen?
4 · 4 = 16 Treffermöglichkeiten. Allgemein: Treffermöglichkeiten = n(A) · n(B).
3Erkläre: Warum ändert ein Katalysator die Lage des Gleichgewichts nicht?
Ein Katalysator senkt die Aktivierungsenergie für Hin- UND Rückreaktion gleichermaßen. Beide Geschwindigkeiten steigen im gleichen Verhältnis → Kc bleibt unverändert.
4Was ändert ein Katalysator, was ändert er nicht?
Ändert: Aktivierungsenergie EA (senkt sie) · Reaktionsgeschwindigkeit (erhöht sie) · Zeit bis zum GG (verkürzt sie)
Ändert nicht: ΔH · Kc · Gleichgewichtslage5Bei 25 °C beträgt Kc für A ⇌ B = 9. Im GG gilt [A] = 0,3 mol/L. Berechne [B] und zeichne die passenden Gleichgewichtspfeile.
Kc = [B]/[A] = 9
[B] = 9 · 0,3 = 2,7 mol/L
Produkte überwiegen stark → längerer Pfeil rechts (A ⇌⟹ B)Weiter im Kapitel Gleichgewichtsreaktionen
← Estergleichgewicht → Benzoesäure-Gleichgewicht
🔁 Verwandte Seiten: Massenwirkungsgesetz · Prinzip von Le Chatelier · Enthalpie H (Energetik)
-
4.3.2 Cellulose
4.3.2 Cellulose
Vorkommen: Cellulose ist das in der Natur am häufigsten auftretende Kohlenhydrat. Sie ist die Gerüstsubstanz in der Pflanzenwelt.
z.B.: Baumwolle, Flachs, Hanf (fast 100%); Stroh (30%); Holz (40-50% Cellulose).
Eigenschaften: Cellulose ist eine weiße, in Wasser und in den meisten organischen Lösungsmitteln unlösliche Substanz.
Hydrolyse der Cellulose:
a) Versuch: Filterpapierschnitzel werden mit konz. Salzsäure übergossen. Diese Mischung gibt man in 50 mL Wasser und erhitzt etwa 10 Minuten.
Anschließend wird die Fehlingsche Probe durchgeführt.
Beobachtung: roter Niederschlag
b) Versuch: GOD-Test mit der hydrolisierten Cellulose.
Beobachtung: Grünfärbung des Teststreifens.Folgerung: Cellulose enthält als Baustein D-Glucose.
c) Versuch: Dünnschichtchromatographie
Ein Chromatogramm gibt genauen Aufschluss über die Bausteine: Glucose. Bei vorsichtiger Hydrolyse ist außer β-D-Glucose auch noch Cellobiose nachweisbar (Cellobiose ist ein Disaccharid aus 2 ∙ β-D-Glucosemolekülen).
Aufbau eines Cellulosemoleküls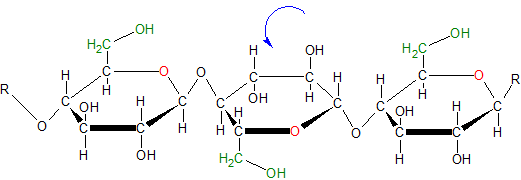
CellobioseAusschließlich β-(1,4)-glycosidische Bindung
Bei der Cellulose handelt es sich um fadenförmig gestreckes Makromoleküle. Diese Makromoleküle lagern sich zu Elementarfibrillen zusammen (H-Brücken).
4.3.3 Unterschied: Cellulose – Stärkea) Räumlich unterschiedliche Verknüpfung der Glucoseringe in den Makromolekülen
Cellulose: (-Glu-Glu-Glu-Glu- verknüpft β 1→4)
Stärke (z.B. Amylose) (-Glu-Glu-Glu-Glu- verknüpft α 1→4 )
b) Unterschiedliche Anordnung der Makromoleküle
Cellulose: langgestreckte, unverzweigte Kettenmoleküle
Stärke: verzweigte Kettenmoleküle, die spiralig aufgerollt sind.
c) Unterschiedliche Molekülmasse
Cellulose: bis 1,8 Millionen u
Stärke: bis 50 000 u4.3.4 Verwendung der Cellulose
Nahrungsmittel: Der Mensch kann β-1,4-Bindungen der Cellulose nicht abbauen ( → Ballaststoffe).
Im Dickdarm schaffen das anaerobe Bakterien→ Umwandlung in Fettsäuren → Resorption.
Kühe: Pansen: Mikroorganismen → Celluloseverdauung
Pferde u.a. Dickdarm
Einige Pilze und Silberfischchen (eine der wenigen Tiere mit eigenen Cellulasen).
Wichtigste Textilfasern: Baumwolle.
Aus Hanf, Flachs, Jute werden Leinen, Säcke, Segeltuch, Matten usw. hergestellt.
Papier
4.3.4 Derivate der Cellulose
a) Cellulose – Kunstseiden
b) Schießbaumwolle (Christian Friedrich Schönbein, Metzinger Chemiker, geb. 1799).
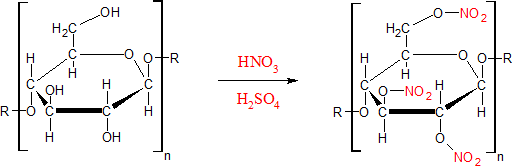
Schießbaumwolle ist Cellulosenitrat (fälschlicherweise als Nitrocellulose bezeichnet).
Herstellung der Schießbaumwolle: 20 mL konz. H2SO4 + 10 ml rauchende HNO3 zur Kühlung kaltes Wasserbad; 2 g Watte dazugeben und mit Galsstab umrühren. Nach 10 Minuten wird die veresterte Watte nur gut mit Wasser ausgewaschen und anschließend im Exsikkator getrocknet.
Schießbaumwolle ist Grundlage für raucharmes Schießpulver, welches das Schwarzpulver ersetzte. z.T. mit Nitroglycerin versetzt dient die Schießbaumwolle als Sprengmittel mit einem Initialzünder.erbrennung
Normale Watte, die fast ausschließlich aus Cellulose besteht, ist nur schwer brennbar. Schießbaumwolle verbrennt explosionsartig mit einer Stichflamme. Bei der Verbrennung der Schießbaumwolle werden große Mengen stabiler Gase frei, die durch ihre Ausdehnung zu einer Druckwelle führen, die typischerweise eine Explosion begleitet. Die entstandenen Gase sind Stickstoff (N2), Stickoxide (NOx) , Kohlenstoffmonoxid (CO), sowie Kohlendioxid (CO2).
Reaktionsgleichung der Herstellung von Nitriersäure
Summenformeln:
2 H2SO4 + HNO3 → NO2+ + H3O1+ + HSO41-
Herstellung von Schießbaumwolle: